2026年天利38套学业水平考试高中化学全一册人教版江苏专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年天利38套学业水平考试高中化学全一册人教版江苏专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第6页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
30.侯氏制碱法的主要产品是$Na_2CO_3$(可能含有碳酸氢钠杂质)。某兴趣小组为测定制得纯碱样品中碳酸钠的质量分数,设计了如下所示的实验方案:
方案一:采用如图所示实验装置,加热$m$g样品至恒重,测定相关数据。
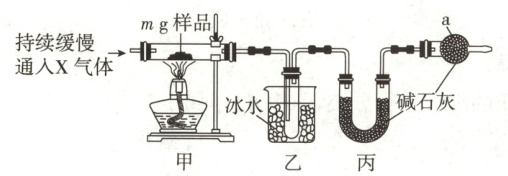
方案二:称量3.600 g样品,配制成100 mL溶液;取其中20.00 mL溶液置于锥形瓶中,滴加甲基橙作指示剂;加入1 mol/L的盐酸溶液,恰好完全反应时消耗盐酸体积为13.00 mL。
回答下列问题:
(1)方案一中:
①X气体选择$N_2$,不选空气的原因是 。
②仪器a的名称是 。
③实验需先通一段时间X气体,再加热样品。若要准确计算样品中碳酸钠的质量分数,还需要提供一个数据,它可以是 (填写字母序号)。
A.加热前后,甲装置的质量变化
B.加热前后,乙、丙装置的质量变化总和
C.加热前后,a处的质量变化
(2)方案二中:
①发生反应的化学方程式是
(写出一种即可)。
②根据该实验方案计算样品中碳酸钠的质量分数,写出计算过程(结果保留一位小数)。
方案一:采用如图所示实验装置,加热$m$g样品至恒重,测定相关数据。

方案二:称量3.600 g样品,配制成100 mL溶液;取其中20.00 mL溶液置于锥形瓶中,滴加甲基橙作指示剂;加入1 mol/L的盐酸溶液,恰好完全反应时消耗盐酸体积为13.00 mL。
回答下列问题:
(1)方案一中:
①X气体选择$N_2$,不选空气的原因是 。
空气中含有的 CO₂、H₂O 等会影响实验数据测定结果准确性
②仪器a的名称是 。
球形干燥管
③实验需先通一段时间X气体,再加热样品。若要准确计算样品中碳酸钠的质量分数,还需要提供一个数据,它可以是 (填写字母序号)。
A 或 B
A.加热前后,甲装置的质量变化
B.加热前后,乙、丙装置的质量变化总和
C.加热前后,a处的质量变化
(2)方案二中:
①发生反应的化学方程式是
Na₂CO₃ + 2HCl ══ 2NaCl + H₂O + CO₂↑ 或 NaHCO₃ + HCl ══ NaCl + H₂O + CO₂↑
(写出一种即可)。
②根据该实验方案计算样品中碳酸钠的质量分数,写出计算过程(结果保留一位小数)。
答案:
30
(1)① 空气中含有的 CO₂、H₂O 等会影响实验数据测定结果准确性 ② 球形干燥管 ③ A 或 B
(2)① Na₂CO₃ + 2HCl ══ 2NaCl + H₂O + CO₂↑ 或 NaHCO₃ + HCl ══ NaCl + H₂O + CO₂↑
② 解:设 3.600 g 样品中含有 Na₂CO₃ x mol,NaHCO₃ y mol。
106x + 84y = 3.600 g
2x + y = 0.013 mol × 100.00 mL / 20.00 mL
解得:x = 0.03 y = 0.005
样品中 Na₂CO₃ 的质量分数为 0.03 mol × 106 g/mol / 3.600 g × 100% ≈ 88.3%
【解析】化学实验与计算
(1)① NaHCO₃ 受热分解生成 Na₂CO₃、H₂O 和 CO₂,乙中冰水浴中的试管用于得到水,丙中碱石灰用于吸收 CO₂,而装置 a(球形干燥管)用于吸收空气中的 CO₂ 和水蒸气,所以通 N₂ 而不通空气的原因是空气中含有的 CO₂、H₂O 等会影响实验数据测定结果的准确性。③ 加热前后甲装置的质量差为生成的 H₂O 和 CO₂ 的质量之和,根据质量差可求算出 NaHCO₃ 的质量,A 正确;加热前后乙和丙装置质量之和的变化也为生成的 H₂O 和 CO₂ 的质量之和,B 正确;加热前后 a 处的质量变化是吸收空气中 H₂O 和 CO₂ 的质量之和,C 错误。
(2)① Na₂CO₃、NaHCO₃ 都能与 HCl 反应:Na₂CO₃ + 2HCl ══ 2NaCl + H₂O + CO₂↑、NaHCO₃ + HCl ══ NaCl + H₂O + CO₂↑。② 通过反应消耗的盐酸的物质的量和称量固体的量联立方程式求出 Na₂CO₃ 与 NaHCO₃ 的物质的量,最终可得 Na₂CO₃ 的质量分数。
(1)① 空气中含有的 CO₂、H₂O 等会影响实验数据测定结果准确性 ② 球形干燥管 ③ A 或 B
(2)① Na₂CO₃ + 2HCl ══ 2NaCl + H₂O + CO₂↑ 或 NaHCO₃ + HCl ══ NaCl + H₂O + CO₂↑
② 解:设 3.600 g 样品中含有 Na₂CO₃ x mol,NaHCO₃ y mol。
106x + 84y = 3.600 g
2x + y = 0.013 mol × 100.00 mL / 20.00 mL
解得:x = 0.03 y = 0.005
样品中 Na₂CO₃ 的质量分数为 0.03 mol × 106 g/mol / 3.600 g × 100% ≈ 88.3%
【解析】化学实验与计算
(1)① NaHCO₃ 受热分解生成 Na₂CO₃、H₂O 和 CO₂,乙中冰水浴中的试管用于得到水,丙中碱石灰用于吸收 CO₂,而装置 a(球形干燥管)用于吸收空气中的 CO₂ 和水蒸气,所以通 N₂ 而不通空气的原因是空气中含有的 CO₂、H₂O 等会影响实验数据测定结果的准确性。③ 加热前后甲装置的质量差为生成的 H₂O 和 CO₂ 的质量之和,根据质量差可求算出 NaHCO₃ 的质量,A 正确;加热前后乙和丙装置质量之和的变化也为生成的 H₂O 和 CO₂ 的质量之和,B 正确;加热前后 a 处的质量变化是吸收空气中 H₂O 和 CO₂ 的质量之和,C 错误。
(2)① Na₂CO₃、NaHCO₃ 都能与 HCl 反应:Na₂CO₃ + 2HCl ══ 2NaCl + H₂O + CO₂↑、NaHCO₃ + HCl ══ NaCl + H₂O + CO₂↑。② 通过反应消耗的盐酸的物质的量和称量固体的量联立方程式求出 Na₂CO₃ 与 NaHCO₃ 的物质的量,最终可得 Na₂CO₃ 的质量分数。
查看更多完整答案,请扫码查看


