第69页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
7. 化学兴趣小组同学进行如图所示的数字化实验。下列有关说法中正确的是(
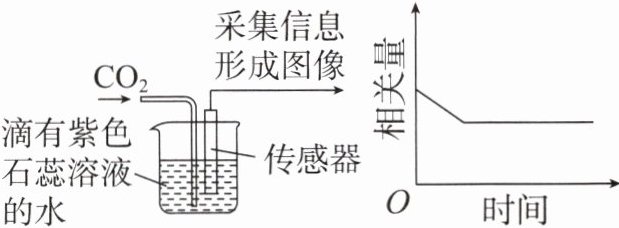
A.实验中可观察到烧杯中溶液变为蓝色
B.反应的化学方程式为$CO_2+H_2O = H_2CO_3$
C.该实验说明二氧化碳气体的密度比空气的密度大
D.纵坐标(相关量)可表示烧杯中物质的总质量
B
)
A.实验中可观察到烧杯中溶液变为蓝色
B.反应的化学方程式为$CO_2+H_2O = H_2CO_3$
C.该实验说明二氧化碳气体的密度比空气的密度大
D.纵坐标(相关量)可表示烧杯中物质的总质量
答案:
7.B 解析:A项,二氧化碳与水反应生成碳酸,碳酸显酸性,使紫色石蕊溶液变红;B项,二氧化碳与水反应生成碳酸,反应的化学方程式为${CO2 + H2O=H2CO3}$;C项,该实验说明二氧化碳能与水反应,但不能说明二氧化碳气体的密度比空气的密度大;D项,若纵坐标(相关量)表示烧杯中物质的总质量,二氧化碳与水反应生成碳酸,则烧杯中物质的总质量会增加。
8. (创新实验)某兴趣小组利用如图所示装置探究二氧化碳的性质。
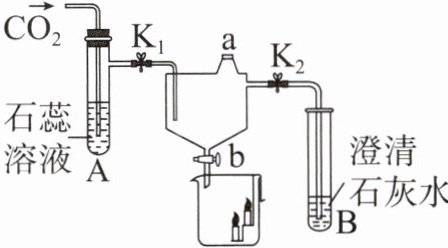
(1)他们先打开弹簧夹$K_1$和$K_2,$关闭活塞a、b,通入$CO_2,$观察到试管A中溶液变为
(2)停止通$CO_2,$关闭弹簧夹$K_1$和$K_2,$打开活塞a、b,观察到烧杯中低处的蜡烛先熄灭,高处的蜡烛后熄灭,说明二氧化碳具有的性质是密度大于空气的密度,不可燃,
(3)最后,打开弹簧夹$K_1、$$K_2,$加热试管A中的溶液,观察到的现象是

(1)他们先打开弹簧夹$K_1$和$K_2,$关闭活塞a、b,通入$CO_2,$观察到试管A中溶液变为
红
色,试管B中发生反应的化学方程式为${CO2 + Ca(OH)2=CaCO3↓ + H2O}$
。(2)停止通$CO_2,$关闭弹簧夹$K_1$和$K_2,$打开活塞a、b,观察到烧杯中低处的蜡烛先熄灭,高处的蜡烛后熄灭,说明二氧化碳具有的性质是密度大于空气的密度,不可燃,
不支持燃烧
。(3)最后,打开弹簧夹$K_1、$$K_2,$加热试管A中的溶液,观察到的现象是
溶液由红色变为紫色
。
答案:
(1)红 ${CO2 + Ca(OH)2=CaCO3↓ + H2O}$
(2)不支持燃烧
(3)溶液由红色变为紫色解析:
(1)先打开弹簧夹${K1}$和${K2}$,关闭活塞a、b,通入${CO2}$,试管A中二氧化碳与水反应生成碳酸,碳酸呈酸性,能使紫色石蕊溶液变红,则观察到试管A中溶液变为红色,试管B中二氧化碳与澄清石灰水中的氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为${CO2 + Ca(OH)2=CaCO3↓ + H2O}$。
(2)停止通${CO2}$,关闭弹簧夹${K1}$和${K2}$,打开活塞a、b,观察到烧杯中低处的蜡烛先熄灭,高处的蜡烛后熄灭,说明二氧化碳具有的性质是密度大于空气的密度,不可燃,不支持燃烧。
(3)加热试管A中的溶液,碳酸在受热的条件下分解生成二氧化碳和水,红色溶液重新变为紫色。
(1)红 ${CO2 + Ca(OH)2=CaCO3↓ + H2O}$
(2)不支持燃烧
(3)溶液由红色变为紫色解析:
(1)先打开弹簧夹${K1}$和${K2}$,关闭活塞a、b,通入${CO2}$,试管A中二氧化碳与水反应生成碳酸,碳酸呈酸性,能使紫色石蕊溶液变红,则观察到试管A中溶液变为红色,试管B中二氧化碳与澄清石灰水中的氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为${CO2 + Ca(OH)2=CaCO3↓ + H2O}$。
(2)停止通${CO2}$,关闭弹簧夹${K1}$和${K2}$,打开活塞a、b,观察到烧杯中低处的蜡烛先熄灭,高处的蜡烛后熄灭,说明二氧化碳具有的性质是密度大于空气的密度,不可燃,不支持燃烧。
(3)加热试管A中的溶液,碳酸在受热的条件下分解生成二氧化碳和水,红色溶液重新变为紫色。
9. (数字化实验)某学习小组设计如下实验验证$CO_2$的性质。
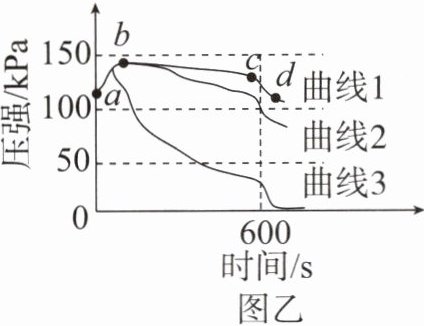
操作步骤:用3个250mL的烧瓶收集满$CO_2$进行实验。如图甲所示,同时迅速将注射器内液体全部注入各个烧瓶中,关闭活塞;一段时间后,同时振荡三个烧瓶。对应得到如图乙所示的烧瓶内压强与时间的关系曲线图。

回答下列问题。
(1)操作步骤中,曲线1、2、3中导致气压快速变小(如cd段)的操作是
(2)曲线2对应发生反应的化学方程式为
(3)根据实验结果,为了充分吸收二氧化碳气体最好选用
(4)在0~600s第一个烧瓶内压强基本没变,说明1体积水大约溶解
操作步骤:用3个250mL的烧瓶收集满$CO_2$进行实验。如图甲所示,同时迅速将注射器内液体全部注入各个烧瓶中,关闭活塞;一段时间后,同时振荡三个烧瓶。对应得到如图乙所示的烧瓶内压强与时间的关系曲线图。


回答下列问题。
(1)操作步骤中,曲线1、2、3中导致气压快速变小(如cd段)的操作是
振荡烧瓶
。(2)曲线2对应发生反应的化学方程式为
${Ca(OH)2 + CO2=CaCO3↓ + H2O}$
。(3)根据实验结果,为了充分吸收二氧化碳气体最好选用
${NaOH}$
溶液。(4)在0~600s第一个烧瓶内压强基本没变,说明1体积水大约溶解
1
体积的二氧化碳。
答案:
(1)振荡烧瓶
(2)${Ca(OH)2 + CO2=CaCO3↓ + H2O}$
(3)${NaOH}$
(4)1解析:
(1)曲线1、2、3中导致气压快速变小(如cd段)的操作是振荡烧瓶,使二氧化碳充分反应,瓶内压强快速减小。
(2)曲线2对应发生的反应是二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为${Ca(OH)2 + CO2=CaCO3↓ + H2O}$。
(3)由烧瓶内压强与时间的关系曲线图可知,曲线3压强变化最大,吸收效果最好,根据实验结果,为了充分吸收二氧化碳气体最好选用${NaOH}$溶液。
(4)加入的水也占有一定的体积,在0~600s第一个烧瓶内压强基本没变,说明1体积水大约溶解1体积的二氧化碳。
(1)振荡烧瓶
(2)${Ca(OH)2 + CO2=CaCO3↓ + H2O}$
(3)${NaOH}$
(4)1解析:
(1)曲线1、2、3中导致气压快速变小(如cd段)的操作是振荡烧瓶,使二氧化碳充分反应,瓶内压强快速减小。
(2)曲线2对应发生的反应是二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为${Ca(OH)2 + CO2=CaCO3↓ + H2O}$。
(3)由烧瓶内压强与时间的关系曲线图可知,曲线3压强变化最大,吸收效果最好,根据实验结果,为了充分吸收二氧化碳气体最好选用${NaOH}$溶液。
(4)加入的水也占有一定的体积,在0~600s第一个烧瓶内压强基本没变,说明1体积水大约溶解1体积的二氧化碳。
查看更多完整答案,请扫码查看


