7. 某同学在整理实验器材时,将还在反应的锌和稀硫酸的残留物,倒入有少量硫酸铜溶液的废液缸中,观察到锌粒表面产生气泡的速度大大加快。与硫酸铜溶液混合怎么会加快锌和稀硫酸的反应速度呢?对此,他查阅资料得知:①相互接触的两种活动性不同的金属,同时放入酸中,活动性较强的金属与酸反应产生氢气的速度会大大加快。②硫酸铜对锌和稀硫酸反应没有催化作用。然后,该同学根据下表进行实验,观察并记录现象。
|组别|第一组|第二组|
||A|B|C|D|
|金属|锌片|绑有铜片的锌片|铁片|绑有铜片的铁片|
|30%硫酸溶液/毫升|20|?|20|20|
|产生气泡快慢|快|明显加快|慢|明显加快|
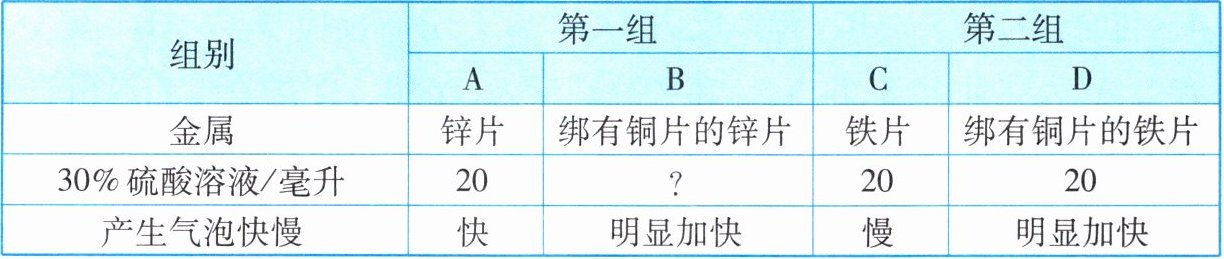
(1)第一组实验中“?”处的数据应为
(2)为了定量比较产生气体的快慢,可以测量“相同时间收集到氢气的体积”或测量
(3)请推测与废液缸中少量硫酸铜溶液混合后,锌与稀硫酸反应速度加快的原因是
|组别|第一组|第二组|
||A|B|C|D|
|金属|锌片|绑有铜片的锌片|铁片|绑有铜片的铁片|
|30%硫酸溶液/毫升|20|?|20|20|
|产生气泡快慢|快|明显加快|慢|明显加快|

(1)第一组实验中“?”处的数据应为
20
。 (2)为了定量比较产生气体的快慢,可以测量“相同时间收集到氢气的体积”或测量
收集相同体积的氢气所需的时间
,然后进行比较。 (3)请推测与废液缸中少量硫酸铜溶液混合后,锌与稀硫酸反应速度加快的原因是
硫酸铜与锌发生置换反应产生的铜附着在锌粒表面,加快了锌与稀硫酸的反应速度
。
答案:
(1) 20
(2) 收集相同体积的氢气所需的时间
(3) 硫酸铜与锌发生置换反应产生的铜附着在锌粒表面,加快了锌与稀硫酸的反应速度
(1) 20
(2) 收集相同体积的氢气所需的时间
(3) 硫酸铜与锌发生置换反应产生的铜附着在锌粒表面,加快了锌与稀硫酸的反应速度
8. 为比较镁和铝的金属活动性强弱,某科学学习小组进行了如下实验。
(1)准备两根表面积相同的镁条和铝条,并除去表面的氧化膜。要求两种金属片表面积相同的目的是
(2)方案一:将除去氧化膜的镁条、铝条,分别与体积和质量分数均相同的硫酸反应,观察到镁比铝反应更剧烈,说明
(3)方案二:连接仪器组装成如图所示的实验装置。某同学用抽拉法检查该装置的气密性,发现被拉出的针筒活塞一段时间后又回到原来的位置,则该装置是否漏气?
(4)请再设计一个简单的、与上述不同的实验方案,比较镁和铝的金属活动性强弱。
(1)准备两根表面积相同的镁条和铝条,并除去表面的氧化膜。要求两种金属片表面积相同的目的是
控制变量
。 (2)方案一:将除去氧化膜的镁条、铝条,分别与体积和质量分数均相同的硫酸反应,观察到镁比铝反应更剧烈,说明
镁的金属活动性比铝强
。 (3)方案二:连接仪器组装成如图所示的实验装置。某同学用抽拉法检查该装置的气密性,发现被拉出的针筒活塞一段时间后又回到原来的位置,则该装置是否漏气?
不漏气
。要比较两种金属的活动性强弱,可以测定两种金属与硫酸反应得到相同体积氢气所需要的时间,也可以测定相同时间内产生的氢气体积
。 (4)请再设计一个简单的、与上述不同的实验方案,比较镁和铝的金属活动性强弱。
将除去表面氧化膜的镁条、铝条分别在空气中点燃,比较燃烧的剧烈程度。
答案:
(1) 控制变量
(2) 镁的金属活动性比铝强
(3) 不漏气 相同时间内产生的氢气体积
(4) 将除去表面氧化膜的镁条、铝条分别在空气中点燃,比较燃烧的剧烈程度。
(1) 控制变量
(2) 镁的金属活动性比铝强
(3) 不漏气 相同时间内产生的氢气体积
(4) 将除去表面氧化膜的镁条、铝条分别在空气中点燃,比较燃烧的剧烈程度。
查看更多完整答案,请扫码查看


