第23页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
9. 小明发现金属钠在二氧化碳中燃烧生成黑色颗粒和白色固体物质。经查证黑色颗粒成分是碳,但不清楚白色固体成分是什么,于是进行了如下探究:
【提出问题】白色固体的成分是什么?
【建立假设】
假设一:白色固体的成分是氧化钠。
假设二:白色固体的成分是碳酸钠。
假设三:白色固体的成分是氧化钠和碳酸钠。
假设四:白色固体的成分是碳酸钙。
【进行实验】步骤一:取适量白色固体于烧杯中并加入适量水,固体全部溶解,形成无色溶液。
步骤二:往步骤一的溶液中滴加氢氧化钙溶液,出现白色沉淀,继续滴加氢氧化钙溶液直至白色沉淀不再产生,将其过滤。
步骤三:用pH试纸检测步骤二中获得的滤液的pH,结果呈碱性。
【查阅资料】氧化钠和水反应生成氢氧化钠(化学方程式:$Na_2O+H_2O= 2NaOH)。$
(1)结合学过的知识和上述信息,写出假设四不成立的依据:
(2)写出步骤三的具体操作:
(3)小明根据实验现象判断假设三成立。请分析小明的判断是否合理,并说明理由:
【提出问题】白色固体的成分是什么?
【建立假设】
假设一:白色固体的成分是氧化钠。
假设二:白色固体的成分是碳酸钠。
假设三:白色固体的成分是氧化钠和碳酸钠。
假设四:白色固体的成分是碳酸钙。
【进行实验】步骤一:取适量白色固体于烧杯中并加入适量水,固体全部溶解,形成无色溶液。
步骤二:往步骤一的溶液中滴加氢氧化钙溶液,出现白色沉淀,继续滴加氢氧化钙溶液直至白色沉淀不再产生,将其过滤。
步骤三:用pH试纸检测步骤二中获得的滤液的pH,结果呈碱性。
【查阅资料】氧化钠和水反应生成氢氧化钠(化学方程式:$Na_2O+H_2O= 2NaOH)。$
(1)结合学过的知识和上述信息,写出假设四不成立的依据:
碳酸钙是不溶于水的白色固体,且反应物中没有钙元素
。(2)写出步骤三的具体操作:
用洁净的玻璃棒蘸取少量滤液,滴到pH试纸上,将试纸显示的颜色与标准比色卡对照
。(3)小明根据实验现象判断假设三成立。请分析小明的判断是否合理,并说明理由:
不合理,滴入氢氧化钙产生白色沉淀说明白色固体中含有碳酸钠,但同时生成氢氧化钠,氢氧化钠溶液显碱性,无法判断白色固体中是否含有氧化钠
。
答案:
(1)碳酸钙是不溶于水的白色固体,且反应物中没有钙元素 (2)用洁净的玻璃棒蘸取少量滤液,滴到pH试纸上,将试纸显示的颜色与标准比色卡对照 (3)不合理,滴入氢氧化钙产生白色沉淀说明白色固体中含有碳酸钠,但同时生成氢氧化钠,氢氧化钠溶液显碱性,无法判断白色固体中是否含有氧化钠
10. 久置的镁带表面会有一层灰黑色固体。为了测量久置镁带中金属镁的质量分数,同学们提出了两种实验方法。
物理方法:取一定质量的镁带,用砂纸打磨,除尽表面的灰黑色固体,根据剩余固体质量计算金属镁的质量分数。
化学方法:取一定质量的镁带,与足量的稀硫酸反应,根据测得生成气体的体积计算金属镁的质量分数。
(1)经讨论,同学们否定了物理方法。理由是打磨过程中______
(2)常温常压下氢气密度已知,因此大家认为化学方法可行。
老师提示:镁与稀硫酸反应放热;灰黑色固体除了氧化镁之外,还存在少量碱式碳酸镁$[MgCO_3·Mg(OH)_2],$它与酸反应会产生$CO_2$气体;碱石灰是CaO和NaOH的混合物。
同学们从如图所示的装置中选择合适的装置,组装并进行实验。
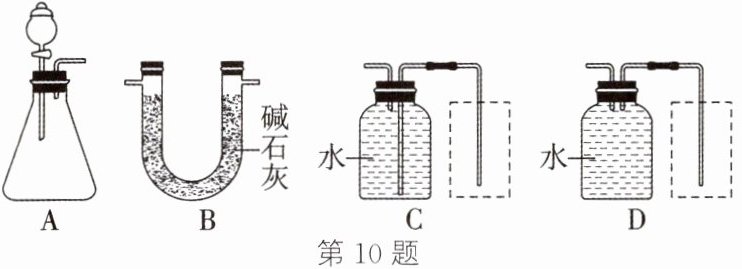
① 装置C、D虚线框内有一种测量体积的仪器(未画出),该仪器是______
② 完成该实验应选择的装置为______
③ 结合实验方法和选择的装置分析,下列会造成实验结果不准确的是______
A. 加入稀硫酸不足,镁带有剩余
B. 装置的气密性不好
C. 反应结束,立即读数
物理方法:取一定质量的镁带,用砂纸打磨,除尽表面的灰黑色固体,根据剩余固体质量计算金属镁的质量分数。
化学方法:取一定质量的镁带,与足量的稀硫酸反应,根据测得生成气体的体积计算金属镁的质量分数。
(1)经讨论,同学们否定了物理方法。理由是打磨过程中______
会磨掉部分金属镁
。(2)常温常压下氢气密度已知,因此大家认为化学方法可行。
老师提示:镁与稀硫酸反应放热;灰黑色固体除了氧化镁之外,还存在少量碱式碳酸镁$[MgCO_3·Mg(OH)_2],$它与酸反应会产生$CO_2$气体;碱石灰是CaO和NaOH的混合物。
同学们从如图所示的装置中选择合适的装置,组装并进行实验。

① 装置C、D虚线框内有一种测量体积的仪器(未画出),该仪器是______
量筒(或量杯)
。② 完成该实验应选择的装置为______
ABC
(填字母)。③ 结合实验方法和选择的装置分析,下列会造成实验结果不准确的是______
ABC
(填字母)。A. 加入稀硫酸不足,镁带有剩余
B. 装置的气密性不好
C. 反应结束,立即读数
答案:
(1)会磨掉部分金属镁 (2)① 量筒(或量杯) ② ABC ③ ABC 解析:
(2)① 实验中常用来测量液体体积的仪器是量筒或量杯。② 由题意可知,实验中的反应物为固液状态且不需要加热,可以选择装置A作为反应容器;为了较为准确地测量生成氢气的体积,需要除去生成的氢气中携带的水蒸气和CO₂,碱石灰能和CO₂及水蒸气反应,且不和H₂反应,所以选择装置B;在用排水法测量气体体积时,应采用短口进、长口出的方式,所以选择装置C。③ 加入稀硫酸不足,镁带有剩余,会导致最终生成氢气的量偏少,计算得到镁的质量分数偏低,A选项符合题意;装置的气密性不好,会导致实验中产生的氢气逸出,测得氢气的体积偏小,计算得到镁的质量分数偏低,B选项符合题意;镁与稀硫酸反应放热,反应结束,立即读数,会导致读数时测得氢气的体积偏大,计算得到镁的质量分数偏高,C选项符合题意。
(2)① 实验中常用来测量液体体积的仪器是量筒或量杯。② 由题意可知,实验中的反应物为固液状态且不需要加热,可以选择装置A作为反应容器;为了较为准确地测量生成氢气的体积,需要除去生成的氢气中携带的水蒸气和CO₂,碱石灰能和CO₂及水蒸气反应,且不和H₂反应,所以选择装置B;在用排水法测量气体体积时,应采用短口进、长口出的方式,所以选择装置C。③ 加入稀硫酸不足,镁带有剩余,会导致最终生成氢气的量偏少,计算得到镁的质量分数偏低,A选项符合题意;装置的气密性不好,会导致实验中产生的氢气逸出,测得氢气的体积偏小,计算得到镁的质量分数偏低,B选项符合题意;镁与稀硫酸反应放热,反应结束,立即读数,会导致读数时测得氢气的体积偏大,计算得到镁的质量分数偏高,C选项符合题意。
查看更多完整答案,请扫码查看


