第10页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
1. 下列物质的用途不是利用酸碱反应的是(
A.用盐酸除铁锈
B.用熟石灰改良酸性土壤
C.用氢氧化铝治疗胃酸过多
D.用氨水处理含有硫酸的废水
A
)A.用盐酸除铁锈
B.用熟石灰改良酸性土壤
C.用氢氧化铝治疗胃酸过多
D.用氨水处理含有硫酸的废水
答案:
A
2. 削山药皮时皮肤会奇痒难忍,这是山药中含有的碱性成分皂角素与皮肤接触造成的,我们可以使用酸性物质止痒。下列物质中可用于止痒的是 (
A.蒸馏水
B.白醋
C.牙膏
D.肥皂水
B
)A.蒸馏水
B.白醋
C.牙膏
D.肥皂水
答案:
B
3. 如图所示为氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论不正确的是 (
A.反应后溶液能使无色酚酞试液变红色
B.反应前后溶液中Na⁺和Cl⁻的个数不变
C.该反应的实质是H⁺和OH⁻结合生成水分子
D.反应前后的溶液均能导电
A
)A.反应后溶液能使无色酚酞试液变红色
B.反应前后溶液中Na⁺和Cl⁻的个数不变
C.该反应的实质是H⁺和OH⁻结合生成水分子
D.反应前后的溶液均能导电
答案:
A
4. 将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,混合溶液的温度变化情况如图所示。
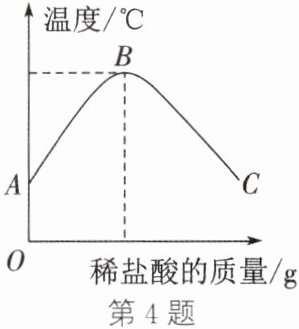
(1) 由图可知,该反应是
(2) 从A到B的过程中,混合溶液的pH逐渐

(1) 由图可知,该反应是
放热
(填“放热”或“吸热”)反应。(2) 从A到B的过程中,混合溶液的pH逐渐
减小
。
答案:
【解析】:
(1) 从图中可以看到,随着稀盐酸的滴入,混合溶液的温度先上升后下降,在B点达到最高。温度上升说明反应过程中有热量放出,因此该反应是放热反应。
(2) 氢氧化钠溶液呈碱性,随着稀盐酸的滴入,氢氧化钠与盐酸发生中和反应,碱性逐渐减弱,pH逐渐减小。
【答案】:
(1) 放热
(2) 减小
(1) 从图中可以看到,随着稀盐酸的滴入,混合溶液的温度先上升后下降,在B点达到最高。温度上升说明反应过程中有热量放出,因此该反应是放热反应。
(2) 氢氧化钠溶液呈碱性,随着稀盐酸的滴入,氢氧化钠与盐酸发生中和反应,碱性逐渐减弱,pH逐渐减小。
【答案】:
(1) 放热
(2) 减小
5. 如图所示的实验可验证酸与碱能发生反应。
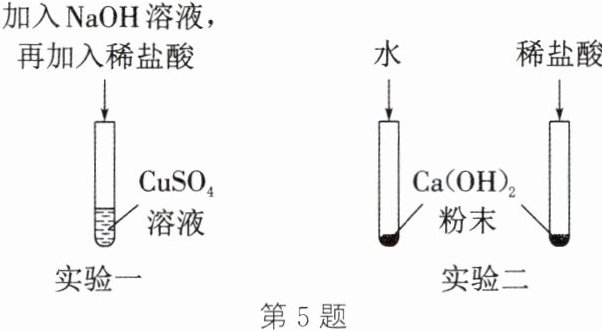
(1) 实验一通过观察稀盐酸与
(2) 实验二通过两支试管中的现象对比,可以判断稀盐酸与Ca(OH)₂能发生反应,该实验除需控制所加水和稀盐酸的温度、体积相同外,还需控制

(1) 实验一通过观察稀盐酸与
Cu(OH)₂
反应的现象,验证了酸与碱能发生反应。(2) 实验二通过两支试管中的现象对比,可以判断稀盐酸与Ca(OH)₂能发生反应,该实验除需控制所加水和稀盐酸的温度、体积相同外,还需控制
Ca(OH)₂粉末的质量
相同。
答案:
(1)Cu(OH)₂ (2)Ca(OH)₂粉末的质量
6. 某校科学小组在利用盐酸和氢氧化钾溶液探究酸碱反应时,将其中一种溶液逐滴加入烧杯中,利用数字化传感器测得烧杯中溶液pH的变化图像如图所示。
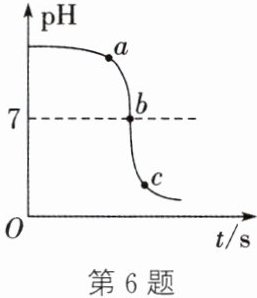
(1) 根据图像分析可知,实验前烧杯中盛有
(2) 向图中c点所示溶液中加入一定量的碳酸钠溶液,待完全反应后所得溶液中一定含有的溶质是

(1) 根据图像分析可知,实验前烧杯中盛有
氢氧化钾
溶液。(2) 向图中c点所示溶液中加入一定量的碳酸钠溶液,待完全反应后所得溶液中一定含有的溶质是
氯化钾、氯化钠
(填名称)。
答案:
(1)氢氧化钾 (2)氯化钾、氯化钠
7. (2023·苏州)常温下,将10 mL5%的NaOH溶液逐滴加入盛有5 mL5%的稀盐酸(含2滴酚酞试液)的锥形瓶中,边滴边振荡。下列有关说法正确的是 (
A.滴加过程中,锥形瓶内溶液中Na⁺的数目不断增加
B.滴加过程中,溶液恰好由无色变为红色时,溶液的pH为7
C.滴加过程中,锥形瓶内溶液温度不断升高
D.滴加结束后,取少量溶液蒸干,所得白色固体是NaCl
A
)A.滴加过程中,锥形瓶内溶液中Na⁺的数目不断增加
B.滴加过程中,溶液恰好由无色变为红色时,溶液的pH为7
C.滴加过程中,锥形瓶内溶液温度不断升高
D.滴加结束后,取少量溶液蒸干,所得白色固体是NaCl
答案:
A 解析:氢氧化钠和盐酸反应生成氯化钠和水,该反应的实质是氢离子和氢氧根离子结合生成水分子,所以滴加过程中,锥形瓶内溶液中Na⁺的数目不断增加,A正确;溶液为红色时,说明滴加的氢氧化钠溶液已过量,此时溶液呈碱性,pH>7,B错误;中和反应放热,反应过程中锥形瓶内溶液温度不断升高,待盐酸完全反应后,再滴加氢氧化钠溶液,溶液温度逐渐下降至室温,C错误;滴加结束后,由于所加的氢氧化钠溶液已过量,所以取少量溶液蒸干,所得白色固体是NaCl和NaOH的混合物,D错误。
查看更多完整答案,请扫码查看


