2025年奔跑吧少年九年级科学全一册浙教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年奔跑吧少年九年级科学全一册浙教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
9. (2023秋·台州市三门县期末)使用果蔬保鲜剂是果蔬保鲜的一种方法。如图甲所示为某果蔬保鲜剂的部分说明,该保鲜剂使用一段时间后成分会有怎样的变化呢?某同学取一包使用一段时间后的保鲜剂按图乙所示的步骤进行实验。(辅料不参与反应)
(第9题)
(1)步骤①的操作是______
(2)若滤液B中含有氢氧化钙,则步骤②中观察到的现象是______
(3)步骤③中产生气泡的化学方程式:______

(第9题)
(1)步骤①的操作是______
过滤
。(2)若滤液B中含有氢氧化钙,则步骤②中观察到的现象是______
无色酚酞试液变红
。(3)步骤③中产生气泡的化学方程式:______
${CaCO_{3} + 2HCl \xlongequal{} CaCl_{2} + H_{2}O + CO_{2} \uparrow}$
。
答案:
(1)过滤
(2)无色酚酞试液变红
(3)${CaCO_{3} + 2HCl \xlongequal{} CaCl_{2} + H_{2}O + CO_{2} \uparrow}$
(1)过滤
(2)无色酚酞试液变红
(3)${CaCO_{3} + 2HCl \xlongequal{} CaCl_{2} + H_{2}O + CO_{2} \uparrow}$
10. (2024秋·湖州市长兴县期末)小科学习了碱和盐的性质后,将少量硫酸铜溶液滴入2毫升氢氧化钠溶液中,没有观察到预期的蓝色絮状沉淀,这是为什么呢?
〔猜想〕猜想一:氢氧化钠与硫酸铜反应放热,使氢氧化铜的溶解度增大。
猜想二:生成的氢氧化铜继续与氢氧化钠发生反应。
〔实验〕实验操作及现象如图所示:
(1)为了验证猜想一,小科应选择
(2)若猜想二正确,则C组中“?”处应填写的现象是
(3)查阅资料得知:氢氧化铜能与氢氧化钠溶液发生反应,生成可溶物。小科再次做硫酸铜溶液与氢氧化钠溶液反应的实验时,他应该怎么做才能立即观察到预期的蓝色絮状沉淀?请你写出一种方法:
(第10题)

〔猜想〕猜想一:氢氧化钠与硫酸铜反应放热,使氢氧化铜的溶解度增大。
猜想二:生成的氢氧化铜继续与氢氧化钠发生反应。
〔实验〕实验操作及现象如图所示:
(1)为了验证猜想一,小科应选择
A、B
两组实验进行对比。根据实验结果,猜想一不成立
(填“成立”或“不成立”)。(2)若猜想二正确,则C组中“?”处应填写的现象是
固体消失
。(3)查阅资料得知:氢氧化铜能与氢氧化钠溶液发生反应,生成可溶物。小科再次做硫酸铜溶液与氢氧化钠溶液反应的实验时,他应该怎么做才能立即观察到预期的蓝色絮状沉淀?请你写出一种方法:
将氢氧化钠溶液滴入硫酸铜溶液中(合理均可)
。(第10题)

答案:
(1)A、B 不成立
(2)固体消失
(3)将氢氧化钠溶液滴入硫酸铜溶液中(合理均可)
(1)A、B 不成立
(2)固体消失
(3)将氢氧化钠溶液滴入硫酸铜溶液中(合理均可)
11. (2024秋·台州市三门县期末)为测出鸡蛋壳中碳酸钙的质量分数,某同学称取已洗净、晾干、研成粉末的鸡蛋壳10克置于烧杯中,将烧杯放在电子天平上,往烧杯中加入足量的稀盐酸,每0.5分钟记录一次电子天平的示数,具体数据如表所示:
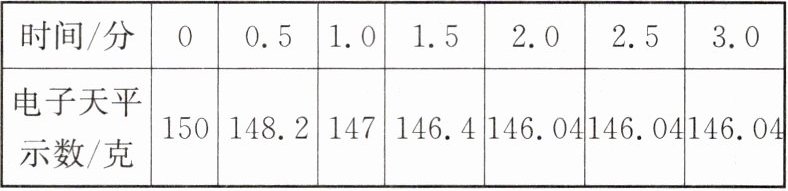
(1)分析表中数据,写出判断鸡蛋壳已经完全反应的理由:
(2)假设产生的气体全部是鸡蛋壳中的碳酸钙与盐酸反应生成的$CO_2,$根据实验结果计算出该鸡蛋壳中碳酸钙的质量分数。
(3)下列情况中,会导致实验中碳酸钙质量分数的测量结果偏小的是
A. 鸡蛋壳未晾干
B. 烧杯中部分水蒸气随二氧化碳逸出
C. 盐酸的溶质质量分数过大
D. 鸡蛋壳碎片太大,未反应完

(1)分析表中数据,写出判断鸡蛋壳已经完全反应的理由:
从 2.0 分钟到 3.0 分钟,电子天平的示数没有发生变化
。(2)假设产生的气体全部是鸡蛋壳中的碳酸钙与盐酸反应生成的$CO_2,$根据实验结果计算出该鸡蛋壳中碳酸钙的质量分数。
由表可知生成的气体的质量为 150 克 - 146.04 克 = 3.96 克。设碳酸钙的质量为$x$。
${CaCO_{3} + 2HCl \xlongequal{} CaCl_{2} + H_{2}O + CO_{2} \uparrow}$
100 44
$x$ 3.96 克
$\frac{100}{44} = \frac{x}{3.96 克}$ $x = 9$克
该鸡蛋壳中碳酸钙的质量分数为$\frac{9 克}{10 克} × 100\% = 90\%$。
${CaCO_{3} + 2HCl \xlongequal{} CaCl_{2} + H_{2}O + CO_{2} \uparrow}$
100 44
$x$ 3.96 克
$\frac{100}{44} = \frac{x}{3.96 克}$ $x = 9$克
该鸡蛋壳中碳酸钙的质量分数为$\frac{9 克}{10 克} × 100\% = 90\%$。
(3)下列情况中,会导致实验中碳酸钙质量分数的测量结果偏小的是
AD
(多选,填字母)。A. 鸡蛋壳未晾干
B. 烧杯中部分水蒸气随二氧化碳逸出
C. 盐酸的溶质质量分数过大
D. 鸡蛋壳碎片太大,未反应完
答案:
(1)从 2.0 分钟到 3.0 分钟,电子天平的示数没有发生变化
(2)由表可知生成的气体的质量为 150 克 - 146.04 克 = 3.96 克。设碳酸钙的质量为$x$。
${CaCO_{3} + 2HCl \xlongequal{} CaCl_{2} + H_{2}O + CO_{2} \uparrow}$
100 44
$x$ 3.96 克
$\frac{100}{44} = \frac{x}{3.96 克}$ $x = 9$克
该鸡蛋壳中碳酸钙的质量分数为$\frac{9 克}{10 克} × 100\% = 90\%$。
(3)AD
(1)从 2.0 分钟到 3.0 分钟,电子天平的示数没有发生变化
(2)由表可知生成的气体的质量为 150 克 - 146.04 克 = 3.96 克。设碳酸钙的质量为$x$。
${CaCO_{3} + 2HCl \xlongequal{} CaCl_{2} + H_{2}O + CO_{2} \uparrow}$
100 44
$x$ 3.96 克
$\frac{100}{44} = \frac{x}{3.96 克}$ $x = 9$克
该鸡蛋壳中碳酸钙的质量分数为$\frac{9 克}{10 克} × 100\% = 90\%$。
(3)AD
查看更多完整答案,请扫码查看


