第47页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
1. 小烧杯中盛有含酚酞的氢氧化钠溶液,逐滴加入稀盐酸至过量,烧杯中溶液颜色变化顺序是 ( )
A. 紫色—红色—蓝色
B. 红色—无色—红色
C. 蓝色—红色
D. 红色—无色
A. 紫色—红色—蓝色
B. 红色—无色—红色
C. 蓝色—红色
D. 红色—无色
答案:
D
2. 在盛有下列固体的试管中,加入足量的稀盐酸,能得到无色溶液的是 ( )
A. Fe
B. Fe₂O₃
C. Cu(OH)₂
D. Na₂CO₃
A. Fe
B. Fe₂O₃
C. Cu(OH)₂
D. Na₂CO₃
答案:
D
3. 研究性学习小组为了探究氢氧化钠溶液与稀硫酸是否恰好完全反应,分别取少量反应后的溶液于试管中,用下表中的不同试剂进行实验。下列选项错误的是 ( )
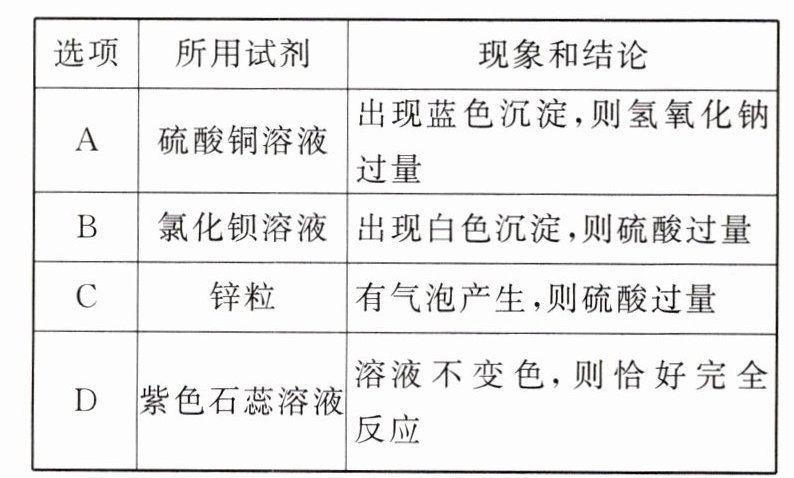

答案:
B
4. 小明同学在学习硫酸的化学性质时,归纳出了稀硫酸与其他物质相互反应的关系,如图(图中直线表示相连的两种物质能发生反应)。

(1)若 X 是与其他三种不同类别的化合物,则 X 可以是 ______(填化学式,只填一种);
(2)根据如图所示物质间的关系,写出①反应的化学方程式:____________。

(1)若 X 是与其他三种不同类别的化合物,则 X 可以是 ______(填化学式,只填一种);
(2)根据如图所示物质间的关系,写出①反应的化学方程式:____________。
答案:
(1)$Fe_{2}O_{3}$(合理即可)
(2)$Zn + H_{2}SO_{4} = ZnSO_{4} + H_{2}\uparrow$
(1)$Fe_{2}O_{3}$(合理即可)
(2)$Zn + H_{2}SO_{4} = ZnSO_{4} + H_{2}\uparrow$
5. 科学探究 小明同学为了进一步加深对“碱的化学性质”的理解,特邀你协助他完成下列活动与探究。
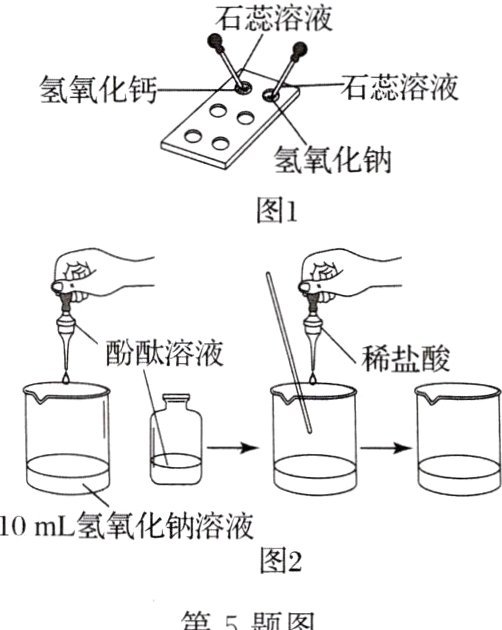
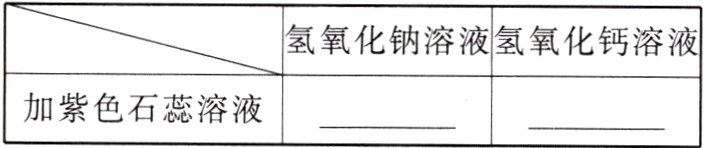
(1)如图 1 所示,在白色点滴板上进行实验,氢氧化钠溶液和氢氧化钙溶液加紫色石蕊溶液;请将实验现象填入下表:
(2)回忆检验二氧化碳气体的反应,写出该反应的化学方程式:____________________;
(3)三氧化硫(SO₃)与氢氧化钠的反应与上面的反应类似,写出这一反应的化学方程式:____________________,该反应______(填“是”或“不是”)复分解反应。
(4)如图 2 所示,在烧杯中加入 10 mL 氢氧化钠溶液,再滴入几滴无色酚酞溶液,溶液显______色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。这一实验说明:酸与碱作用生成了盐和水,这一反应叫作______反应。
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙相似的化学性质(任写两点):①____________;②____________。

(1)如图 1 所示,在白色点滴板上进行实验,氢氧化钠溶液和氢氧化钙溶液加紫色石蕊溶液;请将实验现象填入下表:

(2)回忆检验二氧化碳气体的反应,写出该反应的化学方程式:____________________;
(3)三氧化硫(SO₃)与氢氧化钠的反应与上面的反应类似,写出这一反应的化学方程式:____________________,该反应______(填“是”或“不是”)复分解反应。
(4)如图 2 所示,在烧杯中加入 10 mL 氢氧化钠溶液,再滴入几滴无色酚酞溶液,溶液显______色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。这一实验说明:酸与碱作用生成了盐和水,这一反应叫作______反应。
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙相似的化学性质(任写两点):①____________;②____________。
答案:
(1)溶液变蓝 溶液变蓝
(2)$Ca(OH)_{2} + CO_{2} = CaCO_{3}\downarrow + H_{2}O$
(3)$SO_{3} + 2NaOH = Na_{2}SO_{4} + H_{2}O$ 不是
(4)红 中和
(5)①都能使指示剂变色
②都能与非金属氧化物反应生成盐和水
(1)溶液变蓝 溶液变蓝
(2)$Ca(OH)_{2} + CO_{2} = CaCO_{3}\downarrow + H_{2}O$
(3)$SO_{3} + 2NaOH = Na_{2}SO_{4} + H_{2}O$ 不是
(4)红 中和
(5)①都能使指示剂变色
②都能与非金属氧化物反应生成盐和水
1. 科学种田能有效提高作物产量,助力乡村振兴。草莓适宜生长在弱酸性的土壤中,某地区为种植草莓,对土壤进行检测,“圆梦”活动小组积极参与。请回答下列问题。
取少量土壤样品,加入足量水,搅拌、过滤,测得滤液pH = 8.2,说明土壤呈碱性,由此判断该土壤不适合种植草莓。
【查阅资料】氯化钙和碳酸钠反应产生碳酸钙和氯化钠。
【探究一】土壤中的碱性物质是什么?
结合已有知识,小组同学猜测碱性物质可能是碳酸钠或氢氧化钠中的一种或两种。
【实验探究】
(1)

【探究二】如何改变土壤的碱性?
查阅资料:向土壤中施加硫粉,硫粉在微生物和水的共同作用下最终生成硫酸。
(2)活动小组按照用量要求向试验田中加入硫粉,3个月后,再次测得土壤pH = 6.3,确认可以种植草莓。土壤碱性改变的原因是______(用化学方程式表示)。
【交流反思】(3)针对该地区土壤,除改变其碱性外,还可以选种适合生长的作物。以下作物中,适合在该地区种植的是______。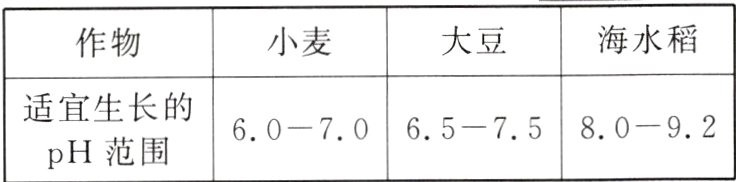
取少量土壤样品,加入足量水,搅拌、过滤,测得滤液pH = 8.2,说明土壤呈碱性,由此判断该土壤不适合种植草莓。
【查阅资料】氯化钙和碳酸钠反应产生碳酸钙和氯化钠。
【探究一】土壤中的碱性物质是什么?
结合已有知识,小组同学猜测碱性物质可能是碳酸钠或氢氧化钠中的一种或两种。
【实验探究】
(1)

【探究二】如何改变土壤的碱性?
查阅资料:向土壤中施加硫粉,硫粉在微生物和水的共同作用下最终生成硫酸。
(2)活动小组按照用量要求向试验田中加入硫粉,3个月后,再次测得土壤pH = 6.3,确认可以种植草莓。土壤碱性改变的原因是______(用化学方程式表示)。
【交流反思】(3)针对该地区土壤,除改变其碱性外,还可以选种适合生长的作物。以下作物中,适合在该地区种植的是______。

答案:
(1)过量氯化钙溶液 滤液不变色
(2)$2NaOH + H_{2}SO_{4} = Na_{2}SO_{4} + 2H_{2}O$
(3)海水稻
(1)过量氯化钙溶液 滤液不变色
(2)$2NaOH + H_{2}SO_{4} = Na_{2}SO_{4} + 2H_{2}O$
(3)海水稻
2. 小强同学家里承包了一块土地,准备种植甘蔗,甘蔗最适宜种植的土壤酸碱度为6.0~8.0。由于担心该地土壤的酸碱性不适合种植甘蔗,邀请化学兴趣小组的同学利用所学化学知识对土壤的酸碱性进行探究。
活动一:用pH试纸测定土壤的酸碱性
【实验方案】
取少量土壤样品,加蒸馏水充分搅拌,静置后过滤得到滤液;用______,读出pH,进一步确定土壤酸碱性;
【实验记录】同学们分别进行了四次实验测定滤液的酸碱度,实验数据记录如下:
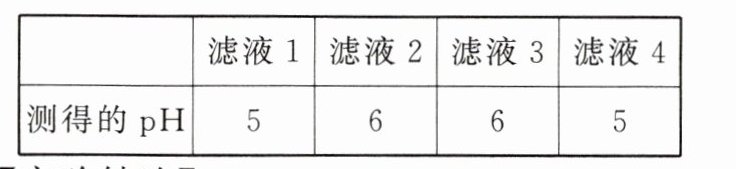
【实验结论】
该土地的土壤呈______性,则该土地______(填“适宜”或“不适宜”)种植甘蔗。
活动二:分析土壤的酸碱性原因
【调查分析】经调查,该土地之前的承包者为使自己种植的农作物生长茂盛,施用了大量化肥——氯化铵,与碱性物质混合产生刺激性气体氨气。
【作出猜想】土壤的酸碱性出现问题的原因是土壤中含有大量的氯化铵。
【设计实验】
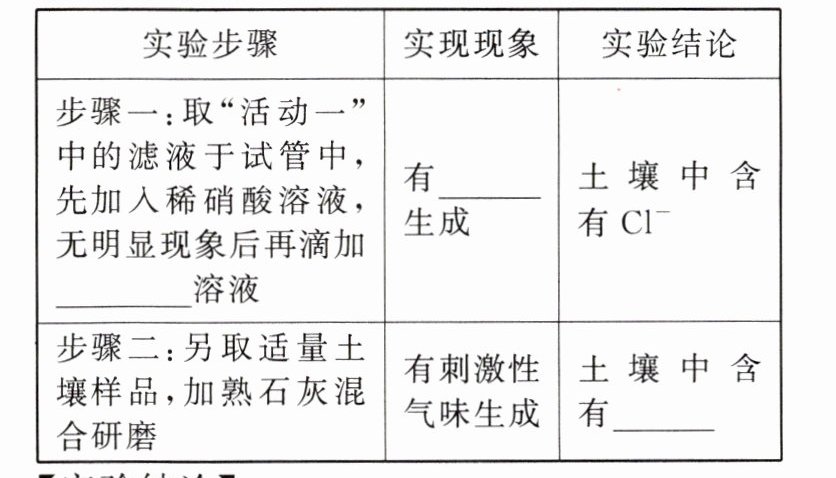
【实验结论】
猜想成立,步骤二发生反应的化学方程式为______;
活动三:寻找改良土壤酸碱性的方法
【查阅资料】常用改良土壤酸碱性的方法如下表所示:
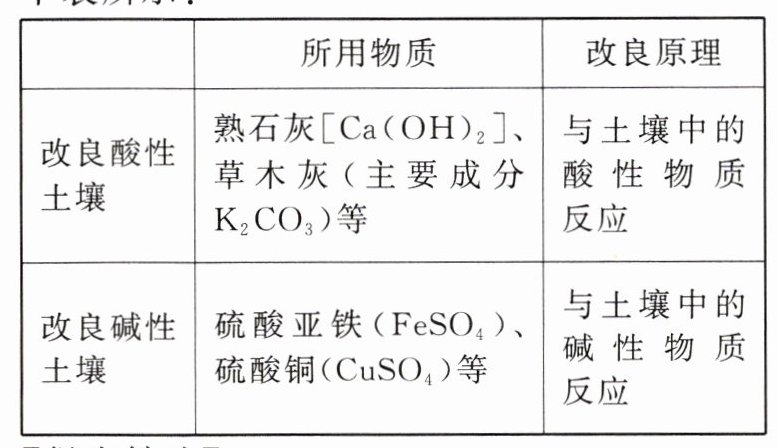
【得出结论】
同学们通过分析确定选用______改良该土壤;
【反思拓展】
开放性 经过本次探究,同学们收获满满,但对土壤施用化肥的利与弊产生了争执,请你选择支持的一方并阐述自己的理由:______。
活动一:用pH试纸测定土壤的酸碱性
【实验方案】
取少量土壤样品,加蒸馏水充分搅拌,静置后过滤得到滤液;用______,读出pH,进一步确定土壤酸碱性;
【实验记录】同学们分别进行了四次实验测定滤液的酸碱度,实验数据记录如下:

【实验结论】
该土地的土壤呈______性,则该土地______(填“适宜”或“不适宜”)种植甘蔗。
活动二:分析土壤的酸碱性原因
【调查分析】经调查,该土地之前的承包者为使自己种植的农作物生长茂盛,施用了大量化肥——氯化铵,与碱性物质混合产生刺激性气体氨气。
【作出猜想】土壤的酸碱性出现问题的原因是土壤中含有大量的氯化铵。
【设计实验】

【实验结论】
猜想成立,步骤二发生反应的化学方程式为______;
活动三:寻找改良土壤酸碱性的方法
【查阅资料】常用改良土壤酸碱性的方法如下表所示:

【得出结论】
同学们通过分析确定选用______改良该土壤;
【反思拓展】
开放性 经过本次探究,同学们收获满满,但对土壤施用化肥的利与弊产生了争执,请你选择支持的一方并阐述自己的理由:______。
答案:
洁净干燥的玻璃棒蘸取待测液滴在pH试纸上,观察颜色的变化,然后与标准比色卡对照
酸 不适宜
硝酸银(或$AgNO_{3}$) 白色沉淀 $NH_{4}^{+}$
$2NH_{4}Cl + Ca(OH)_{2} = CaCl_{2} + 2H_{2}O + 2NH_{3}\uparrow$
熟石灰或草木灰
支持有利一方的理由是:有助于植物的生长,增加农作物的产量(合理即可)
支持有弊一方的理由是:化肥的过量施用会造成土壤酸化,环境污染等(合理即可)
酸 不适宜
硝酸银(或$AgNO_{3}$) 白色沉淀 $NH_{4}^{+}$
$2NH_{4}Cl + Ca(OH)_{2} = CaCl_{2} + 2H_{2}O + 2NH_{3}\uparrow$
熟石灰或草木灰
支持有利一方的理由是:有助于植物的生长,增加农作物的产量(合理即可)
支持有弊一方的理由是:化肥的过量施用会造成土壤酸化,环境污染等(合理即可)
1. 复习酸的化学性质时,某同学总结了盐酸化学性质的思维导图如下图所示(A、B、C、D、E均能与盐酸发生反应)。请根据图示回答下列问题。

(1)若物质C是红棕色固体,则其化学式为________;
(2)若单质B是铁,取一根打磨光亮的铁钉于试管中,向其中加入足量的稀盐酸,可观察到的现象是______________________________;单质B这类物质与稀盐酸发生反应,需满足的条件是____________________;
(3)若E为氢氧化钾溶液,向该溶液中滴加几滴无色酚酞溶液后,再向其中滴加一定量的稀盐酸,当观察到溶液呈无色时,则所得溶液的溶质是________;该实验发生的化学反应基本反应类型为________。
答案:
(1)$Fe_{2}O_{3}$
(2)铁钉表面有气泡产生,溶液由无色变成浅绿色。在金属活动性顺序里,位于氢前面的金属。
(3)KCl或KCl和HCl(氯化钾或氯化钾和氯化氢) 复分解反应
(1)$Fe_{2}O_{3}$
(2)铁钉表面有气泡产生,溶液由无色变成浅绿色。在金属活动性顺序里,位于氢前面的金属。
(3)KCl或KCl和HCl(氯化钾或氯化钾和氯化氢) 复分解反应
2. 某同学在做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,意外看到有气泡产生。仔细确认药品没错后,只是在瓶口发现有白色粉末状物质。该同学认为可能是氢氧化钠溶液变质了。
(1)写出氢氧化钠溶液变质的原因:____________________(用化学方程式表示);
(2)若用pH试纸测氢氧化钠溶液的pH值________(填“能”或“不能”)确定其是否变质,原因是______________________________;
(3)在老师指导下,该同学对氢氧化钠溶液变质的程度进行了大胆的猜想与实验。
【作出猜想】根据所学知识作出以下猜想:
猜想一:部分变质,溶液中含有的溶质是________;
猜想二:全部变质,溶液中只含有溶质Na₂CO₃;
【进行实验】取少量待测溶液,加入过量的________(填字母编号,下同),产生了白色沉淀,再加几滴________,溶液变为红色,实验中产生白色沉淀的化学方程式为____________________;
可选试剂:
A. BaCl₂溶液
B. Ba(OH)₂溶液
C. NaCl溶液
D. 稀盐酸
E. 石蕊溶液
F. 酚酞溶液
【实验结论】猜想一是成立的。
【实验反思】要想除去部分变质溶液中的杂质,可选________试剂(填上述试剂字母编号)。
答案:
(1)$2NaOH + CO_{2}=Na_{2}CO_{3}+H_{2}O$
(2)不能。氢氧化钠溶液和变质后的碳酸钠溶液都显碱性,pH都大于7。
(3)【作出猜想】$NaOH、Na_{2}CO_{3}$(或氢氧化钠、碳酸钠)【进行实验】A F $BaCl_{2}+Na_{2}CO_{3}=BaCO_{3}\downarrow +2NaCl$【实验反思】B
(1)$2NaOH + CO_{2}=Na_{2}CO_{3}+H_{2}O$
(2)不能。氢氧化钠溶液和变质后的碳酸钠溶液都显碱性,pH都大于7。
(3)【作出猜想】$NaOH、Na_{2}CO_{3}$(或氢氧化钠、碳酸钠)【进行实验】A F $BaCl_{2}+Na_{2}CO_{3}=BaCO_{3}\downarrow +2NaCl$【实验反思】B
3. 化学老师在“科技社团”活动时,拿出了一瓶标签残缺的盐溶液(如图),请你和该社团成员一起参加本次探究之旅。
【提出问题】该溶液中溶质是什么?
【猜想与假设】猜想一:根据残缺标签信息,老师提出该溶液中溶质可能是Na₂SO₃;
猜想二:根据残缺标签信息,社团团长提出该溶液中溶质可能是Na₂SO₄;
猜想三:根据残缺标签信息,你提出该溶液中溶质可能是________。
【查阅资料】
Ⅰ. Na₂SO₃能与足量盐酸反应,化学方程式为Na₂SO₃ + 2HCl = 2NaCl + H₂O + SO₂↑;
Ⅱ. SO₂能使澄清石灰水变浑浊。
Ⅲ. 将SO₂通入品红溶液中,品红溶液褪色,且加热后又恢复红色,CO₂不能使品红溶液褪色。
【设计方案】经讨论,大家决定进行以下探究。
【实验探究】请补全表格。
|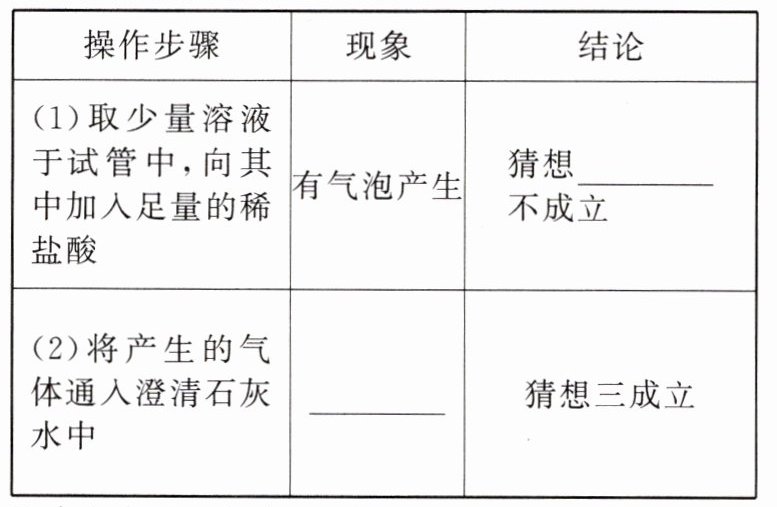
【讨论交流】大家一致认为步骤(2)得出的结论不准确,原因是____________________,要确认猜想三成立的操作及现象是____________________。
【实验结论】猜想三成立。

【提出问题】该溶液中溶质是什么?
【猜想与假设】猜想一:根据残缺标签信息,老师提出该溶液中溶质可能是Na₂SO₃;
猜想二:根据残缺标签信息,社团团长提出该溶液中溶质可能是Na₂SO₄;
猜想三:根据残缺标签信息,你提出该溶液中溶质可能是________。
【查阅资料】
Ⅰ. Na₂SO₃能与足量盐酸反应,化学方程式为Na₂SO₃ + 2HCl = 2NaCl + H₂O + SO₂↑;
Ⅱ. SO₂能使澄清石灰水变浑浊。
Ⅲ. 将SO₂通入品红溶液中,品红溶液褪色,且加热后又恢复红色,CO₂不能使品红溶液褪色。
【设计方案】经讨论,大家决定进行以下探究。
【实验探究】请补全表格。
|

【讨论交流】大家一致认为步骤(2)得出的结论不准确,原因是____________________,要确认猜想三成立的操作及现象是____________________。
【实验结论】猜想三成立。
答案:
【猜想与假设】$Na_{2}CO_{3}$【实验探究】
(1)二
(2)澄清石灰水变浑浊【讨论交流】二氧化硫也能使澄清石灰水变浑浊。将产生的气体通入品红溶液中,品红溶液不褪色。
(1)二
(2)澄清石灰水变浑浊【讨论交流】二氧化硫也能使澄清石灰水变浑浊。将产生的气体通入品红溶液中,品红溶液不褪色。
单元知识清单(十)
一、溶液的酸碱性
1. 酸碱指示剂
(1)定义:能跟酸或碱的溶液发生反应而显示不同颜色的物质,叫酸碱指示剂,简称指示剂。
常见的指示剂有________和________。
(2)指示剂颜色变化:
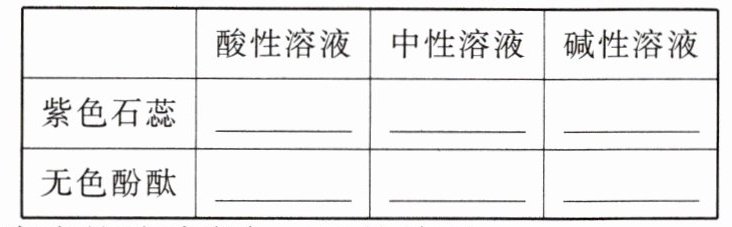
一、溶液的酸碱性
1. 酸碱指示剂
(1)定义:能跟酸或碱的溶液发生反应而显示不同颜色的物质,叫酸碱指示剂,简称指示剂。
常见的指示剂有________和________。
(2)指示剂颜色变化:

答案:
石蕊 酚酞
@@变红 不变色 变蓝 不变色 不变色 变红
@@变红 不变色 变蓝 不变色 不变色 变红
查看更多完整答案,请扫码查看


