第23页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
1. 实验室常采用
加热高锰酸钾
、分解过氧化氢溶液
分解等方法制取氧气。工业上一般采用分离液态空气
的方法制取氧气。
答案:
解:实验室常采用加热高锰酸钾、分解过氧化氢溶液等方法制取氧气。工业上一般采用分离液态空气的方法制取氧气。
2. 在实验室用如图所示装置制取氧气。
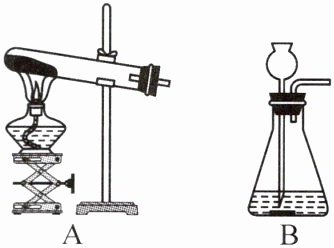
(1)用装置A加热高锰酸钾制取氧气的文字表达式为
(2)用装置B制取氧气的文字表达式为

(1)用装置A加热高锰酸钾制取氧气的文字表达式为
高锰酸钾$\xrightarrow{加热}$锰酸钾 + 二氧化锰 + 氧气
;将带有火星的木条置于导管口,若观察到木条复燃
,则说明已有氧气产生。(2)用装置B制取氧气的文字表达式为
过氧化氢$\xrightarrow{二氧化锰}$水 + 氧气
。
答案:
【解析】
(1) 高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,文字表达式为高锰酸钾$\xrightarrow{加热}$锰酸钾 + 二氧化锰 + 氧气;氧气具有助燃性,所以将带有火星的木条置于导管口,若观察到木条复燃,则说明已有氧气产生。
(2) 装置B是固液常温型制取氧气的装置,是用过氧化氢在二氧化锰的催化作用下分解生成水和氧气,文字表达式为过氧化氢$\xrightarrow{二氧化锰}$水 + 氧气。
【答案】
(1) 高锰酸钾$\xrightarrow{加热}$锰酸钾 + 二氧化锰 + 氧气;木条复燃
(2) 过氧化氢$\xrightarrow{二氧化锰}$水 + 氧气
(1) 高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,文字表达式为高锰酸钾$\xrightarrow{加热}$锰酸钾 + 二氧化锰 + 氧气;氧气具有助燃性,所以将带有火星的木条置于导管口,若观察到木条复燃,则说明已有氧气产生。
(2) 装置B是固液常温型制取氧气的装置,是用过氧化氢在二氧化锰的催化作用下分解生成水和氧气,文字表达式为过氧化氢$\xrightarrow{二氧化锰}$水 + 氧气。
【答案】
(1) 高锰酸钾$\xrightarrow{加热}$锰酸钾 + 二氧化锰 + 氧气;木条复燃
(2) 过氧化氢$\xrightarrow{二氧化锰}$水 + 氧气
1. (2025·毕节模拟)从安全、环保、节能、简便等方面考虑,实验室制取氧气的最佳方法是(
A.加热高锰酸钾制取氧气
B.通电分解水制取氧气
C.加热氧化汞制取氧气
D.用过氧化氢溶液和二氧化锰的混合物制取氧气
D
)A.加热高锰酸钾制取氧气
B.通电分解水制取氧气
C.加热氧化汞制取氧气
D.用过氧化氢溶液和二氧化锰的混合物制取氧气
答案:
【解析】:
本题考查氧气的实验室制取方法,涉及不同制取方式的比较,需从安全、环保、节能、简便等多方面综合考虑。
选项A:加热高锰酸钾制取氧气,需要加热,消耗能源,且加热过程中若操作不当可能存在一定安全隐患,同时高锰酸钾受热分解会产生锰酸钾、二氧化锰和氧气,相对操作较为复杂,不符合节能、简便的要求,故A选项错误。
选项B:通电分解水制取氧气,虽然产物只有氢气和氧气,比较环保,但通电分解水需要消耗大量电能,成本较高,不符合节能的要求,故B选项错误。
选项C:加热氧化汞制取氧气,氧化汞受热分解会产生汞和氧气,汞是一种有毒的重金属,会对环境造成污染,不符合环保的要求,故C选项错误。
选项D:用过氧化氢溶液和二氧化锰的混合物制取氧气,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,该反应不需要加热,节能;产物是水和氧气,无污染,环保;操作简单,只需将过氧化氢溶液和二氧化锰混合即可,符合安全、环保、节能、简便的要求,故D选项正确。
【答案】:D
本题考查氧气的实验室制取方法,涉及不同制取方式的比较,需从安全、环保、节能、简便等多方面综合考虑。
选项A:加热高锰酸钾制取氧气,需要加热,消耗能源,且加热过程中若操作不当可能存在一定安全隐患,同时高锰酸钾受热分解会产生锰酸钾、二氧化锰和氧气,相对操作较为复杂,不符合节能、简便的要求,故A选项错误。
选项B:通电分解水制取氧气,虽然产物只有氢气和氧气,比较环保,但通电分解水需要消耗大量电能,成本较高,不符合节能的要求,故B选项错误。
选项C:加热氧化汞制取氧气,氧化汞受热分解会产生汞和氧气,汞是一种有毒的重金属,会对环境造成污染,不符合环保的要求,故C选项错误。
选项D:用过氧化氢溶液和二氧化锰的混合物制取氧气,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,该反应不需要加热,节能;产物是水和氧气,无污染,环保;操作简单,只需将过氧化氢溶液和二氧化锰混合即可,符合安全、环保、节能、简便的要求,故D选项正确。
【答案】:D
2. 实验室有如下试剂:
紫黑
色高锰酸钾固体,黑
色二氧化锰粉末,无
色过氧化氢溶液。请写出用以上物质制氧气时反应的文字表达式:高锰酸钾$\overset{加热}{\longrightarrow}$锰酸钾+二氧化锰+氧气
、过氧化氢$\overset{二氧化锰}{\longrightarrow}$水+氧气
。
答案:
【解析】:
本题主要考查了实验室常见物质的颜色以及氧气的制取方法和反应的文字表达式。
首先,我们需要知道实验室中常见物质的颜色。高锰酸钾固体是紫黑色的,二氧化锰粉末是黑色的,过氧化氢溶液是无色的。
其次,我们需要知道用这些物质如何制取氧气。高锰酸钾在加热的条件下可以分解生成氧气,同时生成锰酸钾和二氧化锰;过氧化氢在二氧化锰的催化作用下可以分解生成氧气和水。
最后,我们需要根据这些信息写出反应的文字表达式。
【答案】:
紫黑;黑;无;高锰酸钾$\overset{加热}{\longrightarrow}$锰酸钾+二氧化锰+氧气;过氧化氢$\overset{二氧化锰}{\longrightarrow}$水+氧气。
本题主要考查了实验室常见物质的颜色以及氧气的制取方法和反应的文字表达式。
首先,我们需要知道实验室中常见物质的颜色。高锰酸钾固体是紫黑色的,二氧化锰粉末是黑色的,过氧化氢溶液是无色的。
其次,我们需要知道用这些物质如何制取氧气。高锰酸钾在加热的条件下可以分解生成氧气,同时生成锰酸钾和二氧化锰;过氧化氢在二氧化锰的催化作用下可以分解生成氧气和水。
最后,我们需要根据这些信息写出反应的文字表达式。
【答案】:
紫黑;黑;无;高锰酸钾$\overset{加热}{\longrightarrow}$锰酸钾+二氧化锰+氧气;过氧化氢$\overset{二氧化锰}{\longrightarrow}$水+氧气。
3. (2024·苏州)在高锰酸钾制氧气实验中,一定不需要用到的仪器是(
A.酒精灯
B.试管
C.漏斗
D.集气瓶
C
)A.酒精灯
B.试管
C.漏斗
D.集气瓶
答案:
【解析】:
本题考察的是高锰酸钾制取氧气的实验装置及所需仪器。在高锰酸钾制取氧气的实验中,首先需要加热高锰酸钾使其分解产生氧气,因此酒精灯是必需的加热设备。同时,高锰酸钾需要放置在试管中进行加热,所以试管也是必需的。氧气产生后需要收集,集气瓶用于收集产生的氧气。而漏斗主要用于过滤操作,将液体中的固体杂质分离出来,或用于向小口容器中添加液体,在高锰酸钾制取氧气的实验中并不需要使用漏斗。
【答案】:
C
本题考察的是高锰酸钾制取氧气的实验装置及所需仪器。在高锰酸钾制取氧气的实验中,首先需要加热高锰酸钾使其分解产生氧气,因此酒精灯是必需的加热设备。同时,高锰酸钾需要放置在试管中进行加热,所以试管也是必需的。氧气产生后需要收集,集气瓶用于收集产生的氧气。而漏斗主要用于过滤操作,将液体中的固体杂质分离出来,或用于向小口容器中添加液体,在高锰酸钾制取氧气的实验中并不需要使用漏斗。
【答案】:
C
4. (2024·湖南)下列发生装置中,可用于实验室加热高锰酸钾制取氧气的是(
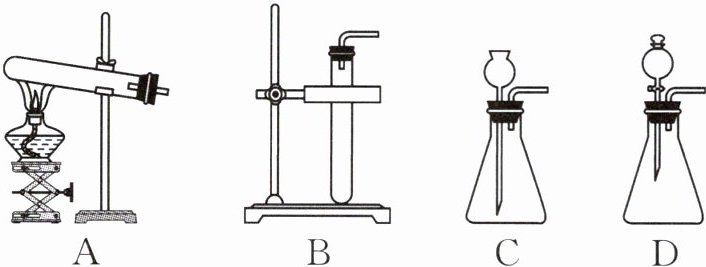
A
)
答案:
【解析】:本题考查实验室加热高锰酸钾制取氧气的发生装置。加热高锰酸钾制取氧气属于固体加热型反应。
A选项:该装置有酒精灯加热,且试管口略向下倾斜,铁架台固定,符合固体加热型反应的要求,可用于加热高锰酸钾制取氧气。
B选项:该装置没有加热仪器,不能用于加热高锰酸钾制取氧气。
C选项:该装置是固液常温型装置,适用于固体和液体在常温下反应制取气体,不适合加热高锰酸钾制取氧气。
D选项:该装置也是固液常温型装置,且分液漏斗用于控制液体滴加速度,适用于固体和液体在常温下反应制取气体,不适合加热高锰酸钾制取氧气。
故A选项正确
【答案】:A
A选项:该装置有酒精灯加热,且试管口略向下倾斜,铁架台固定,符合固体加热型反应的要求,可用于加热高锰酸钾制取氧气。
B选项:该装置没有加热仪器,不能用于加热高锰酸钾制取氧气。
C选项:该装置是固液常温型装置,适用于固体和液体在常温下反应制取气体,不适合加热高锰酸钾制取氧气。
D选项:该装置也是固液常温型装置,且分液漏斗用于控制液体滴加速度,适用于固体和液体在常温下反应制取气体,不适合加热高锰酸钾制取氧气。
故A选项正确
【答案】:A
5. 化学是一门以实验为基础的学科。请结合图示回答问题。
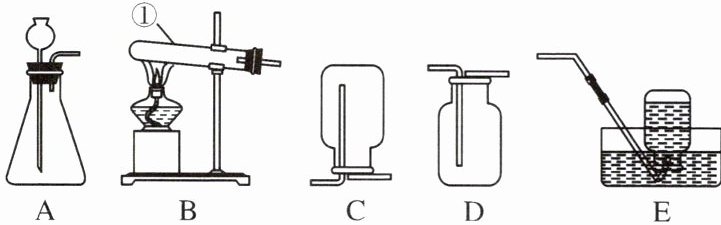
(1)仪器①的名称为
(2)实验室用高锰酸钾制取氧气应选择的发生装置和收集装置为
(3)若采用E装置收集某种气体,当
(4)若用D装置收集氧气,检验氧气已收集满的方法是

(1)仪器①的名称为
试管
。(2)实验室用高锰酸钾制取氧气应选择的发生装置和收集装置为
BD或BE
。其中发生装置还需要改进的是在试管口塞一团棉花
。(3)若采用E装置收集某种气体,当
导管口有连续均匀气泡冒出
时开始收集。(4)若用D装置收集氧气,检验氧气已收集满的方法是
将带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满
。
答案:
(1)试管
(2)BD或BE;在试管口塞一团棉花
(3)导管口有连续均匀气泡冒出
(4)将带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满
(1)试管
(2)BD或BE;在试管口塞一团棉花
(3)导管口有连续均匀气泡冒出
(4)将带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满
6. 利用分离液态空气的方法得到氧气是工业上制取氧气的重要途径,如图是工业上制取氧气流程。
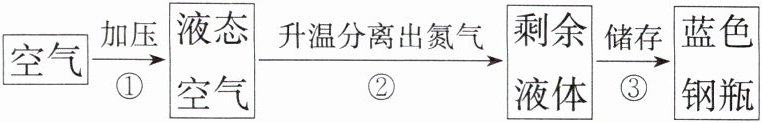
(1)从步骤②可以得出氮气的沸点比氧气的沸点
(2)工业上采用该方法制氧气,这一变化属于
(3)根据下表数据判断:工业上制取氧气,控制温度在-195.8℃<T<
|物质|氢气|二氧化碳|氮气|氧气|
|沸点/℃|-252.8|-56.55|-195.8|-183.0|


(1)从步骤②可以得出氮气的沸点比氧气的沸点
低
(填“高”或“低”)。(2)工业上采用该方法制氧气,这一变化属于
物理
(填“物理”或“化学”)变化。(3)根据下表数据判断:工业上制取氧气,控制温度在-195.8℃<T<
-183.0
℃时,可以将液态空气中的氮气分离。|物质|氢气|二氧化碳|氮气|氧气|
|沸点/℃|-252.8|-56.55|-195.8|-183.0|

答案:
【解析】:
(1) 从步骤②中,经过升温分离出氮气,说明氮气的沸点比氧气的沸点低,因为沸点低的物质先气化分离出来。
(2) 工业上采用分离液态空气的方法制氧气,是利用液态氮和液态氧沸点的不同,将其分离,没有新物质生成,属于物理变化。
(3) 要将液态空气中的氮气分离出来,需要控制温度在氮气的沸点以上,氧气的沸点以下,即$-195.8^{\circ}C<T< - 183.0^{\circ}C$。
【答案】:
(1) 低
(2) 物理
(3) $-183.0$
(1) 从步骤②中,经过升温分离出氮气,说明氮气的沸点比氧气的沸点低,因为沸点低的物质先气化分离出来。
(2) 工业上采用分离液态空气的方法制氧气,是利用液态氮和液态氧沸点的不同,将其分离,没有新物质生成,属于物理变化。
(3) 要将液态空气中的氮气分离出来,需要控制温度在氮气的沸点以上,氧气的沸点以下,即$-195.8^{\circ}C<T< - 183.0^{\circ}C$。
【答案】:
(1) 低
(2) 物理
(3) $-183.0$
查看更多完整答案,请扫码查看


