2026年学易优高考二轮总复习化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年学易优高考二轮总复习化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
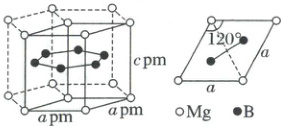
10.(2025·鄂东南省级示范高中联盟联考)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿$c$轴的投影图如下所示,晶胞参数分别为$a\ pm$、$a\ pm$、$c\ pm$,下列叙述正确的是 (
A.一个晶胞中含有 6 个$Mg$原子
B.该物质的化学式为$MgB$
C.B 原子间最近距离为$\frac{\sqrt{3}}{3}a\ pm$
D.晶体的密度为$\frac{46×10^{-30}}{\frac{\sqrt{3}}{2}a^2cN_A}\ g· cm^{-3}$
C
)
A.一个晶胞中含有 6 个$Mg$原子
B.该物质的化学式为$MgB$
C.B 原子间最近距离为$\frac{\sqrt{3}}{3}a\ pm$
D.晶体的密度为$\frac{46×10^{-30}}{\frac{\sqrt{3}}{2}a^2cN_A}\ g· cm^{-3}$
答案:
10.C 结合投影图可知,晶体结构中实线部分为1个晶胞,$Mg$原子个数为$4×\frac{1}{6}+4×\frac{1}{12}=1$,A错误;$Mg$原子个数为$4×\frac{1}{6}+4×\frac{1}{12}=1$,有2个B位于晶胞体内,化学式为$MgB_2$,B错误;晶胞沿$c$轴的投影图中硼原子位于正三角形的中心,$B$原子间的最近距离应为$\frac{\sqrt{3}}{3}apm$,C正确;已知晶胞参数分别为$apm$、$apm$、$cpm$,晶胞体积为$\frac{\sqrt{3}}{2}a^2c×10^{-30}cm^3$,化学式为$MgB_2$,晶胞质量为$\frac{46}{N_A}g$,晶体的密度为$\rho=\frac{m}{V}=\frac{46×10^{30}}{\frac{\sqrt{3}}{2}a^2cN_A}g·cm^{-3}$,D错误。
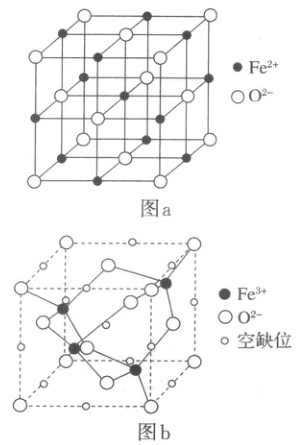
11.(2025·安徽省淮南市二模)$FeO$晶胞结构如图 a 所示,通常制备条件下很难得到整比化合物,而是阳离子偏少的$Fe_{1-x}O$晶体,$Fe_{1-x}O$晶体中存在短程有序的原子簇($Fe_4O_{10}$),称为 Koch 原子簇(如图 b 所示)。下列说法错误的是 (
A.$FeO$晶体中$Fe^{2+}$的配位数为 6
B.$FeO$晶体结构中每缺少 2 个$Fe^{2+}$,则会形成 1 个$Fe_4O_{10}$原子簇
C.图 b 中体心的空缺位可以填充$Fe^{2+}$
D.当$Fe_{1-x}O$中$x=0.1$时,晶体中$Fe^{2+}$、$Fe^{3+}$个数比为$7:2$
C
)
A.$FeO$晶体中$Fe^{2+}$的配位数为 6
B.$FeO$晶体结构中每缺少 2 个$Fe^{2+}$,则会形成 1 个$Fe_4O_{10}$原子簇
C.图 b 中体心的空缺位可以填充$Fe^{2+}$
D.当$Fe_{1-x}O$中$x=0.1$时,晶体中$Fe^{2+}$、$Fe^{3+}$个数比为$7:2$
答案:
11.C 从图a可以看出每个$Fe^{2+}$周围有6个$O^{2-}$离子,所以$Fe^{2+}$的配位数为6,A正确;原子簇$(Fe_4O_{10})$中的铁都是+3价,根据晶体结构呈电中性,$FeO$晶体结构中每缺少2个$Fe^{2+}$,则会有4个$Fe^{2+}$变为$Fe^{3+}$,4个$Fe^{3+}$可以形成1个原子簇$(Fe_4O_{10})$,B正确;图b中体心的空缺位被$Fe^{3+}$包围,不适合填充阳离子(同性电荷斥力大),C错误;当$x=0.1$时,设晶体$Fe_{0.9}O$中$Fe^{2+}$、$Fe^{3+}$个数分别为$a$、$b$,则$a+b=0.9$、$2a+3b=2$,解得$a=0.7$、$b=0.2$,所以$Fe^{2+}$、$Fe^{3+}$个数比为$7:2$,D正确;答案选C。
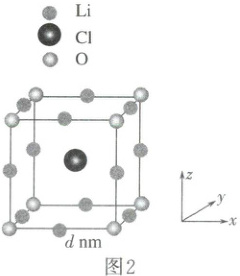
12.(2025·辽宁二模)$Li_2(OH)Cl$在固体离子导电方面具有潜在的应用前景。两种晶型中,一种取长方体晶胞(图 1),另一种取立方体晶胞(图 2)。图中氢原子皆已隐去,立方体晶胞所代表的晶体中部分锂离子(●$Li$)位置上存在缺位现象。
下列说法正确的是 (
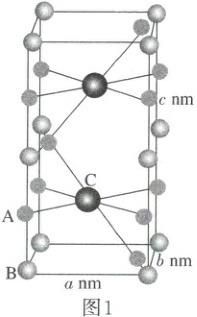
A.图 1 A、B 两微粒的距离为$\frac{1}{4}c\ nm$,则 C 的分数坐标为$(\frac{1}{2},\frac{1}{2},\frac{1}{2})$
B.图 2 立方晶胞中锂离子的缺位率为$\frac{1}{2}$
C.图 2$Cl^-$周围等距且最近的$Cl^-$有 6 个
D.两种晶型的密度近似相等,则$c=\frac{d^3}{ab}$
下列说法正确的是 (
C
)

A.图 1 A、B 两微粒的距离为$\frac{1}{4}c\ nm$,则 C 的分数坐标为$(\frac{1}{2},\frac{1}{2},\frac{1}{2})$
B.图 2 立方晶胞中锂离子的缺位率为$\frac{1}{2}$
C.图 2$Cl^-$周围等距且最近的$Cl^-$有 6 个
D.两种晶型的密度近似相等,则$c=\frac{d^3}{ab}$
答案:
12.C C在$z$轴上的分数坐标是$\frac{1}{4}$,则C的分数坐标为$(\frac{1}{2},\frac{1}{2},\frac{1}{4})$,A错误;根据化学式$Li_2(OH)Cl$知,该晶胞中应该含有2个$Li^+$,图2中$Cl^-$个数为1,$OH^-$个数为$8×\frac{1}{8}=1$,$Li^+$个数为$12×\frac{1}{4}=3$,锂离子的缺位率为$\frac{3 - 2}{3}=\frac{1}{3}$,B错误;图2$Cl^-$周围等距且最近的$Cl^-$有6个,分别位于与该晶胞相邻的6个晶胞的体心上,C正确;图1中$Cl^-$个数为2,$OH^-$个数为$8×\frac{1}{8}+4×\frac{1}{4}=2$,立方体中$Li^+$个数为$8×\frac{1}{4}+1+2×\frac{1}{2}=4$,晶胞体积为$abc×10^{-21}cm^3$,图2中晶胞体积为$d^3×10^{-21}cm^3$,图1中晶胞密度$\rho=\frac{m}{V}=\frac{M×2}{N_Aabc×10^{-21}}=\frac{2M}{N_Aabc×10^{-21}}g·cm^{-3}$,图2中晶胞密度$\rho=\frac{m}{V}=\frac{M}{N_AV}=\frac{M}{N_Ad^3×10^{-21}}g·cm^{-3}$,$c=\frac{2d^3}{ab}$,D错误;答案为C。
查看更多完整答案,请扫码查看


