9. 氢氧化钙化学性质:具有较强的腐蚀性。能与${CO_{2}}$、${SO_{2}}$等反应,如${CO_{2} + Ca(OH)_{2} = CaCO_{3}\downarrow + H_{2}O}$,这一反应常用于检验______。能与酸反应,反应过程无明显现象,如${Ca(OH)_{2}}$与${HCl}$和${H_{2}SO_{4}}$的反应如下:______,______。能与部分盐反应,生成沉淀,如:______,______。
答案:
9.二氧化碳的存在;$Ca(OH)_2 + 2HCl \longrightarrow CaCl_2 + 2H_2O$;$Ca(OH)_2 + H_2SO_4 \longrightarrow CaSO_4 + 2H_2O$;$Na_2CO_3 + Ca(OH)_2 \longrightarrow CaCO_3 \downarrow + 2NaOH$;$2FeCl_3 + 3Ca(OH)_2 \longrightarrow 2Fe(OH)_3 \downarrow + 3CaCl_2$
10. 氢氧化钙能与空气中的二氧化碳反应而变质,所以氢氧化钙溶液敞口放置一段时间,溶液质量
减小
。
答案:
10.减小
11. 用途:重要的建筑材料,也是一种工业原料。如用来制取漂白粉,农业上用于改良
酸
性土壤等。
答案:
11.酸
12. 氢氧化钙的制取:将生石灰${(CaO)}$溶于水(剧烈反应、
放出
大量的热),发生反应的化学方程式为$CaO + H_2O \longrightarrow Ca(OH)_2$
。利用生石灰能与水反应的性质,生石灰可以做某些气体的干燥剂
,但不能干燥酸性气体。
答案:
12.放出;$CaO + H_2O \longrightarrow Ca(OH)_2$;干燥剂
1. 酸碱反应实验:向盛有氢氧化钠的烧杯中滴入几滴酚酞试液,溶液变红,向变红的溶液中滴加稀盐酸(或稀硫酸),边滴边振荡,溶液颜色变浅直至消失,说明溶液由碱性变为中性或酸性,氢氧化钠和酸发生了反应。
实验过程中溶液中溶质、pH 以及颜色的变化
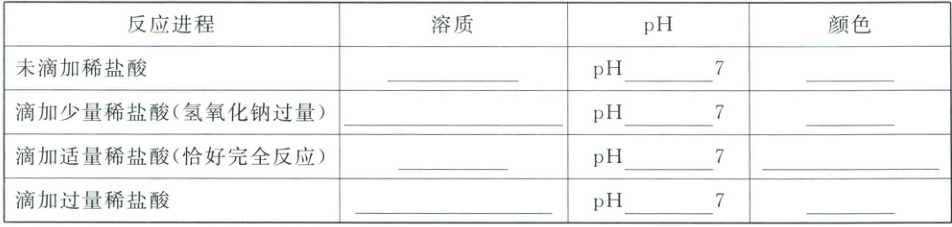
实验过程中溶液中溶质、pH 以及颜色的变化

答案:
1.氢氧化钠;大于;红色;氢氧化钠和氯化钠;大于;红色;氯化钠;等于;红色变为无色;氯化钠和氯化氢;小于;无色
2. 酸碱反应原理:酸和碱之间发生反应能生成
盐和水
。如:$HCl + NaOH = NaCl + H_{2}O$,$H_{2}SO_{4} + 2NaOH = Na_{2}SO_{4} + 2H_{2}O$。
答案:
2.盐和水
3. 酸碱反应的实质:酸中的 $H^{+}$ 和碱中的 $OH^{-}$ 结合生成水分子,即
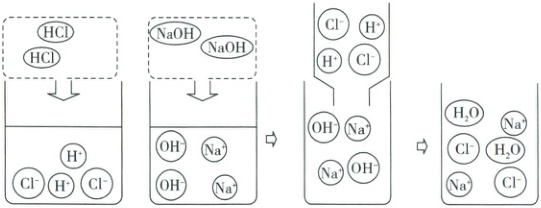
$H^{+} + OH^{-} = H_{2}O$
。
答案:
3.$H^{+} + OH^{-} = H_{2}O$
4. 大多数酸与碱反应生成盐和水时,我们观察不到明显的现象$[H_{2}SO_{4} + Ba(OH)_{2} = BaSO_{4}\downarrow + 2H_{2}O$等除外$]$。探究酸和碱之间发生反应的方法有以下几种:
(1)指示剂法。先在 $NaOH$ 溶液中滴加酚酞试液,溶液显红色,然后再逐滴滴加稀盐酸,若观察到____,则证明 $NaOH$ 溶液与稀盐酸发生化学反应。
(2)pH 试纸法。先用 pH 试纸测定 $NaOH$ 溶液的 pH,再向 $NaOH$ 溶液中逐滴滴加稀盐酸,不断振荡溶液使其充分接触,同时多次测定混合溶液的 pH,若____,则证明 $NaOH$ 溶液与稀盐酸发生化学反应。
(3)热量变化法。化学反应通常伴随着能量的变化,所以可借助反应前后的温度变化来判断反应的发生。酸与碱的反应是
(4)验证反应物的消失。如向氢氧化钠溶液中滴加稀盐酸,反应完全时,可向溶液中滴加 $CuSO_{4}$ 溶液,不再出现
(1)指示剂法。先在 $NaOH$ 溶液中滴加酚酞试液,溶液显红色,然后再逐滴滴加稀盐酸,若观察到____,则证明 $NaOH$ 溶液与稀盐酸发生化学反应。
(2)pH 试纸法。先用 pH 试纸测定 $NaOH$ 溶液的 pH,再向 $NaOH$ 溶液中逐滴滴加稀盐酸,不断振荡溶液使其充分接触,同时多次测定混合溶液的 pH,若____,则证明 $NaOH$ 溶液与稀盐酸发生化学反应。
(3)热量变化法。化学反应通常伴随着能量的变化,所以可借助反应前后的温度变化来判断反应的发生。酸与碱的反应是
放热
反应,如果 $NaOH$ 溶液与稀盐酸混合前后温度有变化,则证明 $NaOH$ 溶液和稀盐酸发生了化学反应。而且氢氧化钠和盐酸恰好完全反应时放出的热量最多
、温度最高
。(4)验证反应物的消失。如向氢氧化钠溶液中滴加稀盐酸,反应完全时,可向溶液中滴加 $CuSO_{4}$ 溶液,不再出现
蓝色絮状
沉淀,说明 $NaOH$ 已完全参加反应,反应发生。
答案:
4.溶液由红色变为无色;pH逐渐减小(由大于7到等于7,再到小于7);放热;多;高;蓝色絮状
查看更多完整答案,请扫码查看


