1. 硫在空气中燃烧生成二氧化硫,在此反应中,硫、氧气、二氧化硫的质量比是( )
A.1∶1∶1
B.1∶1∶2
C.32∶16∶64
D.32∶16∶48
A.1∶1∶1
B.1∶1∶2
C.32∶16∶64
D.32∶16∶48
答案:
B
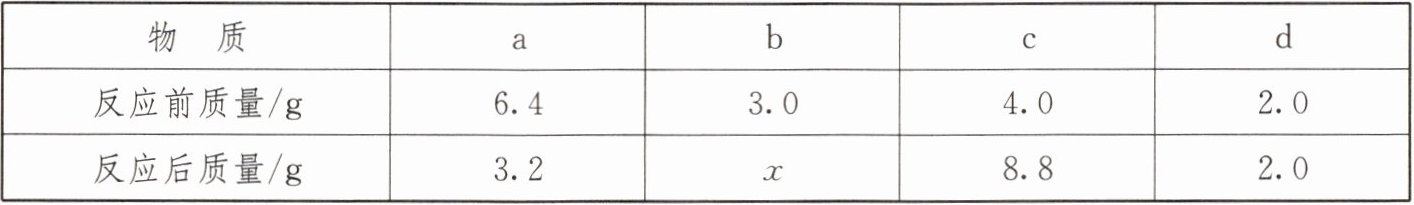
2. 将一定质量的a、b、c、d四种物质放入一密闭容器中在一定条件下反应,测得反应前后各物质的质量如表所示,下列说法正确的是( )
|物 质|a|b|c|d|
|反应前质量/g|6.4|3.0|4.0|2.0|
|反应后质量/g|3.2|x|8.8|2.0|
A.d一定是该反应的催化剂
B.此反应的基本反应类型是分解反应
C.x的值为1.6
D.若继续反应至b反应完全,则此时反应后a的剩余质量为0.4 g
|物 质|a|b|c|d|
|反应前质量/g|6.4|3.0|4.0|2.0|
|反应后质量/g|3.2|x|8.8|2.0|

A.d一定是该反应的催化剂
B.此反应的基本反应类型是分解反应
C.x的值为1.6
D.若继续反应至b反应完全,则此时反应后a的剩余质量为0.4 g
答案:
解:根据质量守恒定律,反应前后总质量相等。
反应前总质量:6.4 + 3.0 + 4.0 + 2.0 = 15.4g
反应后总质量:3.2 + x + 8.8 + 2.0 = 14.0 + x
则14.0 + x = 15.4,解得x = 1.4
A.d反应前后质量不变,可能是催化剂或不参与反应的杂质,“一定”错误。
B.a质量减少(6.4→3.2,减少3.2g),b质量减少(3.0→1.4,减少1.6g),c质量增加(4.0→8.8,增加4.8g),d质量不变。反应物为a、b,生成物为c,属于化合反应,“分解反应”错误。
C.x=1.4,“1.6”错误。
D.a、b反应的质量比为3.2g:1.6g=2:1。b完全反应消耗3.0g,设消耗a的质量为y,则2:1=y:3.0g,y=6.0g。a剩余质量:6.4g - 6.0g=0.4g,正确。
结论:D
反应前总质量:6.4 + 3.0 + 4.0 + 2.0 = 15.4g
反应后总质量:3.2 + x + 8.8 + 2.0 = 14.0 + x
则14.0 + x = 15.4,解得x = 1.4
A.d反应前后质量不变,可能是催化剂或不参与反应的杂质,“一定”错误。
B.a质量减少(6.4→3.2,减少3.2g),b质量减少(3.0→1.4,减少1.6g),c质量增加(4.0→8.8,增加4.8g),d质量不变。反应物为a、b,生成物为c,属于化合反应,“分解反应”错误。
C.x=1.4,“1.6”错误。
D.a、b反应的质量比为3.2g:1.6g=2:1。b完全反应消耗3.0g,设消耗a的质量为y,则2:1=y:3.0g,y=6.0g。a剩余质量:6.4g - 6.0g=0.4g,正确。
结论:D
3.(2022·益阳)我国科学家成功合成新型催化剂,将CO_2高效转化为甲醇(CH_3OH)。这不仅可以缓解碳排放引起的温室效应,还将成为理想的能源补充形式。
(1)若CO_2转化为CH_3OH的化学方程式是$CO_2 + 3H_2 \xlongequal{催化剂} CH_3OH + X,$则生成物X的化学式为______。
(2)根据上述信息,请计算生成96 g CH_3OH时,消耗CO_2的质量。
(1)若CO_2转化为CH_3OH的化学方程式是$CO_2 + 3H_2 \xlongequal{催化剂} CH_3OH + X,$则生成物X的化学式为______。
(2)根据上述信息,请计算生成96 g CH_3OH时,消耗CO_2的质量。
答案:
(1)H₂O
(2)解:设消耗CO₂的质量为x。
CO₂ + 3H₂ $\xlongequal{催化剂}$ CH₃OH + H₂O
44 32
x 96g
$\frac{44}{32} = \frac{x}{96g}$
x = 132g
答:消耗CO₂的质量为132g。
(1)H₂O
(2)解:设消耗CO₂的质量为x。
CO₂ + 3H₂ $\xlongequal{催化剂}$ CH₃OH + H₂O
44 32
x 96g
$\frac{44}{32} = \frac{x}{96g}$
x = 132g
答:消耗CO₂的质量为132g。
4.(2022·孝感)2022年北京冬奥会秉持绿色、共享、开放、廉洁理念,首次采用氢气作为火炬燃料,计算完全燃烧0.4 kg氢气,理论上需要消耗氧气的质量是多少?
答案:
消耗氧气的质量是 $3.2kg$。
查看更多完整答案,请扫码查看


