2024年中考档案初中同步学案导学九年级化学全一册鲁教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2024年中考档案初中同步学案导学九年级化学全一册鲁教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第142页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
7.(临沂中考)如图是a、b、c三种固体物质的溶解度曲线,回答下列问题。
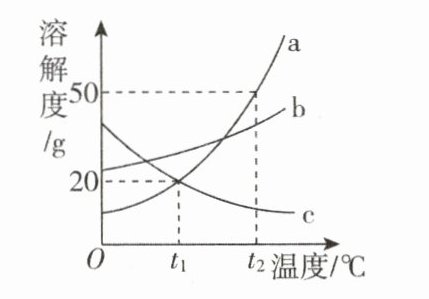
(1)在________$℃$时,a、c两种物质的溶解度相等。
(2)在$t_1℃$时,向盛有30ga物质的烧杯中加入50g水。充分溶解后,所得溶液的质量为________g.
(3)若a物质中混有少量b物质,最好采用________(填“降温结晶”或“蒸发结晶”)的方法提纯a。
(4)$t_2℃$时,a、b、c三种物质的饱和溶液各100g,所含溶质质量由大到小的顺序为________。

(1)在________$℃$时,a、c两种物质的溶解度相等。
(2)在$t_1℃$时,向盛有30ga物质的烧杯中加入50g水。充分溶解后,所得溶液的质量为________g.
(3)若a物质中混有少量b物质,最好采用________(填“降温结晶”或“蒸发结晶”)的方法提纯a。
(4)$t_2℃$时,a、b、c三种物质的饱和溶液各100g,所含溶质质量由大到小的顺序为________。
答案:
(1)$t_{1}$
(2) 60
(3) 降温结晶
(4)$a>b>c$
(1)$t_{1}$
(2) 60
(3) 降温结晶
(4)$a>b>c$
8.(烟台中考)我国化学家侯德榜先生创立的联合制碱法,将碱厂与氨厂联合,既提高效益又减少污染,促进了世界制碱工业的发展。联合制碱法的模拟流程如图1所示。
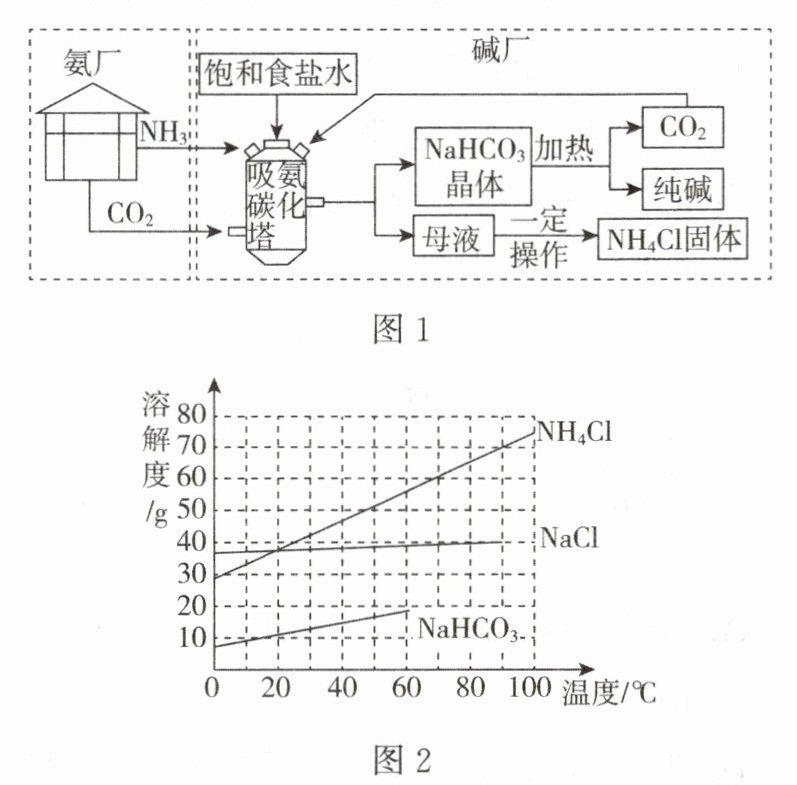
三种盐的溶解度随温度变化的曲线如图2所示。吸氨碳化塔中温度控制在30~35$℃$,其中主要发生的反应是$NH_3 + CO_2 + H_2O + NaCl = NaHCO_3↓ + NH_4Cl$。
(1)氨厂的原料$N_2$来自于空气。分离液态空气是利用空气中各成分的________不同。
(2)通常状况下,$NH_3$的溶解度远大于$CO_2$的溶解度。为了提高产率,吸氨碳化塔中应该先通入的是________(填“$NH_3$”或“$CO_2$”)。
(3)加热$NaHCO_3$制得纯碱的化学方程式是______________________________。
(4)结合图2分析,吸氨碳化塔中析出$NaHCO_3$固体的主要原因是________(填序号)。
①溶剂质量减少
②$NaHCO_3$难溶于水
③30~35$℃$时,$NaCl$、$NaHCO_3$、$NH_4Cl$的溶解度相比较,$NaHCO_3$的溶解度最小,易达到饱和而析出
(5)氨厂生产的$NH_3$溶于水后得到的氨水可以作________(填化肥类别)肥。碱厂与氨厂联合后,用$NH_4Cl$代替氨水作化肥,其优势是________(答一点即可)。

三种盐的溶解度随温度变化的曲线如图2所示。吸氨碳化塔中温度控制在30~35$℃$,其中主要发生的反应是$NH_3 + CO_2 + H_2O + NaCl = NaHCO_3↓ + NH_4Cl$。
(1)氨厂的原料$N_2$来自于空气。分离液态空气是利用空气中各成分的________不同。
(2)通常状况下,$NH_3$的溶解度远大于$CO_2$的溶解度。为了提高产率,吸氨碳化塔中应该先通入的是________(填“$NH_3$”或“$CO_2$”)。
(3)加热$NaHCO_3$制得纯碱的化学方程式是______________________________。
(4)结合图2分析,吸氨碳化塔中析出$NaHCO_3$固体的主要原因是________(填序号)。
①溶剂质量减少
②$NaHCO_3$难溶于水
③30~35$℃$时,$NaCl$、$NaHCO_3$、$NH_4Cl$的溶解度相比较,$NaHCO_3$的溶解度最小,易达到饱和而析出
(5)氨厂生产的$NH_3$溶于水后得到的氨水可以作________(填化肥类别)肥。碱厂与氨厂联合后,用$NH_4Cl$代替氨水作化肥,其优势是________(答一点即可)。
答案:
(1) 沸点
(2)${NH_{3}}$
(3)${2NaHCO_{3}\xlongequal{\triangle}Na_{2}CO_{3} + H_{2}O + CO_{2}\uparrow}$
(4) ③
(5) 氮 肥效高(合理即可)
(1) 沸点
(2)${NH_{3}}$
(3)${2NaHCO_{3}\xlongequal{\triangle}Na_{2}CO_{3} + H_{2}O + CO_{2}\uparrow}$
(4) ③
(5) 氮 肥效高(合理即可)
9.(枣庄中考)某兴趣小组同学在老师的指导下,进入实验室对碳酸钙进行了一系列探究。回答下列问题。
I.碳酸钙与稀盐酸反应
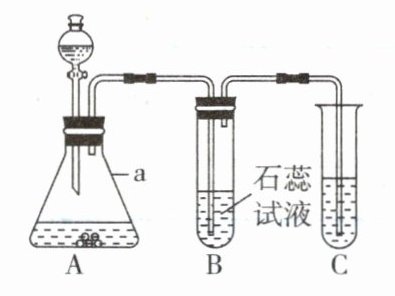
(1)装置A中仪器a的名称为__________。
(2)装置B中的现象是____________________。
(3)装置C若用于检验生成的气体,其中试剂为__________(写名称),发生反应的化学方程式为______________________________。
II.碳酸钙分解
碳酸钙在电炉中高温煅烧一段时间后,对剩余固体进行探究。
[提出问题]剩余固体成分是什么?
[猜想与假设]猜想一:全部是碳酸钙
猜想二:是碳酸钙和氧化钙的混合物
猜想三:全部是氧化钙
[设计并完成实验]
|实验操作|实验现象|解释与结论|
| ---- | ---- | ---- |
|步骤一:取剩余固体于试管中,加水振荡后静置|底部有白色不溶物| |
|步骤二:取上层清液于另一试管中,滴加氯化铜溶液|________|上层清液中一定含有氢氧化钙|
|步骤三:取部分底部白色不溶物于第三支试管中,滴加过量稀盐酸|有气泡产生|白色不溶物中一定含有________|
[实验结论]正确的猜想是________。
[交流与反思]小芳同学认为,步骤二中还可滴加其他试剂用来替代氯化铜溶液,该试剂可以是__________(写一种即可);小华同学认为,只需完成步骤一和步骤三即可获得相同实验结论,他的依据是__________________。
[拓展与分析]查阅资料:生石灰质量的优劣常采用“活性度”来衡量。“活性度”的测定方法:取一定质量的生石灰,加入一定量的水,用一定溶质质量分数的盐酸中和,记录所消耗盐酸的体积(单位为mL)。消耗盐酸的体积数越大,“活性度”越高。
测得煅烧产物($CaO$)的活性度,数据见如表。
|煅烧时间
活性度
煅烧温度|1050$℃$|1100$℃$|1150$℃$|1200$℃$|1250$℃$|1300$℃$|
| ---- | ---- | ---- | ---- | ---- | ---- | ---- |
|12 min|790|836|868|808|454|412|
|16 min|793|856|871|845|556|530|
|20 min|795|863|873|864|617|623|
石灰石煅烧的最佳温度范围一般为1100~1200$℃$的证据是________________________。
I.碳酸钙与稀盐酸反应

(1)装置A中仪器a的名称为__________。
(2)装置B中的现象是____________________。
(3)装置C若用于检验生成的气体,其中试剂为__________(写名称),发生反应的化学方程式为______________________________。
II.碳酸钙分解
碳酸钙在电炉中高温煅烧一段时间后,对剩余固体进行探究。
[提出问题]剩余固体成分是什么?
[猜想与假设]猜想一:全部是碳酸钙
猜想二:是碳酸钙和氧化钙的混合物
猜想三:全部是氧化钙
[设计并完成实验]
|实验操作|实验现象|解释与结论|
| ---- | ---- | ---- |
|步骤一:取剩余固体于试管中,加水振荡后静置|底部有白色不溶物| |
|步骤二:取上层清液于另一试管中,滴加氯化铜溶液|________|上层清液中一定含有氢氧化钙|
|步骤三:取部分底部白色不溶物于第三支试管中,滴加过量稀盐酸|有气泡产生|白色不溶物中一定含有________|
[实验结论]正确的猜想是________。
[交流与反思]小芳同学认为,步骤二中还可滴加其他试剂用来替代氯化铜溶液,该试剂可以是__________(写一种即可);小华同学认为,只需完成步骤一和步骤三即可获得相同实验结论,他的依据是__________________。
[拓展与分析]查阅资料:生石灰质量的优劣常采用“活性度”来衡量。“活性度”的测定方法:取一定质量的生石灰,加入一定量的水,用一定溶质质量分数的盐酸中和,记录所消耗盐酸的体积(单位为mL)。消耗盐酸的体积数越大,“活性度”越高。
测得煅烧产物($CaO$)的活性度,数据见如表。
|煅烧时间
活性度
煅烧温度|1050$℃$|1100$℃$|1150$℃$|1200$℃$|1250$℃$|1300$℃$|
| ---- | ---- | ---- | ---- | ---- | ---- | ---- |
|12 min|790|836|868|808|454|412|
|16 min|793|856|871|845|556|530|
|20 min|795|863|873|864|617|623|
石灰石煅烧的最佳温度范围一般为1100~1200$℃$的证据是________________________。
答案:
Ⅰ.
(1) 锥形瓶
(2) 石蕊试液变红色
(3) 澄清石灰水 ${CO_{2} + Ca(OH)_{2}=CaCO_{3}\downarrow + H_{2}O}$
Ⅱ. 【设计并完成实验】有蓝色沉淀产生 碳酸钙
【实验结论】猜想二 【交流与反思】无色酚酞溶液 氧化钙和水反应放热,温度升高,即可知道剩余固体中有氧化钙
【拓展与分析】煅烧时间长短不同,在 1100~1200 ${^{\circ}C}$ 范围内生石灰的活性度均高
(1) 锥形瓶
(2) 石蕊试液变红色
(3) 澄清石灰水 ${CO_{2} + Ca(OH)_{2}=CaCO_{3}\downarrow + H_{2}O}$
Ⅱ. 【设计并完成实验】有蓝色沉淀产生 碳酸钙
【实验结论】猜想二 【交流与反思】无色酚酞溶液 氧化钙和水反应放热,温度升高,即可知道剩余固体中有氧化钙
【拓展与分析】煅烧时间长短不同,在 1100~1200 ${^{\circ}C}$ 范围内生石灰的活性度均高
查看更多完整答案,请扫码查看


