第73页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
例 1 (2024·西工大附中期中)氢气是未来汽车的理想燃料。1 kg 的氢气就能供一辆功率为 50 kW 的汽车跑大约 100 km,请你计算得到 1 kg 氢气需要电解多少千克的水?
答案:
解:设得到1kg氢气需要电解水的质量为$x$。
$2\mathrm{H}_2\mathrm{O}\stackrel{通电}{=\!=\!=}2\mathrm{H}_2\uparrow+\mathrm{O}_2\uparrow$
36 4
$x$ 1kg
$\frac{36}{4}=\frac{x}{1\mathrm{kg}}$ $x=9\mathrm{kg}$
答:得到1kg氢气需要电解9kg的水。
$2\mathrm{H}_2\mathrm{O}\stackrel{通电}{=\!=\!=}2\mathrm{H}_2\uparrow+\mathrm{O}_2\uparrow$
36 4
$x$ 1kg
$\frac{36}{4}=\frac{x}{1\mathrm{kg}}$ $x=9\mathrm{kg}$
答:得到1kg氢气需要电解9kg的水。
例 2 工业上煅烧石灰石产生的生石灰(CaO)和二氧化碳可分别用于生产建筑材料和化肥。现有 250 kg 石灰石样品(石灰石中的杂质高温时不参与反应),该石灰石样品中碳酸钙的含量为 80%,请计算:
(1)250 kg 该石灰石样品中碳酸钙的质量。
(2)煅烧 250 kg 该石灰石样品,最多可以得到生石灰的质量。
(1)250 kg 该石灰石样品中碳酸钙的质量。
(2)煅烧 250 kg 该石灰石样品,最多可以得到生石灰的质量。
答案:
(1)250kg该石灰石样品中碳酸钙的质量为$250\mathrm{kg}×80\%=200\mathrm{kg}$
(2)解:设最多可以得到生石灰的质量为$x$。
$\mathrm{CaCO}_3\stackrel{高温}{=\!=\!=}\mathrm{CaO}+\mathrm{CO}_2\uparrow$
100 56
200kg $x$
$\frac{100}{56}=\frac{200\mathrm{kg}}{x}$ $x=112\mathrm{kg}$
答:
(1)250kg该石灰石样品中碳酸钙的质量为200kg。
(2)煅烧后最多可以得到生石灰的质量为112kg。
(1)250kg该石灰石样品中碳酸钙的质量为$250\mathrm{kg}×80\%=200\mathrm{kg}$
(2)解:设最多可以得到生石灰的质量为$x$。
$\mathrm{CaCO}_3\stackrel{高温}{=\!=\!=}\mathrm{CaO}+\mathrm{CO}_2\uparrow$
100 56
200kg $x$
$\frac{100}{56}=\frac{200\mathrm{kg}}{x}$ $x=112\mathrm{kg}$
答:
(1)250kg该石灰石样品中碳酸钙的质量为200kg。
(2)煅烧后最多可以得到生石灰的质量为112kg。
例 3 (2024·汉中宁强县期末)实验室有一瓶含有少量杂质的高锰酸钾试剂,某化学兴趣小组的同学为了测定其中高锰酸钾的质量分数,取 40 g 样品持续加热,剩余固体的质量与加热时间的关系如图所示。请完成下列分析与计算:
(1)充分反应后,生成氧气的质量为
(2)计算该样品中高锰酸钾的质量分数。
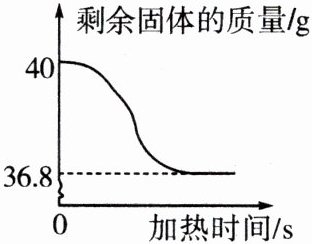
(1)充分反应后,生成氧气的质量为
3.2
g。(2)计算该样品中高锰酸钾的质量分数。

答案:
(1)3.2
(2)解:设混合物中高锰酸钾的质量是$x$。
$2\mathrm{KMnO}_4\stackrel{\triangle}{=\!=\!=}\mathrm{K}_2\mathrm{MnO}_4+\mathrm{MnO}_2+\mathrm{O}_2\uparrow$
316 32
$x$ 3.2g
$\frac{316}{32}=\frac{x}{3.2\mathrm{g}}$ $x=31.6\mathrm{g}$
该样品中高锰酸钾的质量分数为$\frac{31.6\mathrm{g}}{40\mathrm{g}}×100\%=79\%$
答:该样品中高锰酸钾的质量分数为79%。
(1)3.2
(2)解:设混合物中高锰酸钾的质量是$x$。
$2\mathrm{KMnO}_4\stackrel{\triangle}{=\!=\!=}\mathrm{K}_2\mathrm{MnO}_4+\mathrm{MnO}_2+\mathrm{O}_2\uparrow$
316 32
$x$ 3.2g
$\frac{316}{32}=\frac{x}{3.2\mathrm{g}}$ $x=31.6\mathrm{g}$
该样品中高锰酸钾的质量分数为$\frac{31.6\mathrm{g}}{40\mathrm{g}}×100\%=79\%$
答:该样品中高锰酸钾的质量分数为79%。
查看更多完整答案,请扫码查看


