2026年王朝霞考点梳理时习卷九年级化学全一册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年王朝霞考点梳理时习卷九年级化学全一册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
1.下列关于质量守恒定律的说法正确的是
(
A.反应前各物质的质量总和,一定等于反应后生成的各物质的质量总和
B.参加化学反应的各物质的分子个数与反应后各生成物的分子个数相等
C.质量守恒定律只适用于有气体或固体生成的化学反应
D.参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和
(
D
)A.反应前各物质的质量总和,一定等于反应后生成的各物质的质量总和
B.参加化学反应的各物质的分子个数与反应后各生成物的分子个数相等
C.质量守恒定律只适用于有气体或固体生成的化学反应
D.参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和
答案:
1.D
2.[南阳市]双氧水分解生成水和氧气的反应前后,发生改变的是 (
A.元素种类
B.原子种类
C.分子种类
D.原子数目
C
)A.元素种类
B.原子种类
C.分子种类
D.原子数目
答案:
2.C
3. 课后题改编 下列现象不能用质量守恒定律解释的是 (
A.烧杯中的水蒸发一部分后,剩余的水质量减小
B.纸在空气中燃烧后化为灰烬,灰烬的质量比纸的质量小
C.镁条燃烧,生成物的质量比镁条质量大
D.高锰酸钾受热分解后,剩余固体的质量比高锰酸钾的质量小
A
)A.烧杯中的水蒸发一部分后,剩余的水质量减小
B.纸在空气中燃烧后化为灰烬,灰烬的质量比纸的质量小
C.镁条燃烧,生成物的质量比镁条质量大
D.高锰酸钾受热分解后,剩余固体的质量比高锰酸钾的质量小
答案:
3.A
4.[郑州市]氯碱工业的反应原理是电解饱和的食盐水(主要成分为$NaCl$和$H_2O$),
电解饱和食盐水的产物不可能是(
A.$H_2$
B.$Cl_2$
C.$Na_2CO_3$
D.$NaOH$
电解饱和食盐水的产物不可能是(
C
)A.$H_2$
B.$Cl_2$
C.$Na_2CO_3$
D.$NaOH$
答案:
4.C
5. 现代科技情境 零碳甲醇 杭州亚运会首次使用零碳甲醇燃料助力碳中和。已知甲醇与氧气燃烧生成二氧化碳和水,由此推知甲醇中 (
A.一定含碳、氢元素,可能含氧元素
B.一定含碳、氢元素,不含氧元素
C.一定含碳、氢、氧元素
D.无法确定
A
)A.一定含碳、氢元素,可能含氧元素
B.一定含碳、氢元素,不含氧元素
C.一定含碳、氢、氧元素
D.无法确定
答案:
5.A [解析]甲醇与氧气燃烧生成二氧化碳和水,二氧化碳中的碳元素和水中的氢元素均来自甲醇,而二氧化碳中的氧元素和水中的氧元素可能来自甲醇和氧气,也可能完全来自氧气,因此甲醇中一定含碳、氢元素,可能含氧元素。故选A。
6.[天津中考]现将20 g A和足量B在一定条件下充分反应,生成16 g C和11 g D,则参加反应的A和B的质量比是
(
A.20 : 11
B.20 : 7
C.5 : 4
D.16 : 11
(
B
)A.20 : 11
B.20 : 7
C.5 : 4
D.16 : 11
答案:
6.B [解析]根据质量守恒定律可知,参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和,所以参加反应的B的质量为16g +11g−20g=7g,则参加反应的A和B的质量比是20:7。故选B。
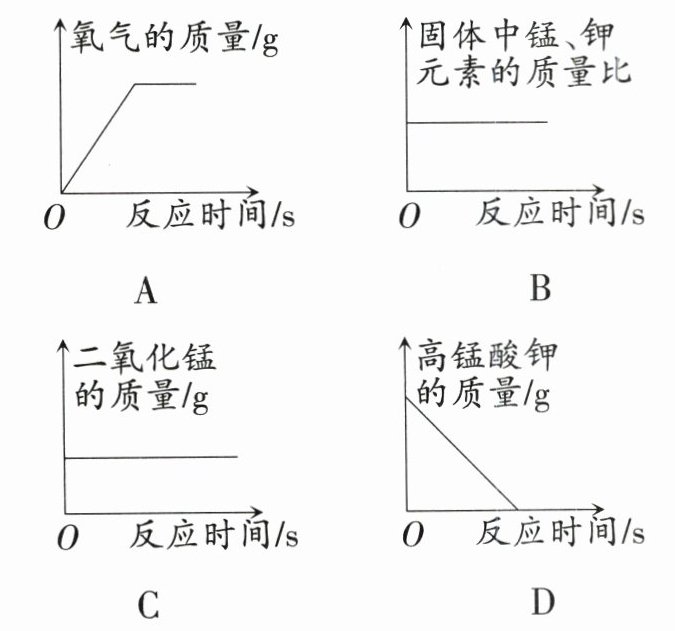
7. 实验室使用一定质量的高锰酸钾加热分解制氧气,下列图像表示受热过程中某些量随反应时间变化的趋势,其中错误的为
(
A
B
C
D
(
C
)A
B
C
D
答案:
7.C [解析]加热一定质量的高锰酸钾,反应生成锰酸钾、二氧化锰和氧气,随着反应的进行,氧气和二氧化锰的质量不断增大,高锰酸钾的质量不断减小,至高锰酸钾反应完全,氧气和二氧化锰的质量不再变化,A、D正确,C错误;反应前后锰元素和钾元素均存在于固体中,根据质量守恒定律可知,反应前后锰元素和钾元素的质量均不发生变化,故固体中锰、钾元素的质量比不变,B正确。故选C。
8.[石家庄市]把一定质量的甲、乙、丙、丁放入一个密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下表。下列说法不正确的是
(
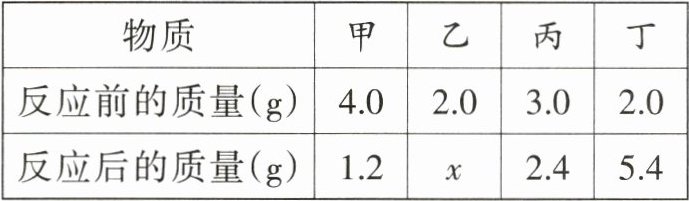
物质
甲
乙
丙
丁
反应前的质量(g)
4.0
2.0
3.0
2.0
反应后的质量(g)
1.2
$x$
2.4
5.4
A. 该反应是化合反应
B. $x=2.0$,乙可能是催化剂
C. 参加反应的甲、丙的质量比是1 : 2
D. 丙可能是单质
(
C
)
物质
甲
乙
丙
丁
反应前的质量(g)
4.0
2.0
3.0
2.0
反应后的质量(g)
1.2
$x$
2.4
5.4
A. 该反应是化合反应
B. $x=2.0$,乙可能是催化剂
C. 参加反应的甲、丙的质量比是1 : 2
D. 丙可能是单质

答案:
8.C [解析]根据质量守恒定律可知,x=4.0+2.0 +3.0+2.0−1.2−2.4−5.4=2.0。反应前后甲、丙的质量减小,为反应物;丁的质量增大,为生成物;乙的质量不变,可能是该反应的催化剂,也可能未参与反应。所以该反应为化合反应,A、B正确;参加反应的甲、丙的质量比是(4.0g−1.2g):(3.0g−2.4g)=14:3,C错误;丙为反应物,可能为单质,D正确。故选C。
查看更多完整答案,请扫码查看


