20. (10分)下表是元素周期表中1~18号元素的排列情况,根据此表进行探究。

(1)第13号元素属于________(填“金属”或“非金属”)元素,它的原子在化学反应中容易________(填“得”或“失”)电子,它的离子符号为________。
(2)研究表明:在同一周期中,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强。由此推断:第三周期中得电子能力最强的是________(填元素符号,下同)原子;失电子能力最强的是________原子,具有稳定结构的是________原子。
(3)某元素的原子结构示意图为 ,则它位于元素周期表中的第________周期,该元素的化学性质与上表中________族元素的化学性质相似。
,则它位于元素周期表中的第________周期,该元素的化学性质与上表中________族元素的化学性质相似。
(4)已知某微粒的结构示意图为 ,请写出该微粒的符号:________。
,请写出该微粒的符号:________。
(5)表中Ne和Ar的化学性质相似的原因是________。

(1)第13号元素属于________(填“金属”或“非金属”)元素,它的原子在化学反应中容易________(填“得”或“失”)电子,它的离子符号为________。
(2)研究表明:在同一周期中,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强。由此推断:第三周期中得电子能力最强的是________(填元素符号,下同)原子;失电子能力最强的是________原子,具有稳定结构的是________原子。
(3)某元素的原子结构示意图为
 ,则它位于元素周期表中的第________周期,该元素的化学性质与上表中________族元素的化学性质相似。
,则它位于元素周期表中的第________周期,该元素的化学性质与上表中________族元素的化学性质相似。(4)已知某微粒的结构示意图为
 ,请写出该微粒的符号:________。
,请写出该微粒的符号:________。(5)表中Ne和Ar的化学性质相似的原因是________。
答案:
(1)金属 失 Al³⁺
(2)Cl Na Ar
(3)五 ⅦA
(4)O²⁻
(5)原子的最外层电子数相同
(2)Cl Na Ar
(3)五 ⅦA
(4)O²⁻
(5)原子的最外层电子数相同
21. (11分)在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
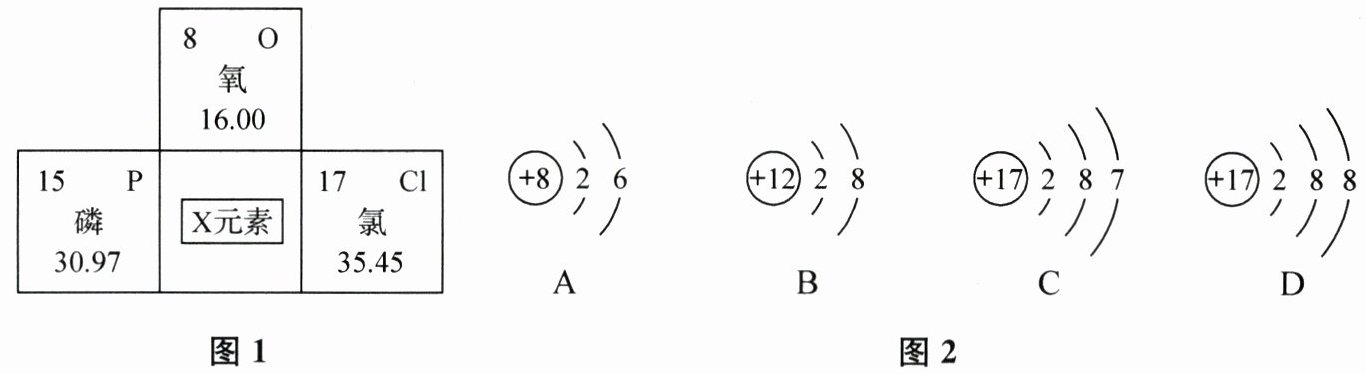
(1)下列说法不正确的是________(填字母)。
A. 氯原子的质子数为17,最外层电子数为7
B. 磷的相对原子质量为30.97g
C. X元素的原子序数为16,元素名称为硫,元素符号为S
D. X元素与磷、氯元素位于同周期,与氧元素位于同一族
(2)一种碳原子叫作碳12,是含有6个质子和6个中子的碳原子,一个碳12原子的质量为$a$g,则一个氧原子的质量为________(用含$a$的代数式表示)。
(3)图2所示粒子共表示________种元素,X元素的化学性质与图2中________(填字母)的化学性质相似。
(4)下图为某化学反应的微观示意图:
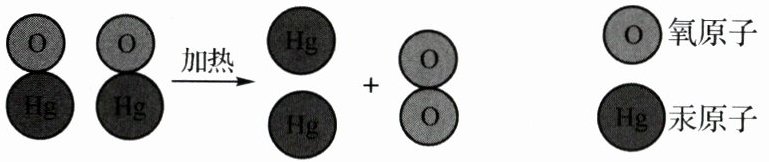
①该反应中没有变化的粒子是________。
②写出该反应的文字表达式:________。

(1)下列说法不正确的是________(填字母)。
A. 氯原子的质子数为17,最外层电子数为7
B. 磷的相对原子质量为30.97g
C. X元素的原子序数为16,元素名称为硫,元素符号为S
D. X元素与磷、氯元素位于同周期,与氧元素位于同一族
(2)一种碳原子叫作碳12,是含有6个质子和6个中子的碳原子,一个碳12原子的质量为$a$g,则一个氧原子的质量为________(用含$a$的代数式表示)。
(3)图2所示粒子共表示________种元素,X元素的化学性质与图2中________(填字母)的化学性质相似。
(4)下图为某化学反应的微观示意图:

①该反应中没有变化的粒子是________。
②写出该反应的文字表达式:________。
答案:
(1)B
(2)$\frac{4a}{3}$g
(3)3 A
(4)①汞原子、氧原子 ②氧化汞$\xrightarrow{加热}$汞+氧气
(2)$\frac{4a}{3}$g
(3)3 A
(4)①汞原子、氧原子 ②氧化汞$\xrightarrow{加热}$汞+氧气
查看更多完整答案,请扫码查看


