【题目】请根据下列装置如图1,回答问题:
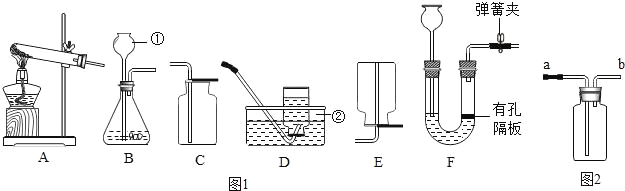
(1)写出标号①②的仪器名称:①_____,②_____.
(2)某同学想要用高锰酸钾制制取一瓶较干燥的氧气,他应该选择_____组合.装置A还需做的一点改动是_____,写出高锰酸钾制取氧气的化学方程式_____.
(3)如果选择BD组合可以制取_____气体,写出该反应的化学方程式_____.
(4)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过溶解、过滤、_____干燥就能得到纯净的二氧化锰固体.
(5)把(4)中滤液蒸发结晶可得到氯化钾晶体,在蒸发操作中玻璃棒的作用是_____.
(6)若选择装置F作为制取氢气的发生装置,其优点是_____.如果如图2所示的装置来收集一瓶氧气,验满时应该将带火星的木条放在_____.(选填“a”或“b”)导管口处.
参考答案:
【答案】长颈漏斗 水槽 AC 在试管口放一团棉花 2KMnO4![]() K2MnO4+MnO2+O2↑ 氧气或氢气 2H2O2
K2MnO4+MnO2+O2↑ 氧气或氢气 2H2O2![]() 2H2O+O2↑(或Zn+H2SO4═ZnSO4+H2↑) 洗涤 搅拌,防止液体受热不均而飞溅 可以控制反应的发生和停止 b
2H2O+O2↑(或Zn+H2SO4═ZnSO4+H2↑) 洗涤 搅拌,防止液体受热不均而飞溅 可以控制反应的发生和停止 b
【解析】
(1)标号①②的仪器分别是长颈漏斗和水槽;
(2)高锰酸钾制取氧气需要加热,属于固体加热型,故选发生装置A,氧气的密度比空气大,因此制取干燥的氧气用向上排空气法;该反应试管口要放一团棉花,防止加热时高锰酸钾粉末进入导管,方程式是2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)BD组合可制取的气体是:反应物是固体和液体,且不需加热,不溶于水的气体;实验室利用二氧化锰催化过氧化氢制取氧气,锌和稀硫酸反应制取氢气均不需加热,可用此套装置,因为氧气不易溶于水,氢气难溶于水,均可用排水法收集;方程式分别是:2H2O2![]() 2H2O+O2↑、Zn+H2SO4═ZnSO4+H2↑;
2H2O+O2↑、Zn+H2SO4═ZnSO4+H2↑;
(4)氯化钾溶于水,二氧化锰不溶于水,因此可以用溶解、过滤、洗涤、干燥的方法得到二氧化锰;
(5)滤液蒸发结晶可得到氯化钾晶体,在蒸发操作中玻璃棒的作用是搅拌,防止液体局部过热飞溅出来;
(6)F装置中弹簧夹打开,固体和液体接触生成气体,关闭弹簧夹,U型管内气压增大,将液体压入长颈漏斗,固液分离,反应停止,故该装置最大的优点就是可随时控制反应的发生和停止;氧气的密度比空气大,因此应从长导管进气,故验满时带火星的木条应放在短导管口;
故答案为:(1)长颈漏斗;水槽;
(2)AC;在试管口放一团棉花;2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)氧气(或氢气);2H2O2![]() 2H2O+O2↑(或Zn+H2SO4═ZnSO4+H2↑);
2H2O+O2↑(或Zn+H2SO4═ZnSO4+H2↑);
(4)洗涤;
(5)搅拌,防止液体受热不均而飞溅;
(6)可以控制反应的发生和停止;b.
-
科目: 来源: 题型:
查看答案和解析>>【题目】图1是从元素周期表中截取的四种元素的信息,请回答下列问题:
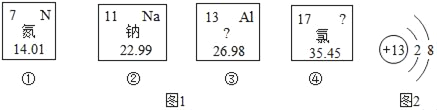
(1)①元素原子的相对原子质量是_____;
(2)③元素的一种微粒的结构示意图如图2,它属于_____(填“金属元素”或“非金属元素”或“稀有气体元素”),该微粒的符号为_____;
(3)由②与④形成化合物的化学式是_____,是由_____ (原子、分子、离子)构成。
-
科目: 来源: 题型:
查看答案和解析>>【题目】复方冬青软膏具有强力迅速镇痛作用,其有效成分A的分子模型如图所示。
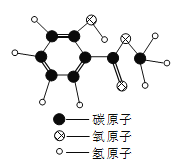
(1)A物质属于_____物(填“纯净”或“混合”)。
(2)A物质的化学式为_____。
(3)A物质中碳、氢的原子个数比为_____(填最简比)。
(4)A物质中碳元素的质量分数为_____(结果精确到0.1%)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如同氧元素一样,碳元素的单质及化合物在生产生活实际中也有着十分广泛的应用。请根据你掌握的知识回答下列问题:
(1)重要档案或票据,一殷都要求运用碳素墨水笔书写,其理论依据是_____。
(2)焦炭是工业上高炉炼铁的重要原料之一,它们在高炉中发生了一系列化学反应,其中CO使氧化铁转化为铁,就是最重要的反应之一,请写出该反应的化学方程式:_____。
(3)小章同学准备在实验室用下图所示装置模拟工业炼铁。
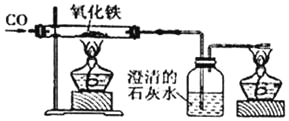
其中:
①实验中产生的现象主要有:_____。
②装置图中澄清石灰水的作用是_____,其中所发生的反应的化学方程式是_____。
③某同学实验完成后,发现过量的澄清石灰水增重4.4g,则该同学通入装置的CO气体质量肯定大于_____,其理由是_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(9分)水蒸气通过灼热的焦炭后得到的混合气体有哪些成分?某化学兴趣小组在老师的指导下,对此进行了实验探究。
【提出猜想】1.该混合气体只含有一氧化碳、氢气
2.该混合气体含有一氧化碳、二氧化碳、氢气和水蒸气
3.该混合气体只含有二氧化碳、氢气和水蒸气
4.该混合气体只含有一氧化碳、二氧化碳和氢气
【查阅资料】a.无水硫酸铜遇水由白色变为蓝色。
b.碱石灰是固体氢氧化钠和氧化钙的混合物。
c.浓硫酸具有强烈的吸水性,常用作某些气体的干燥剂
【实验过程】同学们在老师的指导下设计了如下图所示装置,并进行了实验(部分夹持仪器已略去)。
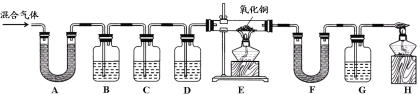
(1)装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊,由此得出的结论为混合气体中有 。B中变化的化学方程式为 。
(2)装置C中的药品为 。
(3)E中氧化铜变红、F中无水硫酸铜变蓝、G中澄清石灰水变浑浊,说明混合气体中还存在的气体是 ; E中的变化说明氧化铜具有 性。
【实验结论】猜想 正确。
【实验反思】
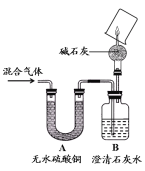
经过讨论,同学们将上图中装置C~H进行了简化,只 用下图所示装置并自选必要试剂就能完成探究。其中,干燥管中碱石灰的作用为 , 烧杯上能观察到的现象是 。最后一步的实验操作及现象是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知A﹣E都是初中化学中的常见物质,其中A和D是无色无味气体,B是黑色粉末,C是红色固体,它们的转化关系如图所示(部分反应的反应条件或生成物已省略).
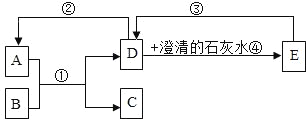
(1)写出C物质的化学式:_____.
(2)写出反应①的化学方程式:_____;若反应③的反应条件是高温,请写出反应③的化学方程式:_____,属于_____反应(填基本反应类型).
(3)D能转化为A,还需要的物质是_____.
-
科目: 来源: 题型:
查看答案和解析>>【题目】在实验室制取氧气时,取MnO2和KClO3的固体混合物15.25g,加热至不再产生气体为止,收集到一定质量的氧气。某化学兴趣小组欲求得所制氧气的质量,他们将加热后剩余物冷却到一定温度后,通过多次加水测定剩余物质量的办法即可求出。加水的质量与剩余固体的质量见下表:(MnO2是不溶于水的固体粉末)
编号
1
2
3
4
加水的质量(g)
10
10
10
10
剩余固体的质量(g)
7.25
4.05
m
3
试求:
(1)表中m值为_____;
(2)混合物中KClO3的质量_____;
(3)所制得氧气的质量____恰好完全反应后固体中氯化钾的质量分数____(写出具体计算过程,质量分数保留0.01%)。
相关试题

