40.某学校的学习小组对当地的石灰石矿区进行调查,欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16g,把80g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,不与稀盐酸反应)。
|
实验次数 |
1 |
2 |
3 |
4 |
|
加入稀盐酸的质量/g |
20 |
20 |
20 |
20 |
|
剩余固体的质量/g |
11 |
6 |
2.8 |
n |
根据实验数据计算:
(1)表中n的数值为 。
(2)样品中碳酸钙的质量分数是 。
(3)盐酸中溶质的质量分数 。
39.镁条在空气中易被氧化,有一根在空气中放置一段时间的镁条样品,其质量为2.56g,把该样品与足量的稀硫酸反应得到氢气0.18g。请计算:
(1)样品中未被氧化的镁的质量是多少?
(2)该镁条未被氧化时的质量是多少?
38.(6分)某同学对盐酸溶液与氢氧化钠溶液的反应,按下图所示过程进行探究:

(1)填充实验过程空格项:
|
实 验 步 骤 |
实 验 现 象 |
实 验 结 论 |
|
|
步骤① |
取适量NaOH溶液放入烧杯中,滴入几滴酚酞试液。 |
。 |
 |
|
步骤② |
用胶头滴管将稀盐酸慢慢逐滴滴入到步骤①所得的溶液中,
。 |
溶液颜色逐渐变浅直至到无色。 |
氢氧化钠与稀盐酸反应。 |
|
步骤③ |
当滴加稀盐酸至发生上述现象出现,立即停止。 |
 |
 |
|
步骤④ |
将③所得溶液移入广口瓶,并与盛有浓硫酸的广口瓶用导管连接导通,放置一段时间。 |
。 |
。 |
(2)模型探究:对上述过程采用微观模型加以认识,如下图:
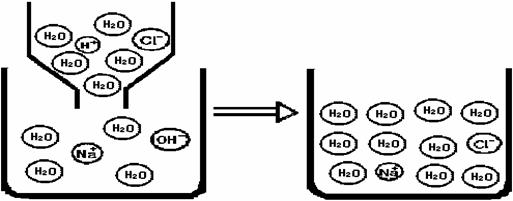
①.氢氧化钠溶液与盐酸反应。反应中消失的离子有:
②.上图微观模型所反映的NaCl溶液溶质的质量分数:
37.(6分)铁暴露在空气中会生锈。切开的苹果放置不久,果肉上也会产生一层咖啡色的物质,也好象是生了“锈”一样。某化学活动组对此进行了探究。
[提出问题]切开的苹果“生锈”与什么因素有关?
[猜想与假设]
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”。
猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”;
猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”;
猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”;
猜想⑤:可能果肉中的物质与空气作用而“生锈”的速度还与温度有关。
[查阅资料] 苹果果肉里的物质(酚和酶)与空气接触发生反应,生成咖啡色的物质。
[实验探究]针对以上猜想,活动组认为实际上可以排除 。但他们仍对所有猜想设计了如下图所示的实验方案进行了验证,并观察到实验现象。

请你完成下表中空余部分。
|
猜想 |
实验设计及装置 |
观察到的实验现象 |
|
猜想① |
A |
果肉表面不变色 |
|
猜想② |
C |
|
|
猜想③ |
D |
果肉表面不变色 |
|
猜想④ |
E |
|
|
猜想⑤ |
|
温度高的先变色。 |
[得出结论]苹果果肉里的物质(酚和酶)与空气中氧气发生了反应,生成咖啡色的物质。
[反思与评价]在验证猜想①时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变色,其原因是 。
[应用]根据上述结论,要防止果汁变质,加工和保存果汁时可采取的措施是:
。
36.(6分) 结合下列实验装置图回答问题:
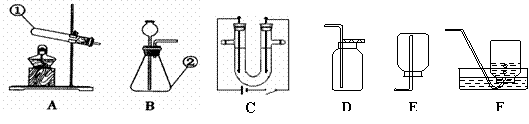
(1)写出指定仪器的名称:① ②
(2)实验室中通常可用 装置制得氧气,可用 装置收集氧气。
写出用高锰酸钾制氧气的化学方程式: 。
(3)实验室制取二氧化碳时,可选用的装置是 。
33.(4分)现在市场上食品保鲜的方式多种多样。
①一类做法是直接在食品中添加防腐剂,其中山梨酸钾(化学式为C6H7O2K)是常用的一种,山梨酸钾中碳、氢、氧、钾元素的原子个数比是 。
②另一类做法是对那些易受挤压破碎的小食品充填保护气体,其中氮气是首选,其目的是 。
③第三类做法是放置脱氧保鲜剂,当打开食品包装袋后,里面常见标有“禁止食用” 字样的一小纸包物质,将纸包里黑色物质倒入盛有盐酸的试管内,产生气泡,该纸包里最初所装入的估计是 。
④用PE塑料保鲜膜包裹,是对新鲜蔬菜及水果保鲜广泛使用的做法。保鲜膜具有调节内外O2、CO2平衡和保留内部果蔬水分的作用,这一现象说明的微观事实是______ _ ___。
34.(5分)用如图所示装置进行实验:
(1)当打开止水夹,挤压滴管将液体A滴入试管①时,观察到试管②有气泡产生。
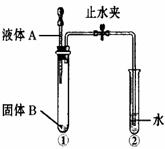 ①若固体B来源于饮料罐,写出一合理的化学反应方程式:
①若固体B来源于饮料罐,写出一合理的化学反应方程式:
。
②若固体B来源于废电池,且发生分解反应,写出一合理的
化学反应方程式: 。
③若液体A遇固体B发生化合反应,写出一合理的化学反应
方程式: 。
④若固体B来源于厨房用品,写出一合理的化学反应方程式:
。
(2)当打开止水夹,挤压滴管将液体A滴入试管①时,观察到试
管②中的水慢慢被倒吸于导气管内一段,固体B可做化肥,固体B是 。
35.(4分)如图已知A、B、C、D、E、F为六种常见化合物相互反
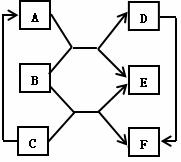 应及转化关系,B通常为无色气体,E通常为无色液体,请回答:
应及转化关系,B通常为无色气体,E通常为无色液体,请回答:
(1)B的化学式为 ;
(2)D的俗称是 ;
(3)B与C反应生成E和F的化学方程式:
;
(4)C → A反应的化学方程式:
。
32.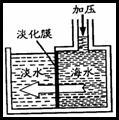 (6分)我国东依广阔的大海,具有丰富的海洋资源。
(6分)我国东依广阔的大海,具有丰富的海洋资源。
(1)我国是内陆缺水比较严重的国家,将丰富的海水经过淡化膜处理既
可以得到淡水输往内陆,以解决工业和生活用水困难。该过程是通
过 变化实现的。
(2)海低蕴藏有丰富的石油天然气资源。
①天然气燃烧用化学方程式表示为 。
②化石类资源的开采和使用,会产生大量“温室气体”,为减少“温室气体”的形成,则对海洋资源利用研究应着力于以下___ ___ _。
A. 海洋风力发电 B. 海水潮汐发电 C. 海洋地热开发 D.制氢储氢系列
(3)通过晒海水可以得到粗盐。粗盐中含有泥沙、氯化钙等杂质,可通过下列步骤制取精盐:
a → 加过量的Na2CO3溶液 → b → 加适量的盐酸 → c
①操作a、b、c中均使用的仪器是 。
②加过量Na2CO3的作用,用化学方程式表示为: ;
③加适量的盐酸的目的,用化学方程式表示为: .
31.(7分)科技推动着奥林匹克运动的发展,化学的表现十分突出。
 (1)右图:“鸟巢”的建造中使用了大量的钢铁。生产这些钢铁时首先要将铁矿石(Fe2O3)在高温下用一氧化碳还原成生铁,其化学方程式为
;“水立方”的膜结构是由化学合成材料ETFT制成的,其化学式是(C2H2F2)n ,则其相对分子质量的计算式是
。
(1)右图:“鸟巢”的建造中使用了大量的钢铁。生产这些钢铁时首先要将铁矿石(Fe2O3)在高温下用一氧化碳还原成生铁,其化学方程式为
;“水立方”的膜结构是由化学合成材料ETFT制成的,其化学式是(C2H2F2)n ,则其相对分子质量的计算式是
。
(2)奥运参赛者不断利用新科技成果助推其实现“更高、更快、更强”。
 如图:
如图:
连体紧身泳装“快皮” “红色魔鞋”及碳纤维 玻璃纤维杆
①撑杆跳高用上是玻璃纤维杆,使撑杆跳高纪录得以腾飞。玻璃纤维主要组成成分是SiO2、Al2O3等,在物质分类中他们属于 。
A.单质 B. 化合物 C. 有机物 D. 无机物 E. 氧化物
②连体紧身泳装快皮的面料为一种特细尼龙,具有延展性强,吸水率极低,水的阻力小,质量轻、速度快的特点。关于快皮的面料所述的特点在化学中属于 。
A.物理性质 B. 化学性质
③耐克公司为刘翔参加奥运会专门制做的跑鞋人称“红色魔鞋”,其良好的性能主要是因为它使用了一种叫做碳纤维的制作材料。将普通有机合成纤维在惰性气流中高温分解就可以得到碳纤维,则这里惰性气体的作用是 。
(3)奥运比赛对运动员食物及饮品要科学合理,对此你的建议是:
①跑、跳、投、举重、游泳等赛前应多进食 ,有利于创造好的成绩。
A.米饭及各种面食 B. 鸡蛋及各种肉类 C.水果及各种蔬菜 D. 油炸或油焖食物
②赛后要多喝些运动饮品,可做该种饮品的是 。
A.含矿物质、微量元素、维生素、糖的饮料 B. 糖水 C. 纯水 D. 啤酒
30.锌粉、铝粉、镁粉的混合物3.8g与一定质量的稀硫酸恰好完全反应,将反应后的混合物蒸发水份得固体硫酸锌、硫酸铝、硫酸镁混合物11g,则反应中生成氢气的质量为
A.0.15g B.0.20g C.0.30g D.0.45g
第Ⅱ卷(非选择题 共50分)

