【题目】ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛.某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究. 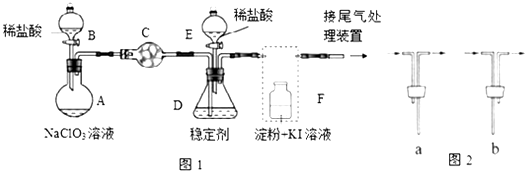
(1)仪器D的名称是 , 仪器E的名称是 . 安装F中导管时,应选用图2中的 .
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O,这个反应中氧化剂和还原剂的物质的量之比为 , 为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜(填“快”或“慢”).
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2 , 此时F中溶液的颜色不变,则装置C的作用是 .
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2 , 该反应的离子方程式为 , 在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是 .
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示.若将其用于水果保鲜,你认为效果较好的稳定剂是 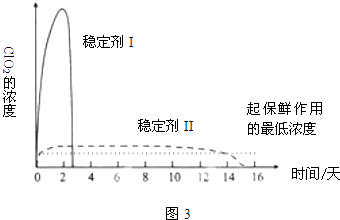
参考答案:
【答案】
(1)锥形瓶;分液漏斗;b
(2)1:1;慢
(3)吸收Cl2
(4)4H++5ClO2﹣=Cl﹣+4ClO2↑+2H2O;验证是否有ClO2生成
(5)稳定剂Ⅱ
【解析】解:(1)根据仪器特征,可知仪器D是锥形瓶;仪器E带有球形特征且带有玻璃活塞,为分液漏斗,F装置应是Cl2和KI反应,还需要连接尾气处理装置,所以应长管进气,短管出气,故选b,故答案为:锥形瓶;分液漏斗;b;
(2.)2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O反应中,2HCl→Cl2 , ﹣1价的氯元素化合价升高到0价,所以4HCl中2HCl是还原剂,2NaClO3→2ClO2 , +5价的氯元素的化合价降低到+4价,所以NaClO3作氧化剂;所以该反应中氧化剂和还原剂的物质的量之比为2:2=1:1,为使ClO2在D中被稳定剂充分吸收,产生ClO2的速率要慢,故滴加稀盐酸的速度要慢,故答案为:1:1;慢;
(3.)F装置中发生Cl2+2KI=2KCl+I2时,碘遇淀粉变蓝,而F中溶液的颜色不变,则装置C的作用是吸收Cl2 , 故答案为:吸收Cl2;
(4.)在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2 , 根据元素守恒可知应还有水生成,该反应的离子方程式为:4H++5ClO2﹣=Cl﹣+4ClO2↑+2H2O; 在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是验证是否有ClO2 生成,故答案为:4H++5ClO2﹣=Cl﹣+4ClO2↑+2H2O;验证是否有ClO2 生成;
(5.)由图可知,稳定剂Ⅱ可以缓慢释放ClO2 , 能较长时间维持保鲜所需的浓度,所以稳定剂Ⅱ好,故答案为:稳定剂Ⅱ.
装置A中盛放NaClO3溶液,装置B盛放稀盐酸,两者发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O,装置C的作用是吸收Cl2 , 除去氯气,ClO2在装置D中被稳定剂完全吸收生成NaClO2 , 在酸性条件下NaClO2可发生反应4H++5ClO2﹣=Cl﹣+4ClO2↑+2H2O生成NaCl并释放出ClO2 , 装置F检验二氧化氯中氯气是否完全被装置C吸收.(1)根据仪器特征,可知仪器D是锥形瓶;F装置应是Cl2和KI反应,还需要连接尾气处理装置,所以应长管进气,短管出气;(2)根据在反应物中,化合价降低的物质是氧化剂,化合价升高的物质是还原剂来分析解答;为使ClO2在D中被稳定剂充分吸收,产生ClO2的速率要慢;(3)F装置中发生Cl2+2KI=2KCl+I2时,碘遇淀粉变蓝,而F中溶液的颜色不变,说明Cl2被吸收;(4)在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2 , 根据元素守恒可知应还有水生成,该反应的离子方程式为4H++5ClO2﹣=Cl﹣+4ClO2↑+2H2O; 在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是验证是否有ClO2 生成;(5)由图可知,稳定剂Ⅱ可以缓慢释放ClO2 , 能较长时间维持保鲜所需的浓度.
-
科目: 来源: 题型:
查看答案和解析>>【题目】一定温度下,在2.5L的恒容密闭容器中发生如下反应:CO2(g)+H2S(g)
 COS(g)+H2O(g)
COS(g)+H2O(g)实验
温度/K
起始物质的量/mol
平衡物质的量/mol
平衡常数
CO2
H2S
H2O
I
607
0.11
0.41
0.01
II
607
0.22
0.82
III
620
0.1
0.4
6.74×10-3
下列说法不正确的是( )
A. 该反应正反应为吸热反应
B. 607K时,把物质的量均为0.1mol四种反应物加入该反应器中,反应将向正反应方向进行
C. 实验Ⅱ达到平衡时容器中COS的物质的量为0.02mol
D. 实验Ⅲ中,无论是开始还是至化学平衡状态,混合气体的密度始终不变
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质分离(括号内的物质为杂质)的方法错误的是( )
A.硝基苯(苯)--蒸馏
B.乙烯(SO2)--氢氧化钠溶液
C.己烷(己烯)--溴水,分液
D.乙酸乙酯(乙醇)--碳酸钠溶液,分液
-
科目: 来源: 题型:
查看答案和解析>>【题目】亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去):
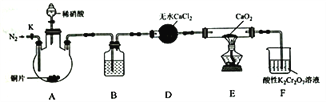
已知:2NO+CaO2 =Ca(NO2)2;2NO2+CaO2=Ca(NO3)2。
请回答下列问题:
(1)将分液漏斗中的稀硝酸滴入三颈烧瓶中的操作为______________。
(2)向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的N2,原因为_________________。
(3)装置D中的仪器名称为_______________。装置B所加试剂为_______________。
(4)装罝F中,酸性K2Cr2O7溶液可将剩余的NO氧化为NO3-,溶液由橙色变为绿色(Cr3+),发生反应的离子方程式为_________________。
(5)已知:Ca(NO2)2溶液遇酸会产生NO气体。设计实验证明装置E中有亚硝酸钙生成:____________。
(6)工业上可用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化空气,又能获得应用广泛的 Ca(NO2)2,反应原理为Ca(OH)2 + NO+NO2=Ca(NO2)2 + H2O。
①若n(NO):n(NO2)>l:l,则会导致______________________________。
②若n(NO):n(NO2)<1:1,则会导致________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】0.1mol金属锡跟100mL12mol/LHNO3共热一段时间,完全反应后放出气体0.4mol,测定溶液c(H+)=8mol/L,溶液体积仍为100mL。由此推断氧化产物可能是
A. Sn(NO3)2 B. Sn(NO3)4
C. SnO24H2O D. Sn(NO3)2和Sn(NO3)4
-
科目: 来源: 题型:
查看答案和解析>>【题目】NA表示阿伏加德罗常数,下列叙述中正确的是( )
A. 常温常压下,48g O3所含的原子数为3NA
B. 1mol NH3所含有的原子数为NA
C. 标准状况下,22.4L水中所含原子数为3 NA
D. 0.1mol/L NaC1溶液中所含Na+数目为0.1 NA
-
科目: 来源: 题型:
查看答案和解析>>【题目】A、B、C、D、E、F属于短周期主族元素.A的原子半径是短周期中最大,B元素的原子最外层电子数为m、次外层电子数为n,C元素的原子L层电子数为m+n,M层电子数为m﹣n,D元素与C元素同主族,E元素原子与B元素原子的核外电子数之比为2:1,F的一种原子中,质量数与质子数之差为零.
(1)B2﹣的离子结构示意图 , DE2的电子式 .
(2)A、B形成的简单离子的半径由大到小的顺序为(用具体符号表示).
(3)A、E形成的是(填共价或离子)化合物
(4)C在周期表中的位置是
(5)由元素C形成的单质Y与由A,B,F三种元素形成的化合物X的水溶液反应的离子方程式为 .
相关试题

