【题目】下列各表述与示意图一致的是( )
A.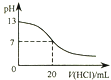
图表示25℃时,用0.1 molL﹣1盐酸滴定20 mL 0.1 molL﹣1 NaOH溶液,溶液的pH随加入酸体积的变化
B.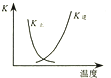
图中曲线表示反应2SO2(g)+O2(g)═2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化
C.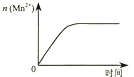
图③表示10 mL 0.01 molL﹣1 KMnO4 酸性溶液与过量的0.1 molL﹣1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.
图中a、b曲线分别表示反应CH2=CH2 (g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化
参考答案:
【答案】B
【解析】A.用盐酸滴定氢氧化钠溶液,当恰好中和时溶液的pH=7,酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,题中图象变化与实际不相符,A不符合题意;
B.因反应为放热反应,则升高温度,平衡逆向移动,平衡后升温K(逆)会增大,而K(正)会减小,且正逆反应的平衡常数互为倒数关系,图象中变化与实际上的变化相符,B符合题意;
C.溶液中离子浓度等因素影响反应速率,随反应进行反应速率变化,Mn2+的物质的量与时间不呈线性关系,C不符合题意;
D.图象a活化能减小,a使用了催化剂,因该反应是放热反应,应反应物的总能量大于生成物的总能量,但图象描述是吸热反应,D不符合题意;
所以答案是:B
-
科目: 来源: 题型:
查看答案和解析>>【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 标准状况下,5.6L.Cl2与足量NaOH反应转移的电子数为0.25NA
B. 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C. 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
D. 5NH4NO3
 2HNO3+4N2↑+9H2O反应中,生成56gN2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成56gN2时,转移的电子数目为3.75NA -
科目: 来源: 题型:
查看答案和解析>>【题目】下列说法不正确的是
A. 反应MgO(s)+C(s)=Mg(s)+CO(g)在室温下不能自发进行,则该反应的△H>0
B. 原电池输出电能的能力取决于组成原电池的反应物的氧化还原能力
C. 0.1 mol·L-1CH3COOH溶液加水稀释后,溶液中
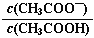 的值减小
的值减小D. 锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去
-
科目: 来源: 题型:
查看答案和解析>>【题目】关于下列粒子的描述不正确的是( )
A. PH3的电子式为
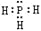 ,其热稳定性不如NH3
,其热稳定性不如NH3B. HS-的电子式为
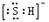 ,是含有极性键的18电子的粒子
,是含有极性键的18电子的粒子C. CH2Cl2的电子式为
 ,是结构呈正四面体的分子
,是结构呈正四面体的分子D. KF的电子式为
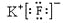 ,它是易溶于水的离子化合物
,它是易溶于水的离子化合物 -
科目: 来源: 题型:
查看答案和解析>>【题目】将面团包在纱布中在清水中搓洗,鉴定黏留在纱布上的黏稠物质和洗出的白浆用的试剂分别是 ( )
A.碘液、苏丹Ⅲ染液 B.双缩脲试剂、碘液
C.斐林试剂、碘液 D.碘液、斐林试剂
-
科目: 来源: 题型:
查看答案和解析>>【题目】将20 mL 0.5 mol/L Al2(SO4)3溶液加水稀释到500 mL,稀释后溶液中SO42﹣浓度为( )
A.0.01 mol/L
B.0.02 mol/L
C.0.03mol/L
D.0.06mol/L -
科目: 来源: 题型:
查看答案和解析>>【题目】占肝细胞干重50%以上的化合物是 ( )
A.蛋白质 B.糖类 C.脂类 D.核酸
相关试题

