【题目】还原沉淀法是处理含铬(含Cr2O72﹣和CrO42﹣)工业废水的常用方法,过程如下:
CrO42﹣ ![]() Cr2O72﹣
Cr2O72﹣ ![]() Cr3+
Cr3+ ![]() Cr(OH)3↓
Cr(OH)3↓
己知转化过程中的反应为:2CrO42﹣(aq)+2H+(aq)═Cr2O72﹣(aq)+H2O(1).转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣ . 下列说法不正确的是( )
A.转化过程中,增大c(H+),平衡向正反应方向移动,CrO42﹣的转化率提高
B.常温下Ksp[Cr(OH)3]=1×10﹣32 , 要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,应调溶液的pH=5
C.若用绿矾(FeSO47H2O)(M=278)作还原剂,处理1L废水,至少需要917.4g
D.常温下转化反应的平衡常数K=104 , 则转化后所得溶液的pH=1
参考答案:
【答案】C
【解析】解:转化后所得溶液中铬元素含量为28.6g/L,则1L废水中n(Cr)= ![]() =0.55mol,
=0.55mol,
A.存在平衡:2CrO42﹣(aq)+2H+(aq)═Cr2O72﹣(aq)+H2O(1),氢离子浓度增大,平衡正向进行,CrO42﹣的转化率提高,故A正确;
B.常温下Ksp[Cr(OH)3]=1×10﹣32 , 要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,则c(Cr3+)×c3(OH﹣)=1×10﹣32 , c(OH﹣)=1×10﹣9mol/L,pH=5,故B正确.
C.若用绿矾(FeSO47H2O)(M=278)作还原剂,处理1L废水,设需要xmolFeSO47H2O,由氧化还原反应中氧化剂和还原剂得失电子数目相等可知0.55×(6﹣3)=x×(3﹣2),x=1.65,m(FeSO47H2O)=1.65mol×278g/mol=458.7g,故C错误;
D.1L废水中n(Cr)= ![]() =0.55mol,CrO42﹣有
=0.55mol,CrO42﹣有 ![]() 转化为Cr2O72﹣ , 则酸化后c(CrO42﹣)=0.55mol/L×(1﹣
转化为Cr2O72﹣ , 则酸化后c(CrO42﹣)=0.55mol/L×(1﹣ ![]() )=0.05mol/L,c(Cr2O72﹣)=0.55mol/L×
)=0.05mol/L,c(Cr2O72﹣)=0.55mol/L× ![]() ×
× ![]() =0.25mol/L,常温下转换反应的平衡常数K=1×104 , 则
=0.25mol/L,常温下转换反应的平衡常数K=1×104 , 则 ![]() =1×104 , c(H+)=0.1mol/L,所以pH=1,故D正确;
=1×104 , c(H+)=0.1mol/L,所以pH=1,故D正确;
故选C.
【考点精析】认真审题,首先需要了解化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)).
-
科目: 来源: 题型:
查看答案和解析>>【题目】黄铜矿不仅可用于火法炼铜,也可用于湿法炼铜,湿法可同时生产铜、磁性氧化铁和用于橡胶工业的一种固体物质A,流程如下:
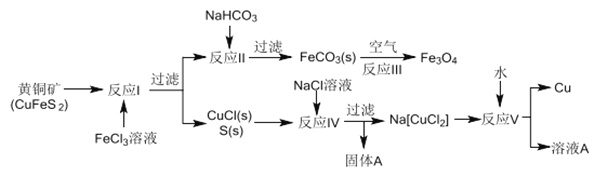
(1)黄铜矿中Cu 的化合价是______,反应I中65gFeC13 可氧化________mol CuFeS2。
(2)工业生产中的过滤操作多采用倾析法分离出固体物质,下列适合用倾析法的有______。
A.沉淀的颗粒较大 B.沉淀容易沉降 C.沉淀呈胶状 D.沉淀呈絮状
(3)在反应Ⅱ中,计算NaHCO3饱和溶液(其中CO32-平衡浓度为1.2×10-3mol/L)可产生FeCO3沉淀时的最小Fe2+浓度是_________(己知FeCO3的Ksp=3.0×10-11)
(4)反应Ⅲ是在设备底部鼓入空气,高温氧化锻烧法来制备磁性氧化铁,写出对应的化学方程式_________________。
(5)固体物质A的成分________(写名称)。
(6)潮湿的FeCO3固体若不及时灼烧处理会在空气中逐渐变红,写出相关的化学方程式:_______________。
(7)本流程中可实现循环使用的物质除了水外,还有_____________
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知2SO2(g)+O2(g)
 2SO3(g) △H=-197kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲)2molSO2和lmolO2;(乙) lmolSO2和0.5molO2;(丙)2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3(g) △H=-197kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲)2molSO2和lmolO2;(乙) lmolSO2和0.5molO2;(丙)2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是A. 容器内压强P:P甲=P丙>2P乙
B. SO3的质量m:m甲=m丙>2m乙
C. c(SO2)与c(O2)之比 k:k甲=k丙>k乙
D. 反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙
-
科目: 来源: 题型:
查看答案和解析>>【题目】工业上用铋酸钠(NaBiNO3)检验溶液中的Mn2+,反应方程式为:4MnSO4+10NaBiO3+14H2SO4═4NaMnO4+5Bi2(SO4)3+3Na2SO4+口,下列说法不正确的是
A. 口内的物质为水,配平系数为14。
B. 若生成1mol NaMnO4,则转移5mole-
C. 反应方程式中的硫酸可换为盐酸
D. 溶液中有Mn2+的现象是溶液变为紫红色
-
科目: 来源: 题型:
查看答案和解析>>【题目】我国古代就有湿法炼铜的记载“曾青得铁则化为铜”,反应为Fe+CuSO4==FeSO4+Cu。有关该反应的说法正确的是 ( )
A. Fe是氧化剂 B. CuSO4是还原剂
C. Fe被氧化 D. CuSO4发生氧化反应
-
科目: 来源: 题型:
查看答案和解析>>【题目】现有短周期元素R、X、Y、Z、T,R与T原子最外层电子数均是电子层数的2倍,Y元素能与大多数金属和非金属元素形成化合物;Z+与Y2-电子层结构相同。五种元素的原子半径如图所示,下列推断正确的是

A. Y、Z组成的化合物只含离子键
B. 氢化物的沸点:R<X<Y
C. T的最高价氧化物的水化物酸性比R的强
D. Y和Z分别与T、X组成的二元化合物的水溶液一定呈中性
-
科目: 来源: 题型:
查看答案和解析>>【题目】温室下,用0.1molL﹣1NaOH溶液分别滴定体积均为20ml浓度均为0.1molL﹣1HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化图,下列说法不正确的是( )
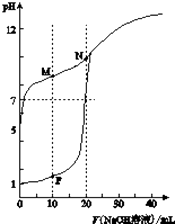
A.HX为弱酸
B.M点c(HX)﹣c(X﹣)>c(OH﹣)﹣c(H+)
C.将P点和N点的溶液为混合,呈酸性
D.向N点溶液中通入HCl至pH=7:c(Na+)>c(HX)=c(Cl﹣)>c(X﹣)
相关试题

