【题目】某溶液中可能含有K+、Na+、Fe2+、Fe3+、SO42﹣、CO32﹣、I﹣、Cl﹣中的一种或多种,进行如图所示的实验,下列说法正确的是( )
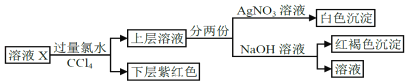
A. “下层紫红色”为I2的CCl4溶液,可用分液方法分离
B. 溶液X中有Fe2+、I﹣,可能有SO42﹣、Cl﹣、K+、Na+
C. 溶液X中一定有I﹣、Cl﹣
D. 溶液X中有I﹣,Fe2+和Fe3+两种离子中至少有一种
参考答案:
【答案】B
【解析】
由上述分析可知,原溶液X中一定含有I﹣、Fe2+,一定不存在Fe3+、CO32﹣,不能确定是否存在K+、Na+、SO42﹣、Cl﹣。
A.加入CCl4萃取后下层的紫红色为I2的CCl4溶液,互溶,不能用分液方法分离,可用蒸馏方法分离,选项A错误;
B.由分析可知:溶液X中有Fe2+、I﹣,可能有K+、Na+、SO42﹣、Cl﹣,选项B正确;
C.不能确定是否存在Cl﹣,选项C错误;
D.X中不可能含Fe3+,选项D错误;
答案选:B。
-
科目: 来源: 题型:
查看答案和解析>>【题目】用NA代表阿伏加德罗常数,下列说法中正确的是( )
A.18g水中含有的氢原子数目为NA
B.1 mol氩气分子所含的原子数目为2NA
C.106g碳酸钠中含有的钠离子为2NA
D.含0.5 mol HNO3的硝酸溶液中含有的氧原子为1.5 NA
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列离子方程式的书写及评价,均合理的是
选项
离子方程式
评价
A
用铜电极电解饱和KCl溶液:2H2O+2Cl-
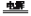 H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-正确:Cl-的失电子能力比OH-强
B
向CuSO4溶液中通入过量的H2S气体:Cu2++H2S=CuS↓+2H+
错误:H2S的酸性比H2SO4弱
C
Ba(HCO3)2溶液与足量的NaOH溶液反应:Ba2++HCO3- +OH- ═BaCO3↓+H2O
错误:Ba2+与HCO3-系数比应为1:2
D
过量SO2通入到NaClO溶液中:SO2+ClO- +H2O= HClO+HSO3-
正确:H2SO3的酸性比HClO强
A.AB.BC.CD.D
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是H2 和Cl2 反应生成HCl的能量变化示意图,由图可知( )
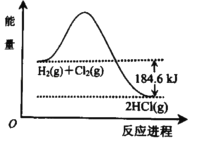
A. 反应物的能量总和小于生成物的能量
B. 生成1molHCl(g)需吸收92.3kJ的能量
C. H2(g)+Cl2(g)=2HCl(g)△H=﹣184.6 kJmol﹣1
D. H2(g)+Cl2(g)=2HCl(g)△H=﹣184.6 kJ
-
科目: 来源: 题型:
查看答案和解析>>【题目】按要求填空
(1)天然气的主要成分是_____(写化学式),其分子空间构型是_____;
(2)苯与液溴在铁粉为催化剂时发生反应的化学方程式_____;反应类型为_____;
(3)写出Na与水反应的离子方程式_____;
(4)CH2=CH﹣CH=CH2与H2在一定条件下发生1,4﹣加成反应的化学方程式_____;
(5)萘的结构简式是
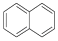 ,其分子式_____;一氯代物有_____种。
,其分子式_____;一氯代物有_____种。(6)某摩尔质量为42gmol﹣1的链烃A可使溴水褪色,A的结构简式为_____;A在一定条件下可以发生加聚反应,产物的结构简式为_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A是一种重要的化工原料,部分性质及转化关系如图:
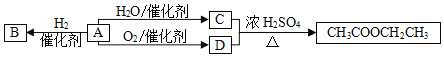
请回答:
(1)D中官能团的名称是_____。
(2)A→B的反应类型是_____。
A.取代反应B.加成反应C.氧化反应
(3)写出A→C反应的化学方程式_____。
(4)下列说法不正确的是_____。
A.B物质不能使溴水和酸性高锰酸钾褪色
B.A在一定条件下可与氯化氢发生加成反应
C.有机物C、D可用金属钠鉴别
D.A分子所有原子在同一个平面内
-
科目: 来源: 题型:
查看答案和解析>>【题目】现有NaCl、Na2SO4和NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现氯离子(Cl-)、硫酸根离子(SO42-)和硝酸根离子(NO3-)的相互分离,实验过程如下:
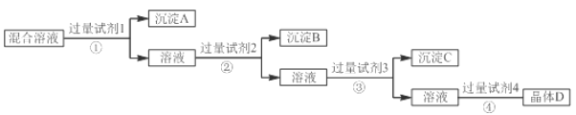
试剂3:Na2CO3;试剂4:硝酸
请回答下列问题:
(1)写出试剂②的名称______________。
(2)写出过量Na2CO3的目的是___________________________________________________。
(3)写出混合溶液D与过量硝酸反应的化学方程式:________________________________。
(4)写出操作④的名称______________。
相关试题

