2025年优化探究同步导学案高中化学选择性必修2人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年优化探究同步导学案高中化学选择性必修2人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
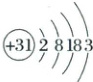
镓元素的原子结构示意图如图所示。
(+31)2 8 18 3
(1)该元素的原子 $n = 3$ 的电子层上有
(2)该元素的原子 $n = 4$ 的电子层上有
(3)若电子在进入原子轨道时优先进入能量低的原子轨道,然后进入能量高的原子轨道,且每个原子轨道上最多容纳 2 个电子,那么在 $n = 4$ 的电子层上 4p 轨道上的电子为

(+31)2 8 18 3
(1)该元素的原子 $n = 3$ 的电子层上有
3
个能级,这些能级的能量由高到低的顺序是3d、3p、3s
,该元素原子核外每一电子层上的 s 轨道的能量由高到低的顺序是4s、3s、2s、1s
。(2)该元素的原子 $n = 4$ 的电子层上有
4
个能级,16
个原子轨道。(3)若电子在进入原子轨道时优先进入能量低的原子轨道,然后进入能量高的原子轨道,且每个原子轨道上最多容纳 2 个电子,那么在 $n = 4$ 的电子层上 4p 轨道上的电子为
1
个。
答案:
提示:
(1)3 3d、3p、3s 4s、3s、2s、1s
(2)4 16
(3)1
(1)3 3d、3p、3s 4s、3s、2s、1s
(2)4 16
(3)1
1.下列有关电子层和能级的叙述正确的是 (
A.M 电子层有 s、p 共 2 个能级,最多容纳 8 个电子
B.3d 能级最多容纳 5 个电子,3f 能级最多容纳 7个电子
C.无论哪一电子层的 s 能级最多容纳的电子数均为 2
D.任一电子层都有 s、p 能级,但不一定有 d 能级
C
)A.M 电子层有 s、p 共 2 个能级,最多容纳 8 个电子
B.3d 能级最多容纳 5 个电子,3f 能级最多容纳 7个电子
C.无论哪一电子层的 s 能级最多容纳的电子数均为 2
D.任一电子层都有 s、p 能级,但不一定有 d 能级
答案:
1.C A项,M电子层有s、p、d共3个能级,最多容纳18个电子; B项,3d能级最多容纳10个电子,从N电子层开始有f能级,最多 容纳14个电子,不存在3f能级;C项,每个电子层都从s能级开始, 且s能级最多容纳2个电子;D项,K电子层只有s能级,不含有p 能级。
2.下列有关认识正确的是 (
A.各电子层的原子轨道数按 s、p、d 的顺序分别为 1、3、5
B.各电子层的能级都是从 s 能级开始至 f 能级结束
C.各电子层含有的能级数为 $n - 1$
D.各电子层含有的原子轨道数为 $2n^2$
A
)A.各电子层的原子轨道数按 s、p、d 的顺序分别为 1、3、5
B.各电子层的能级都是从 s 能级开始至 f 能级结束
C.各电子层含有的能级数为 $n - 1$
D.各电子层含有的原子轨道数为 $2n^2$
答案:
2.A 各能级的原子轨道数目取决于原子轨道在三维空间的分布情 况,s能级有1个原子轨道,p能级有3个原子轨道,d能级有5个原 子轨道,A项正确;各电子层的能级都是从s能级开始,但能级数等 于电子层数,不一定到f能级结束,故B、C两项错误;各电子层含有 的原子轨道数为$n^{2}$,D项错误。
1. 原子轨道的图形描述
原子中单个电子的

特别提醒 s 轨道为球形,p 轨道为“$\infty$”形,并不是说 s 轨道上的电子绕核做圆周运动,p 轨道上的电子绕核做“$\infty$”形运动。
原子中单个电子的
空间运动状态
用原子轨道来描述,而原子轨道在量子力学中用波函数
来表示,并可以将其以图形的方式在直角坐标系中呈现出来。如图给出了 1s 和 2p 原子轨道示意图。从图中可以看出,s 轨道在三维空间分布的图形为球形,即该原子轨道具有球对称性;p 轨道在三维空间分布的图形与 s 轨道明显不同,它的空间分布特点是分别相对于 $x、y、z$ 轴对称,也就是说,p 轨道在空间分别沿 $x、y、z$ 轴的方向分布。
特别提醒 s 轨道为球形,p 轨道为“$\infty$”形,并不是说 s 轨道上的电子绕核做圆周运动,p 轨道上的电子绕核做“$\infty$”形运动。
答案:
1.空间运动状态 波函数
2. 电子在核外的空间分布
人们能通过对
处于 1s 轨道上的电子(通常也称 1s 电子)的概率分布呈
人们能通过对
波函数
进行数学处理计算出电子在什么地方出现的概率大、在什么地方出现的概率小。通常用单位体积内小点的疏密程度
来表示电子在原子核外某处单位体积内出现概率
的大小:点密集的地方,表示电子在此处单位体积内出现的概率大
;点稀疏的地方,表示电子在此处单位体积内出现的概率小。这种形象地描述电子在核外空间某处单位体积内的概率分布的图形称为电子云图
。处于 1s 轨道上的电子(通常也称 1s 电子)的概率分布呈
球形
对称,而且电子在原子核附近单位体积内出现的概率大,离核越远,单位体积内电子出现的概率越小。2p 电子云具有一定的空间取向
。
答案:
2.波函数 单位体积内小点的疏密程度 概率 大 电子云图 球形 空间取向
1.钠原子的 1s、2s、3s 电子云半径相同。 (
2.$1s、2p_x、2p_y、2p_z$ 轨道都具有球对称性。 (
3.s 电子绕核旋转,其轨道为一圆圈。 (
4.电子云是用小点的疏密程度来表示电子在核外空间某处单位体积内的概率分布的图形。 (
×
)2.$1s、2p_x、2p_y、2p_z$ 轨道都具有球对称性。 (
×
)3.s 电子绕核旋转,其轨道为一圆圈。 (
×
)4.电子云是用小点的疏密程度来表示电子在核外空间某处单位体积内的概率分布的图形。 (
√
)
答案:
1.× 2.× 3.× 4.√
回答下列问题:
(1)可正确表示原子轨道的是
A.2s
B.2d
C.3p
D.3f
(1)可正确表示原子轨道的是
AC
(填字母)。A.2s
B.2d
C.3p
D.3f
答案:
提示:
(1)AC
(1)AC
查看更多完整答案,请扫码查看


