【题目】归纳与演绎是重要的科学方法,也常用于化学的学习.请根据下列实验装置,回答问题:

(1)我们已经学过实验室制取氧气、二氧化碳两种气体的反应原理、制取与收集方法,请你归纳出实验室制取这两种气体反应的共同点____(填序号).
A.需要加热 B.需用催化剂 C.没有气体参加反应 D.生成的气体只有一种
(2)用高锰酸钾制取氧气可选用发生装置是____(填序号),反应的方程式____;
(3)装置B中反应的方程式为____;要随时使反应停止或发生可选择的发生装置有__(填序号,从A-E中选择);若用E和G组装一套气密性好的装置来测定二氧化碳的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏小得多,原因是____.
(4)化学上可通过多种反应得到氨气(极易溶于水,密度比空气小),例如:
①氯化铵(固)+氢氧化钙(固)![]() 氯化钙+氨气+水
氯化钙+氨气+水
②碳酸氢铵(固)![]() 氨气+二氧化碳+水
氨气+二氧化碳+水
结合以上实验装置完成下列填空(以下均填序号):你选择上述反应____作为实验室制取氨气的反应原理,选用上图中A~H的____作为反应的发生装置,采用的收集装置是F和H,其中氨气应从____管导入(填“a”或“b”)F中,H中用倒置漏斗比直接用导管通入水中吸收氨气的优点是____,实验室中漏斗的其它用途____(写一种)
参考答案:
【答案】 CD A 2KMnO4 ![]() K2MnO4+MnO2+O2↑ CaCO3+2HCl==CaCl2+H2O+CO2↑ BE 二氧化碳可溶于水 ① A b 防止倒吸或增大接触面积 向小口容器中添加液体或过滤.
K2MnO4+MnO2+O2↑ CaCO3+2HCl==CaCl2+H2O+CO2↑ BE 二氧化碳可溶于水 ① A b 防止倒吸或增大接触面积 向小口容器中添加液体或过滤.
【解析】根据所学知识和题中信息知,(1)根据实验室制取氧气、二氧化碳两种气体的反应原理、制取与收集方法,归纳出实验室制取这两种气体反应的共同点C.没有气体参加反应 ,D.生成的气体只有一种。(2)用高锰酸钾制取氧气可选用发生装置是A;反应的方程式是2KMnO4 ![]() K2MnO4+MnO2+O2↑。(3)装置B中反应的方程式为 CaCO3+ 2HCl==CaCl2+H2O+CO2↑。要随时使反应停止或发生可选择的发生装置有BE;若用E和G组装一套气密性好的装置来测定二氧化碳的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏小得多,原因是二氧化碳可溶于水;(4)化学上可通过多种反应得到氨气(极易溶于水,密度比空气小)。结合以上实验装置,选择上述反应①作为实验室制取氨气的反应原理,选用上图中A~H的A作为反应的发生装置,采用的收集装置是F和H,其中氨气应从b管导入F中,H中用倒置漏斗比直接用导管通入水中吸收氨气的优点是防止倒吸或增大接触面积,实验室中漏斗的其它用途是向小口容器中添加液体或过滤。
K2MnO4+MnO2+O2↑。(3)装置B中反应的方程式为 CaCO3+ 2HCl==CaCl2+H2O+CO2↑。要随时使反应停止或发生可选择的发生装置有BE;若用E和G组装一套气密性好的装置来测定二氧化碳的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏小得多,原因是二氧化碳可溶于水;(4)化学上可通过多种反应得到氨气(极易溶于水,密度比空气小)。结合以上实验装置,选择上述反应①作为实验室制取氨气的反应原理,选用上图中A~H的A作为反应的发生装置,采用的收集装置是F和H,其中氨气应从b管导入F中,H中用倒置漏斗比直接用导管通入水中吸收氨气的优点是防止倒吸或增大接触面积,实验室中漏斗的其它用途是向小口容器中添加液体或过滤。
点睛∶本题主要考查实验室制取氧气,二氧化碳装置,原理,收集方法等知识。
-
科目: 来源: 题型:
查看答案和解析>>【题目】扑灭图书档案、贵重设备、精密仪器等火灾,不会留下任何痕迹而使物品损坏,最适宜的灭火器具有( )
A.高压水枪 B.液态二氧化碳灭火器 C.干粉灭火器 D.泡沫灭火器
-
科目: 来源: 题型:
查看答案和解析>>【题目】某气体既能用排水法收集,又能用向上排空气法收集,该气体具有的物理性质是( )
A.难溶于水,密度比空气大 B.难溶于水,密度比空气小
C.易溶于水,密度比空气大 D.易溶于水,密度比空气小
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列化学用语与含义相符的是( )
A. 3Al3+—— 三个铝离子带3个单位的正电荷 B. 2H2——两个氢气分子
C. 2H ——2个氢元素 D. S2-——硫元素的化合价为-2价
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知A—G均为初中化学常见的物质.其中A、B的组成元素相同,D是形成温室效应的主要原因,F中含有三种元素,E和G只有阳离子不同.根据图中所示的转化关系(图中“—”表示相互间能反应,“→”表示在一定条件下能生成该物质,部分生成物、反应条件均已略去),请回答:

(1)C的化学式____、E中的阴离子符号是____、F的俗名为____;
(2)反应①是自然界最常见的反应,我们称之为____;反应②的化学方程式是____;反应③的化学方程式是____,该反应的基本类型是____反应.
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组围绕“酸碱中和反应”,在老师引导下开展探究活动.
探究:证明氢氧化钠溶液与稀盐酸确实能发生反应.
【方案1】测定稀盐酸与NaOH溶液混合前后的pH.
测定某NaOH溶液的pH,pH大于7.将一定量的稀盐酸加入该NaOH溶液中,混合均匀后测定其pH,发现pH减小了,但仍然大于7,小组中有的同学认为根据这个测定结果不可以认为稀盐酸与NaOH溶液发生了反应,你认为他的理由____.经过讨论后,他们向溶液中又加入一定量的稀盐酸,混合均匀后测定其pH,pH小于7.
结论:稀盐酸与氢氧化钠溶液发生了化学反应,并且稀盐酸过量.
【方案2】借助于无色酚酞试液.
【药品仪器】
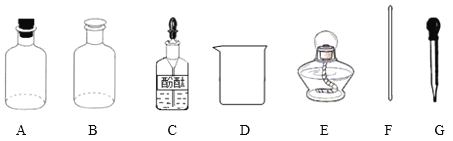
①取____(选填“A”或“B”)中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色;
②用胶头滴管向①中溶液滴加稀盐酸,红色消失;
③用F蘸取②中溶液,在酒精灯上灼烧,有白色固体产生.
【思考拓展】
(1)如不使用酸碱指示剂,进一步确认步骤③中的白色固体不是氢氧化钠的方法是:____;
(2)探究步骤②中无色溶液中稀盐酸是否过量.
根据上述反应过程中溶液变成无色,不能确定稀盐酸是否过量,兴趣小组同学又分别选取了AgNO3溶液、紫色石蕊试液、铁锈粉末设计实验方案,请你分析并判断:
实验方案
实验步骤
现象
结论
①
取样,加入适量的AgNO3溶液
出现白色沉淀
稀盐酸过量
②
取样,加入几滴紫色石蕊试液
溶液变红
稀盐酸过量
③
取样,加入铁锈粉末
稀盐酸过量
方案③中反应的化学方程式____.上述设计方案中,不正确的是____(填“①”、“②”或“③”),错误的原因是____;
(3)碱与酸反应不一定都无明显现象,写出一个有沉淀生成的中和反应:____.
-
科目: 来源: 题型:
查看答案和解析>>【题目】某样品硫酸钠中含有氯化钠杂质.学校化学兴趣小组的同学开展了测定其中硫酸钠质量分数的探究实验.他们设计了如下的实验方案:

(1)过滤中使用到玻璃棒的作用是 ;
(2)沉淀应该洗涤后烘干称量,否则会使测定的结果 (填“偏大”或“偏小”或“不变”);
(3)为了检验沉淀是否洗涤干净,可取最后一次洗涤后的液体少量于试管中,再滴加 溶液,无明显现象则说明沉淀已洗涤干净;
(4)该样品中硫酸钠的质量分数是多少?(写出解题过程)
相关试题

