【题目】实验小组对久置生石灰的成分进行分析,实验操作及部分现象如下图所示。
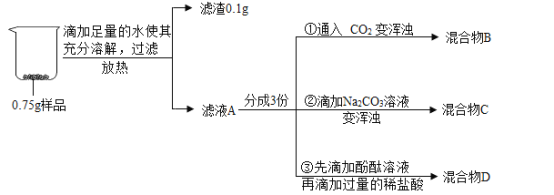
回答下列问题:
(1)样品加水放热的原因是_____(化学方程式表示)。
(2)②中反应的化学方程式是_____。
(3)③中的实验现象是_____。
(4)将混合物B、C、D倒入一个洁净的烧杯中,发现烧杯中有白色沉淀且上层清液呈红色,过滤,得滤液E和1g滤渣。向滤液E中滴加![]() 溶液,有白色沉淀生成,依据实验现象及数据判断,原样品的成分是_____。
溶液,有白色沉淀生成,依据实验现象及数据判断,原样品的成分是_____。
参考答案:
【答案】CaO+H2O=Ca(OH)2 Na2CO3+Ca(OH)2=2NaOH+CaCO3↓ 滴加无色酚酞溶液,溶液由无色变成红色;再滴加过量稀盐酸,溶液由红色变成无色 氧化钙、氢氧化钙、碳酸钙[CaO、Ca(OH)2、CaCO3]
【解析】
(1)氧化钙和水反应生成氢氧化钙,同时放出大量的热,化学方程式为CaO+H2O=Ca(OH)2;
(2)②根据题意“加足量水充分溶解过滤”,可知在滤液中只有氢氧化钙能够溶于水,那么滤渣是碳酸钙,滤液中含有的氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(3)③滤液中含有氢氧化钙,溶液显碱性,能使无色酚酞溶液由无色变成红色,再滴加过量的稀盐酸,稀盐酸和氢氧化钙反应生成中性的氯化钙和水,当氢氧化钙被完全消耗时,由于酸过量,溶液呈酸性,则溶液由红色变成无色;
(4)由①向滤液中通入适量二氧化碳若观察到滤液变浑浊,说明氢氧化钙和二氧化碳反应生成碳酸钙,混合物B中含有碳酸钙,可能还有氢氧化钙;由②知,滴加碳酸钠可以生成碳酸钙沉淀和氢氧化钠,则C中一定有碳酸钙沉淀和氢氧化钠,可能有氢氧化钙或碳酸钠,由③知,滴加无色酚酞溶液,再加过量的稀盐酸,则D中含有氯化钙和剩余的氯化氢,将混合物B、C、D倒入一个洁净的烧杯中,发现烧杯中有白色沉淀且上层清液呈红色,说明溶液显碱性,溶质可能是氢氧化钠、氢氧化钙,向滤液E中滴加CaCl2溶有液,有白色沉淀生成,说明溶液中有碳酸钠,有碳酸钠就没有氢氧化钙,由此可知滤液E中的溶质可能是NaCl、Na2CO3或NaCl、Na2CO3、NaOH;同时可知1g滤渣是由氢氧化钙反应生成的,设氢氧化钙的质量是x,则根据反应前后钙原子个数守恒可得:
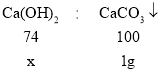
![]()
x=0.74g
0.75g样品中含有0.1g不溶于水的碳酸钙,得到的滤液中含有氢氧化钙0.74g,而样品溶于水时有热量放出,则样品中一定含有氧化钙,如果0.74g全部是氧化钙,则对应得到的氢氧化钙的质量一定大于0.74g,所以样品中一定含有氧化钙、氢氧化钙和碳酸钙。
-
科目: 来源: 题型:
查看答案和解析>>【题目】我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献,工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质,现称取只含氯化钠杂质的纯碱样品11g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液的质量为121g。
试求:(1)该纯碱样品的纯度(计算结果精确到0.1%)
(2)所得溶液中溶质的质量分数。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在下图所示的转化关系中,
 等都是初中化学学过的物质,其中
等都是初中化学学过的物质,其中 是单质,
是单质,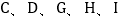 是化合物。
是化合物。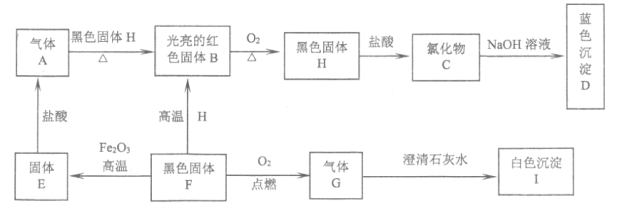
(1)写出
 的化学式:A_____F_____。
的化学式:A_____F_____。(2)根据上述转化关系,写出有关反应的化学方程式。
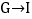 :_____;
:_____;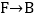 :_____。
:_____。 -
科目: 来源: 题型:
查看答案和解析>>【题目】水、溶液与人们的生产生活密切相关请回答:
(1)如图所示电解水的实验中,试管a、b中产生气体的体积比约为_____,该实验证明水是由_____组成的。
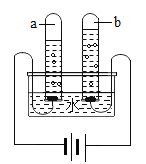
(2)下列净化水的单一操作中,相对净化程度较高的是_____(填字母)。
A 静置沉淀 B 吸附沉淀 C 过滤 D 蒸馏
(3)测定某地下水的酸碱度,最简单的方法是使用_____。
(4)下图是三种固体物质的溶解度曲线。根据溶解度曲线回答问题:
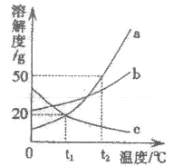
①物质c的溶解度随温度的升高而_____;
②物质a的溶解度大于物质c的溶解度的温度范围_____;
③
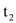 ℃时,用50g水配制物质a的饱和溶液,至少需要a物质_____g;
℃时,用50g水配制物质a的饱和溶液,至少需要a物质_____g;④将
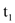 ℃时
℃时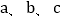 三种物质的饱和溶液升温至
三种物质的饱和溶液升温至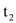 ℃(溶剂量不变),溶液中溶质质量分数不变的是_____。
℃(溶剂量不变),溶液中溶质质量分数不变的是_____。 -
科目: 来源: 题型:
查看答案和解析>>【题目】金属及金属材料在日常生活中应用广泛。
(1)铝块能制成铝箔是利用了铝的_____性(填“导电”或“延展”)。
(2)X,Y,Z三种常见金属及其盐溶液存在以下反应,则三种金属的活动性顺序正确是_____(填字母)。
①
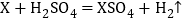 ②
②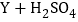 不发生反应③
不发生反应③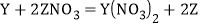 .
.A
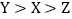 B
B 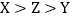 C
C 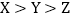 D
D 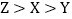
(3)金属钛(Ti)不仅能在空气中燃烧,也能在二氧化碳或氮气中燃烧.在稀有气体和高温条件下,用四氯化钛和镁发生置换反应可制备金属钛。请写出四氯化钛制备金属钛的化学方程式是_____。
(4)“辽宁号”航母的服役举世瞩目。钢铁是制造航母的主要材料,它很容易与空气中的_____等发生反应而锈蚀。用稀盐酸除铁锈的化学方程式是_____。
(5)某钢铁厂每天需消耗4900t含
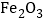 76%的赤铁矿石,该厂理论上可日产含
76%的赤铁矿石,该厂理论上可日产含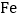 98%的生铁的质量是_____t。
98%的生铁的质量是_____t。(6)将一定量的锌粉放入稀盐酸、氯化亚铁、氯化铜的混合溶液中,充分反应后过滤,再向滤渣中加盐酸有气泡产生,则滤渣中一定含有的固体是_____(写化学式);滤液中一定不含的物质是_____(写化学式)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在物质混合、反应等过程中,存在着“1+1≠2”的有趣现象,通常情况下,下列选项符合“1+1=2”的是( )
A. 1mL酒精与1mL水混合后的总体积
B. 1g碳和1g氧气反应后生成物的质量
C. 1g氢氧化钠溶液和1g硫酸溶液混合后溶液的质量
D. 1g氯化钠饱和溶液中加入1g氯化钠固体后所得溶液的质量
-
科目: 来源: 题型:
查看答案和解析>>【题目】溶液的组成变化与浓溶液和稀溶液有着密切的关系。下列有关溶液浓、稀的说法正确的是( )
①溶质质量增大,溶剂质量不变,则溶液质量增大,溶液会变浓。
②溶质质量减小,溶剂质量不变,则溶液质量减小,溶液会变稀。
③溶质质量不变,溶剂质量增大,则溶液质量增大,溶液会变稀。
④溶质质量不变,溶剂质量减小,则溶液质量减小,溶液会变浓。
A. ①②③④ B. ①②③ C. ②③④ D. ①③④
相关试题

