【题目】我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献,工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质,现称取只含氯化钠杂质的纯碱样品11g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液的质量为121g。
试求:(1)该纯碱样品的纯度(计算结果精确到0.1%)
(2)所得溶液中溶质的质量分数。
参考答案:
【答案】(1)96.4%;(2)l0%
【解析】纯碱中碳酸钠与稀盐酸反应放出二氧化碳,根据质量守恒定律,利用反应前后物质总质量差即反应放出二氧化碳的质量;根据反应的化学方程式,计算出纯碱中碳酸钠的质量和反应后溶液中溶质氯化钠的质量。
解:反应放出的CO2的质量为:64.4g+50g+11g-121g=4.4g
设参加反应的Na2CO3质量为x,生成的NaCl的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
xy4.4g
![]()
解之得 x=10.6g
y=11.7g
(1)碳酸钠纯度=![]() ≈96.4%;
≈96.4%;
(2)纯碱样品中NaCl的质量=11g-10.6g=0.4g
反应后溶液中NaCl的质量为=11.7g+0.4g=12.1g
反应后溶液中NaCl的质量分数=![]() ×100%=10%
×100%=10%
答:(1)该纯碱样品的纯度约为96.4%;(2)所得溶液中溶质的质量分数为10%。
-
科目: 来源: 题型:
查看答案和解析>>【题目】学校禁止吸烟,是因为燃着的香烟产生的烟气有害学生健康,其中含有一种能与血液中血红蛋白结合的有毒气体,它是
A.CO2 B.CO C.N2 D.SO2
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列变化中,属于物理变化的是
A. 煤气燃烧 B. 钢铁生锈 C. 葡萄酿酒 D. 酒精挥发
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学兴趣小组用以下装置探究炼铁的原理。
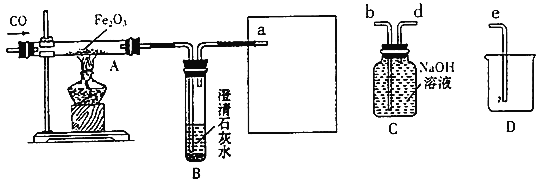
(1)加热Fe2O3之前要先通一会儿CO,目的是____________________________。
(2)方框中连接的是C和D,导管接口的连接顺序为a→(______)→(______)→(______),如果导管连接错误,后果是__________________________________。
(3)玻璃管A中发生反应的化学方程式为_______________________,用这种方法“炼”得的铁与工业上炼出的生铁在组成上的最大区别是______________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组用化学方法测定一种钢样品中铁的含量。同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中。在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如下表:

(1)反应中产生氢气_________克,这种钢样品中铁的含量是多少?(精确到0.1%) ______
(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;0.6%~2%为高碳钢。假设残留在烧杯中的黑色固体全部是炭,则这种钢属于________。
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻。可是他们将一定量的钢样品灼烧后,发现质量反而增加了很多。原因是__________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】联合国教科文组织认为中国铁锅是有推广价值的一种烹饪工具。因为使用铁锅在一定程度上可预防
A.贫血 B.甲状腺肿大 C.龋齿 D.佝偻病
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列鉴别物质的方法中,不可行的是
A. 用闻气味的方法鉴别白酒和食醋
B. 用酚酞溶液鉴别稀硫酸和Na2SO4溶液
C. 用点燃的方法鉴别羊毛和涤纶
D. 用蒸馏水鉴别NaCl和CaCO3固体
相关试题

