【题目】下图是实验室制取气体的仪器,按要求回答问题:
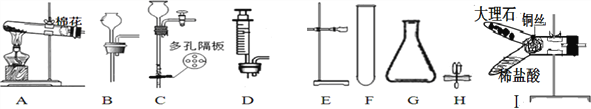
(1)仪器G的名称是________ , 可用于加热固体制取O2的发生装置为______(填字母),该装置中发生反应的化学方程式为 _________________.
(2)若用37.5%的过氧化氢溶液制取O2,最好选用DG组合成发生装置,理由是_________,若要将上述溶液稀释成60g、5%的溶液,则需要原溶液的质量为_______g.
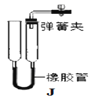
(3)下图J装置可用于实验室制取CO2,检验该装置气密性的方法:从长玻璃管口加入一定量的水,然后用弹簧夹夹紧胶皮管,将左侧长玻璃管向上提起一段后静置,若观察到______________,则气密性良好。该装置在操作上具有的优点是_________________,若从B~H中选择 __________(填字母)进行组合,也能具有同样的优点。
(4)上图I装置的Y型试管内装有制取CO2的药品, 反应的化学方程式为________, 可通过______________________的操作来制得CO2,该装置______(填“有”或“没有”)J装置的操作优点。
参考答案:
【答案】 锥形瓶 A 2KMnO4 △ K2MnO4 + MnO2 + O2↑ 可以控制反应速率 8 左侧水柱不下降(或液面左高右低或出现高度差) 可控制反应发生和停止 CEF(或CF) CaCO3+2HCl==CaCl2+H2O+CO2↑ 旋转Y型试管 有
【解析】本题考查装置的选择、化学方程式的书写,溶液的稀释,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、密度、能否和空气中的物质发生化学反应等因素。
(1)仪器G的名称是锥形瓶; 可用于加热固体制取O2的发生装置为A,A装置中试管口有一团棉花,说明是用高锰酸钾加热制氧气,高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO4 △ K2MnO4 + MnO2 + O2↑;
(2)D中注射器能控制液体的滴加速率,能控制反应的速率。若用37.5%的过氧化氢溶液制取O2,最好选用DG组合成发生装置,理由是可以控制反应速率;设:需要原溶液的质量为x,溶液在稀释前后溶质的质量保持不变,则有:x×37.5%=60g×5% ,x=8g,所以将上述溶液稀释成60g、5%的溶液,则需要原溶液的质量为8g;
(3) J装置可用于实验室制取CO2,检验该装置气密性的方法:从长玻璃管口加入一定量的水,然后用弹簧夹夹紧胶皮管,将左侧长玻璃管向上提起一段后静置,若观察到左侧水柱不下降(或液面左高右低或高度差),则气密性良好。该装置通过弹簧夹的关或开能控制液体和固体的接触或分离,控制反应的发生和停止,所以该装置在操作上具有的优点是可控制反应发生和停止,若从B~H中选择CEF(或CF)进行组合,也能具有同样的优点;
(4) 碳酸钙与盐酸反应生成氯化钙、水和二氧化碳, 反应的化学方程式为CaCO3+2HCl==CaCl2+H2O+CO2↑,旋转Y型试管可使大理石与盐酸接触或脱离控制反应的发生和停止,所以可通过旋转Y型试管的操作来制得CO2,该装置有J装置的操作优点。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下图回答问题

(1)小孩血铅超标中的“铅”指的是______(填原子、元素或单质),有人认为图一中小孩的疑虑是没有必要的,你的解释是 ____________________
(2)观察图二火灾场景,提出一条合理的逃生建议 ___________________.
(3)图三净水器宣称“净化的水不会再产生水垢”,该广告是否科学并做简要分析____________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A-G是初中化学常见的物质,由氢、碳、氧、钙、铁中的一种或几种组成。已知A是一种红色固体,C是常见的金属,D有助燃性,A、B、E、F都是氧化物,G是含钙的化合物,物质之间的相互反应及转化关系如图所示,图中“→”表示转化关系,“ — ”表示能相互反应。 (部分反应物、生成物或反应条件已略去)。
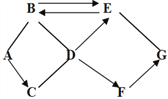
请回答下列问题
(1)分别写出物质E、G的化学式: _______ ________.
(2)写出C、D发生剧烈氧化时的现象 __________________
(3)写出A-B发生反应的化学方程式_________________________________
(4) 物质F可以是__________,也可以是 __________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室中有一桶含Fe2(SO4)3、FeSO4、CuSO4和H2SO4的废液。他们想从中回收铜并制取“还原铁粉” ,主要步骤如图所示。
查阅资料:Fe2(SO4)3 + Fe=3FeSO4 ,FeCO3
 FeO+CO2↑
FeO+CO2↑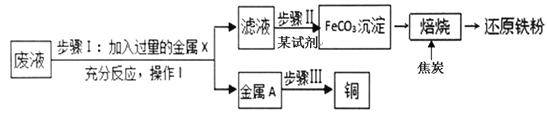
(1)金属X为_______,步骤I加入过量的金属X后发生了________个化学反应。
(2)金属A中的成分有______,步骤III可采用最简单的方法为 _____________________ 。
(3)在此流程中一定需要用到过滤操作的步骤是 ___________(填Ⅰ~Ⅲ)。
(4)FeCO3沉淀隔绝空气进行“焙烧”后,加入焦炭才能制得铁粉,写出加入焦炭后发生反应的化学方程式________________________________ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学进行下图实验,充分反应后,将试管①②内的物质倒入同一烧杯中混合,再次充分反应后过滤,结果得到滤渣A和无色滤液B。
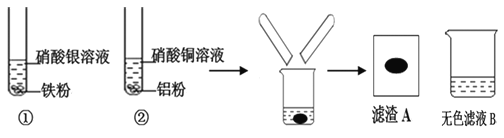
(1)试管①中反应的化学方程式为:_____________________ 。试管②中观察到的现象是:有红色固体析出,溶液________________。
(2)无色滤液B中含有的溶质为___________填化学式)
(3)设计实验探究滤渣A的成分
【提出问题】滤渣A的成分是什么?
【查阅资料】银、铜、铁、铝四种金属中,只有铝能与氢氧化钠溶液反应,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑
【提出猜想】滤渣A的成分为:
猜想一:银、铜 猜想二:银、铜、铁 猜想三:银、铜、铁、______.
【分析思考】猜想一______(填“是”或“否”)合理,理由是__________________
【进行实验】区两份滤渣A样品进行以下实验,请填写下列空白。
样品
加入试剂
实验现象
第一份样品
足量稀盐酸
产生气泡,固体部分溶解,溶液变为___________
第二份样品
足量氢氧化钠溶液
现象b
【做出判断】①如果现象b为“产生气泡,固体部分溶解”,则猜想_____成立;
②如果现象b为“______________________”,则猜想_____成立;
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列标签为哈药集团生产的“新盖中盖牌”高钙片的部分文字,请回答:

(1)碳酸钙是由______种元素组成;
(2)碳酸钙中钙元素的质量分数为 ______ ;
(3)若要补钙1g,则要服用钙片________片。
(4)每片高钙片中碳酸钙的质量分数为_______;
-
科目: 来源: 题型:
查看答案和解析>>【题目】为测定铜锌合金中锌的质量分数,进行了以下实验;取40g铜锌合金放入烧杯中,称得烧杯及所盛铜锌合金的总质量为140g,再把120g盐酸平均分成四份依次加入烧杯中,每次充分反应后进行称量,实验数据如下:
所加盐酸的次数
第一次
第二次
第三次
第四次
烧杯及所盛物质的总质量/g
169.7
199.4
229.2
259.2
请你据此分析计算:
(1)第一次实验生成氢气的质量是 ________ g.
(2)利用第一次实验的数据,计算30g盐酸中溶质的质量分数________ (写出计算过程,精确到0.1%)
(3)实验最终结束后,同学们求出了合金中锌的质量分数=__________.
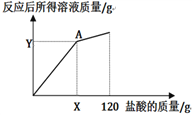
(4)下图表示所加盐酸的质量与反应后所得溶液质量的关系曲线,请写出A点(X=______ ,Y=______)的坐标。
相关试题

