【题目】请根据下图所示的实验装置图填空。
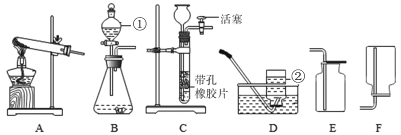
(1)D图中②的仪器名称为__________。
(2)实验室用B装置制取氧气时,发生反应的化学方程式为__________,
仪器①的作用是__________(写一点即可)。
(3)现有大理石、碳酸钠粉末、稀盐酸、稀硫酸,选择合适的物质用C装置制取CO2气体,其化学方程式为__________,在反应过程中,使反应停止的操作是__________。
(4)实验室常用加热醋酸钠和碱石灰的固体混合物来制取甲烷气体。甲烷是一种无色无味、密度比空气小、极难溶于水的气体,则制取并收集甲烷的装置组合是__________,若用右图装置收集甲烷,气体应从_________端导入(选填“a”或“b”)。

(5)小明同学用锌粒和稀盐酸制取氢气,小华认为小明制取的氢气不纯,杂质气体除了水蒸气外还含有__________(填化学式),基于以上问题,两位同学最终设计了如下方案制取纯净、干燥的氢气,请回答下列问题。
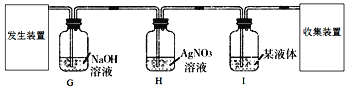
①H中硝酸银溶液的作用是__________;
②I中液体是__________(填名称)。
参考答案:
【答案】 集气瓶 2H2O2 ![]() 2H2O + O2↑ 便于添加液体药品、控制滴加液体速率可以控制化学反应的速率(合理即可) CaCO3+2HCl=CaCl2 +CO2↑ +H2O 关闭活塞 AF或AD b HCl 检验氯化氢已除尽(或证明氯化氢已除尽) 浓硫酸(没浓或写化学式不给分)
2H2O + O2↑ 便于添加液体药品、控制滴加液体速率可以控制化学反应的速率(合理即可) CaCO3+2HCl=CaCl2 +CO2↑ +H2O 关闭活塞 AF或AD b HCl 检验氯化氢已除尽(或证明氯化氢已除尽) 浓硫酸(没浓或写化学式不给分)
【解析】(1)由图可知D图中②的仪器是集气瓶;(2)B装置是固液在常温下反应的装置,故是用过氧化氢制取氧气:2H2O2 ![]() 2H2O + O2↑;过氧化氢接触到二氧化锰后,反应便立即开始,不能人为控制其速率和生成氧气的量,故要控制其反应速率,可通过控制过氧化氢的加入量来实现;分液漏斗就可以控制加入液体药品的量和速率;(3)实验室用石灰石或大理石和稀盐酸反应制取二氧化碳气体,同时还生成了氯化钙和水:CaCO3+2HCl=CaCl2 +CO2↑ +H2O;C装置中可将石灰石放在有孔隔板上,当不需要反应时,关闭活塞,稀盐酸进入到长颈漏斗中,石灰石和稀盐酸分离,反应停止;(4)根据反应物的状态和反应条件选择发生装置,用加热醋酸钠和碱石灰的固体混合物来制取甲烷气体属固固加热型,选A为发生装置;甲烷密度比空气小、极难溶于水,故可用向下排空气法或排水法收集,收集装置选F或D;甲烷的密度比空气小,会先聚集在集气瓶的上部,故甲烷应从b端通入;(5)盐酸具有挥发性,故用锌粒和稀盐酸制取的氢气中可能含有氯化氢气体;要制取纯净、干燥的氢气,那么先要把氯化氢气体除去,再通过浓硫酸进行干燥。氯化氢气体溶于水形成盐酸,盐酸能与氢氧化钠溶液反应,故G装置用于除去氯化氢气体,盐酸能与氯化银溶液反应生成氯化银沉淀,故用氯化银溶液来检验氯化氢气体是否除尽,最后将气体通过浓硫酸干燥剂可得到纯净干燥的氢气。
2H2O + O2↑;过氧化氢接触到二氧化锰后,反应便立即开始,不能人为控制其速率和生成氧气的量,故要控制其反应速率,可通过控制过氧化氢的加入量来实现;分液漏斗就可以控制加入液体药品的量和速率;(3)实验室用石灰石或大理石和稀盐酸反应制取二氧化碳气体,同时还生成了氯化钙和水:CaCO3+2HCl=CaCl2 +CO2↑ +H2O;C装置中可将石灰石放在有孔隔板上,当不需要反应时,关闭活塞,稀盐酸进入到长颈漏斗中,石灰石和稀盐酸分离,反应停止;(4)根据反应物的状态和反应条件选择发生装置,用加热醋酸钠和碱石灰的固体混合物来制取甲烷气体属固固加热型,选A为发生装置;甲烷密度比空气小、极难溶于水,故可用向下排空气法或排水法收集,收集装置选F或D;甲烷的密度比空气小,会先聚集在集气瓶的上部,故甲烷应从b端通入;(5)盐酸具有挥发性,故用锌粒和稀盐酸制取的氢气中可能含有氯化氢气体;要制取纯净、干燥的氢气,那么先要把氯化氢气体除去,再通过浓硫酸进行干燥。氯化氢气体溶于水形成盐酸,盐酸能与氢氧化钠溶液反应,故G装置用于除去氯化氢气体,盐酸能与氯化银溶液反应生成氯化银沉淀,故用氯化银溶液来检验氯化氢气体是否除尽,最后将气体通过浓硫酸干燥剂可得到纯净干燥的氢气。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列方法可使海水转化为饮用水的是
A.过滤 B.静置沉淀 C.活性炭吸附 D.蒸馏
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据要求回答下列问题。
(1)用化学用语表示:
①氯化钠中的阳离子__________;②硫酸亚铁中铁元素的化合价__________。
③氯气(Cl2)是一种重要工业原料,实验室通常以二氧化锰和浓盐酸制备氯气,发生如下反应:MnO2+4HCl(浓)
 Cl2↑+X+2H2O,其中X的化学式是__________。
Cl2↑+X+2H2O,其中X的化学式是__________。④氢气是清洁能源,其燃烧的化学方程式为__________。
(2)铁是应用最广泛的金属。
①喷漆能防止铁生锈,原因是__________。
②工业炼铁时,一氧化碳和赤铁矿(主要成分是氧化铁)发生的主要反应的化学方程式为__________。
(3)水是生命之源。
①生活中既能降低水的硬度,又能杀菌消毒的方法是__________。
②含氮的物质进入水中会造成水中藻类大量繁殖,使水体富营养化,导致水质恶化。这里的“氮”是指__________(填序号)。
A.元素 B.原子 C.离子 D.分子
-
科目: 来源: 题型:
查看答案和解析>>【题目】小杰同学从家里带来一个小纸袋,上面写着“石灰干燥剂”,纸袋上信息如图,实验小组同学对该干燥剂进行如下探究。

【辨析推断】
(1)“石灰干燥剂”中的石灰是指__________(填字母)。
A.消石灰 B.生石灰 C.石灰石
(2)不可食用,幼儿勿取的原因__________。
【提出问题】该袋干燥剂的现有成份是什么呢?
【实验探究】分别取该石灰干燥剂进行如表实验,并记录。
实验目的
实验步骤
实验现象
实验结论
实验一:验证有无
CaCO3
__________
样品中有碳酸钙
实验二:__________

无放热现象
__________
【问题分析】同学们由上表现象结合已学知识综合分析后,认为该袋干燥剂的成份可能为:
①碳酸钙 ②碳酸钙和__________
【成分探究】取少量样品加水溶解,静置后取少量上层清液于试管中,再向试管中__________,观察到__________,证明该固体成分是两种物质。
-
科目: 来源: 题型:
查看答案和解析>>【题目】生活中的下列事件,利用了溶解原理的是
A. 将硬水变为软水 B. 用洗洁精洗去餐具上的油污
C. 用汽油洗去衣服上的油污 D. 海水晒盐
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列关于物质的组成和构成的说法不正确的是
A.酒精(C2H5OH)是由碳、氢、氧三种元素组成
B.二氧化碳分子是由碳原子和氧原子构成
C.氧气和臭氧都是由氧元素组成的单质
D.双氧水(H2O2)由氢分子和氧分子构成
-
科目: 来源: 题型:
查看答案和解析>>【题目】硫酸的用途极广,常用于生产化肥、冶炼金属等。浓硫酸具有吸水性、脱水性和强腐蚀性等。工业制硫酸的流程:

(1)①上述流程中一共出现了__________种氧化物,工业制H2SO4可能会引起的环境问题是___________。
②用小木棍蘸少量浓硫酸,放置一会儿后,可观察到蘸有浓硫酸的部位变__________色。
(2)某工厂用一定质量分数的稀硫酸处理含有Ba(OH)2的残液,变化关系如图。
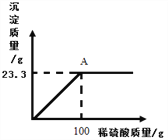
①A点液体的pH=__________(不考虑其它影响);
②所用稀硫酸的溶质质量分数为多少________(写出计算过程)。
相关试题

