【题目】为了帮助同学们更好的理解空气中氧气含量测定的实验原理,老师利用传感器技术实时测定了实验装置(如图1)内的压强、温度和氧气浓度,三条曲线变化趋势如图2所示。
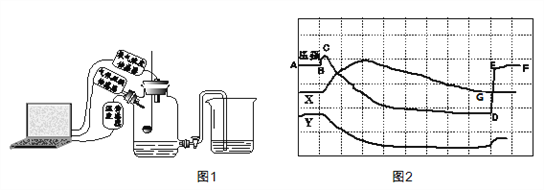
(1)Y曲线表示的是__________(填“温度”或“氧气的浓度”)。
(2)从图中哪里可以看出降至室温时打开的旋塞? __________
(3)从图中哪里可以看出集气瓶中的氧气并没有消耗到0? __________
参考答案:
【答案】 氧气的浓度 G点开始温度恒定,D点的横坐标在G点之后 Y曲线后部分纵坐标值增大
【解析】本题考查了空气中氧气的含量的测定实验。认真审题,结合已有的知识,读懂几个物理量的变化趋势是解题的关键。
(1)Y曲线主要是逐渐下降的过程,红磷燃烧时,氧气在不断消耗,氧气浓度不断减小,所以Y曲线表示的是氧气浓度,红磷燃烧放热,容器内的温度升高,反应结束后容器内的温度逐渐下降至室温,所以X曲线表示的是温度;
(2)红磷燃烧放热,容器内的温度升高,反应结束后容器内的温度逐渐下降至室温,所以X曲线表示的是温度,G点开始温度恒定,D点的横坐标在G点之后,所以该实验是降至室温时打开的旋塞;
(3)Y曲线后部分纵坐标值增大,可以看出集气瓶中的氧气并没有消耗到0。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验小组同学通过以下实验研究二氧化碳的性质。
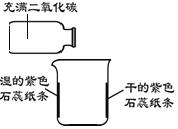
①在烧杯内壁上贴上干的和用水润湿的紫色石蕊纸条
②将充满二氧化碳的集气瓶轻轻在烧杯上方倾斜
一段时间后,湿的紫色石蕊纸条变为红色
(1)烧杯内壁上贴干的紫色石蕊纸条的目的是__________。
(2)该实验发生反应的化学方程式为__________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】二氧化钛(TiO2)是许多反应的催化剂。工业上用钛铁矿(主要成分为FeTiO3(钛酸亚铁,不溶于水)、Fe2O3及少量SiO2(不与H2SO4反应且不溶于水))作原料,制取二氧化钛及绿矾(FeSO4·7H2O),其生产流程如下:
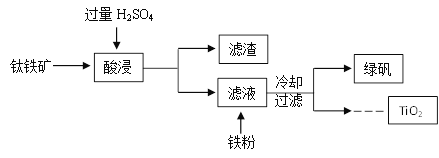
(1)TiO2中钛元素的化合价为__________。
(2)加入铁粉,发生置换反应的化学方程式为__________。
(3)以TiO2为原料还可以制取金属Ti。请将其中的一步反应的化学方程式补充完整:TiO2+2Cl2+C=TiCl4 +__________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】学习了二氧化锰对过氧化氢分解有催化作用的知识后,某兴趣小组同学在课外进行了有关过氧化氢分解反应的再探究。
(查阅资料)催化剂指的是能够改变化学反应的速率而自身的质量和化学性质在化学反应前后均不发生变化的物质。
(探究一)影响过氧化氢分解速率的因素有哪些?
兴趣小组同学做了四个实验,实验数据如下表:
实验
序号
H2O2溶液的溶质质量分数%
H2O2溶液的体积/mL
温度/℃
MnO2的用量/g
收集O2的体积/mL
反应
时间
①
5
1
20
0.1
4
16 s
②
15
1
20
0.1
4
6 s
③
30
5
35
0
4
98 min
④
30
5
55
0
4
20min
(1)过氧化氢分解速率与温度的关系是__________。
(2)能说明过氧化氢的分解速率与其质量分数有关的实验是__________(填实验序号)。
(探究二)MnO2的聚集状态是否影响其催化效果?
将质量相同但聚状态不同的MnO2分别加入到5mL5%的H2O2溶液中,测试结果如下:
MnO2的状态
操作情况
观察结果
粉末状
混合不振荡
剧烈反应,带火星的木条复燃
块状
反应较慢,火星红亮但木条未复燃
由上述实验得到的结论是__________。
(探究三)其他金属氧化物能否起到类似MnO2的催化作用?
兴趣小组同学用天平称量0.2gCuO,用量筒量取5mL5%的H2O2溶液,进行如下图所示实验(①~⑦代表实验操作步骤)。

(1)小组同学通过上述实验得出结论:CuO可作过氧化氢分解的催化剂,支持该结论的实验证据是__________。
(2)过氧化氢能被CuO催化分解放出氧气的化学反应方程式为__________。
(3)欲比较不同催化剂CuO和MnO2对H2O2分解速率的影响,实验时需要控制的变量有__________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】物质的下列用途主要利用其化学性质的是




A.液氧(支持燃烧)
B.金属铜(制电线)
C.活性炭(做防毒面具的吸附剂)
D.不锈钢(做水壶)
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关说法正确的是
A. 氧气、二氧化碳和过氧化氢三种物质中都含有氧分子
B.
 表示的粒子都是阴离子
表示的粒子都是阴离子C. 打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
D. 硝酸钾、氯化钠和硫酸铵三种物质在pH=10的溶液中能大量共存
-
科目: 来源: 题型:
查看答案和解析>>【题目】有一不纯的Na2CO3样品,杂质可能是K2CO3、CaCO3、FeCl3和NaCl中的一种或几种,取该样品10.6g,加入足量稀盐酸完全反应后得到无色容液,同时产生4.4g气体,下列判断正确的是
A. 杂质一定有FeCl3和CaCO3
B. 杂质一定没有NaCl
C. 杂质可能是K2CO3、CaCO3、NaCl组成的
D. 杂质可能是K2CO3和NaCl组成的
相关试题

