【题目】有一不纯的Na2CO3样品,杂质可能是K2CO3、CaCO3、FeCl3和NaCl中的一种或几种,取该样品10.6g,加入足量稀盐酸完全反应后得到无色容液,同时产生4.4g气体,下列判断正确的是
A. 杂质一定有FeCl3和CaCO3
B. 杂质一定没有NaCl
C. 杂质可能是K2CO3、CaCO3、NaCl组成的
D. 杂质可能是K2CO3和NaCl组成的
参考答案:
【答案】C
【解析】取该样品10.6g,加入足量稀盐酸完全反应后得到无色溶液,同时产生4.4g气体,说明原固体中一定不含氯化铁,故A错误;
设生成4.4g的二氧化碳气体,需要碳酸钠的质量为x
Na2CO3+2HCl ==2NaCl+H2O+CO2↑
106 44
x 4.4g
![]() =
=![]() ,解得x=10.6g,说明原混合物中一定含有另外一种碳酸盐,且该碳酸盐产生二氧化碳的能力要与碳酸钠相等或比碳酸钠强,碳酸钠中碳酸根离子的质量分数为60÷106×100%=56.6%,碳酸钾中碳酸根离子的质量分数为60÷138×100%=43.5%,碳酸钙中碳酸根离子的质量分数为60÷100×100%=60%,经计算碳酸钾产生二氧化碳的能力比碳酸钠弱,碳酸钙产生二氧化碳的能力比碳酸钠强,故混合物中一定含有碳酸钠和碳酸钙,可能含有碳酸钾和氯化钠,故BD错误。故选C。
,解得x=10.6g,说明原混合物中一定含有另外一种碳酸盐,且该碳酸盐产生二氧化碳的能力要与碳酸钠相等或比碳酸钠强,碳酸钠中碳酸根离子的质量分数为60÷106×100%=56.6%,碳酸钾中碳酸根离子的质量分数为60÷138×100%=43.5%,碳酸钙中碳酸根离子的质量分数为60÷100×100%=60%,经计算碳酸钾产生二氧化碳的能力比碳酸钠弱,碳酸钙产生二氧化碳的能力比碳酸钠强,故混合物中一定含有碳酸钠和碳酸钙,可能含有碳酸钾和氯化钠,故BD错误。故选C。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为了帮助同学们更好的理解空气中氧气含量测定的实验原理,老师利用传感器技术实时测定了实验装置(如图1)内的压强、温度和氧气浓度,三条曲线变化趋势如图2所示。
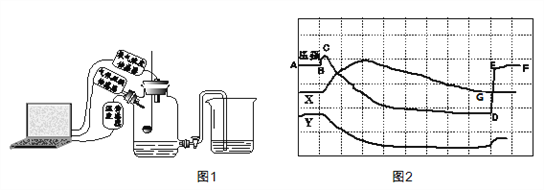
(1)Y曲线表示的是__________(填“温度”或“氧气的浓度”)。
(2)从图中哪里可以看出降至室温时打开的旋塞? __________
(3)从图中哪里可以看出集气瓶中的氧气并没有消耗到0? __________
-
科目: 来源: 题型:
查看答案和解析>>【题目】物质的下列用途主要利用其化学性质的是




A.液氧(支持燃烧)
B.金属铜(制电线)
C.活性炭(做防毒面具的吸附剂)
D.不锈钢(做水壶)
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关说法正确的是
A. 氧气、二氧化碳和过氧化氢三种物质中都含有氧分子
B.
 表示的粒子都是阴离子
表示的粒子都是阴离子C. 打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
D. 硝酸钾、氯化钠和硫酸铵三种物质在pH=10的溶液中能大量共存
-
科目: 来源: 题型:
查看答案和解析>>【题目】下表中,有关量的变化图像与其对应叙述相符的是
A
B
C
D
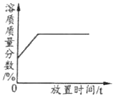
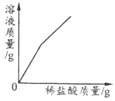
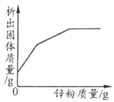
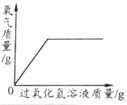
浓硫酸敞口放置一段时间
向一定质量的氧化铁粉末中加入稀盐酸
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn粉
向一定质量的二氧化锰中加入过氧化氢溶液
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)用化学式填空:石墨______ ;改良酸性土壤的碱_________。
(2)火箭推进器中装有液态肼(N2H4)和过氧化氢,当它们混合反应时,放出大量的热量,同时产生一种气态单质和一种常见的液体,写出有关反应的化学方程式_______________。
(3)在一定条件下,A和B两种物质发生反应生成C和D。下图为该反应的微观示意图。
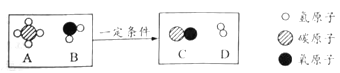
①从微观角度分析该反应的实质是______________。
②该反应中,生成C和D的质量比是___________。
(4)在托盘天平(灵敏度极高)两边各放盛有等质量、等质量分数足量稀硫酸的烧杯,天平平衡。向左烧杯中加入一定质量的金属M,同时向右烧杯中加入相同质量的金属N,观察到从反应开始至结束天平指针始终偏向右边(注:反应中都生成+2价的硫酸盐)。则:
①M、N两种金属的活动性由强到弱的顺序为____________。
②M、N两种金属的相对原子质量由大到小的顺序为__________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下图回答问题:
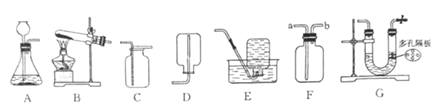
(1)实验室用高锰酸钾制取并收集较纯净的氧气,应选用的装置是________(填字母)。向气体发生装置内加入药品前应进行的操作是____________。
(2)实验室用石灰石和稀盐酸反应制取二氧化碳时,可选用发生装置A或G,G与A相比较,其优点是_________;若用F装置收集二氧化碳,检验二氧化碳已收集满的方法是______。如果要证明制取二氧化碳实验后的废液呈酸性,可选用的试剂是_______(填字母)。
a.紫色石蕊溶液 b.石灰石 c.氢氧化钠溶液 d.硝酸银溶液 e.铜
相关试题

