【题目】下列是甲、乙两组同学进行空气中氧气含量的测定实验探究.回答下列问题:
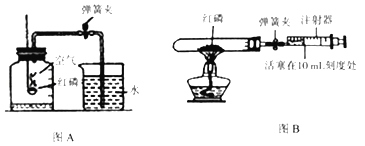
Ⅰ.甲组同学用图A装置进行实验.
(1)该实验过程中红磷需要过量,目的是_____,该反应的化学方程式为_____,其反应的基本类型属于_____反应.
(2)若将红磷换成炭粉,该实验能否获得成功?_____(填“能”或“不能”)成功,原因是_____.
Ⅱ.乙组同学用图B装置进行实验,选用容积为30mL的试管作为反应容器,实验步骤如下:
①将足量红磷装入试管中,将注射器活塞置于10mL刻度处,并按图B中所示的连接方式固定好,再将弹簧夹夹紧橡皮管.
②点燃酒精灯,给红磷加热.
③撤去酒精灯,待试管冷却后松开弹簧夹.
④读取注射器活塞的数据.
(1)充分冷却后打开弹簧夹,注射器活塞将从10mL刻度处慢慢向_____移动(填“左”或“右”)到约为_____mL刻度处才停止.若上述实验步骤①中,未用弹簧夹夹住橡皮管,其它步骤不变,则实验结束后注射器的活塞最终停在_____mL处刻度处.
(2)比较甲、乙两组实验,你认为乙组实验的优点是_____(答一点).
参考答案:
【答案】 使装置中的氧气完全反应 4P+5O2![]() 2P2O5 化合 不能 炭粉燃烧生成二氧化碳气体 左 4 2 实验结果更准确
2P2O5 化合 不能 炭粉燃烧生成二氧化碳气体 左 4 2 实验结果更准确
【解析】Ⅰ.(1)该实验过程中红磷需要过量,目的是使装置中的氧气完全反应。由两种物质生成另一种物质的反应属于化合反应。(2)测定空气中氧气含量的实验,所选择的物质必须是只与氧气反应,且无气体生成,而炭粉燃烧生成二氧化碳气体,故若将红磷换成炭粉,该实验不能获得成功。Ⅱ.(1)红磷燃烧消耗氧气,无气体生成,冷却到室温,试管内压强变小,故活塞向左移动。试管内的氧气体积是:30mL×![]() =6mL,故活塞向左移动到10mL-6mL=4mL处。若上述实验步骤①中,未用弹簧夹夹住橡皮管,其它步骤不变,则活塞与试管连通,其中氧气的体积是(30mL+10mL)×
=6mL,故活塞向左移动到10mL-6mL=4mL处。若上述实验步骤①中,未用弹簧夹夹住橡皮管,其它步骤不变,则活塞与试管连通,其中氧气的体积是(30mL+10mL)×![]() =8mL,故实验结束后注射器的活塞最终停在10mL-8mL=2mL刻度处。(2)乙组实验的实验结果更准确。
=8mL,故实验结束后注射器的活塞最终停在10mL-8mL=2mL刻度处。(2)乙组实验的实验结果更准确。
-
科目: 来源: 题型:
查看答案和解析>>【题目】模型与示意图是联系宏观与微观的桥梁.
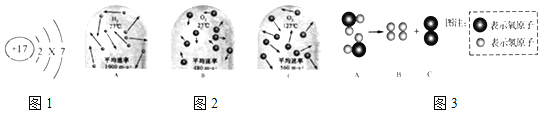
(1)如图1是氯原子的结构示意图.
①x的数值为_____.
②氯原子在化学反应中总易得到1个电子,形成_____(填离子符号).
(2)如图2是氢分子和氧分子运动的示意图.
①在A、B和C中,能比较得出“温度越高,分子运动速率越快”的是_____(填标号).
②从图中可见,影响分子运动速率的因素除温度外,还与_____有关.
(3)某物质A在通电时分解生成B和C,根据如图3微观结构示意图,写出其化学反应方程式:_____.
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图表示几种物质之间的转化关系:
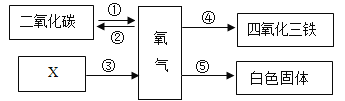
(1)反应①有利于维持空气中氧气含量的基本稳定,绿色植物实现转化①的过程发生了_____(填标号)
A.呼吸作用 B.光合作用 C.燃烧反应
(2)写出反应②中的另一种反应物_____.
(3)若反应③是分解反应,从物质的组成上分析,X中一定含有_____元素.
(4)反应④的化学方程式为_____.
(5)反应⑤燃烧时发出耀眼的白光,经常用做照明弹,其反应原理用化学方程式表示为_____.
-
科目: 来源: 题型:
查看答案和解析>>【题目】某饮用矿泉水1000g中的成分如图所示。
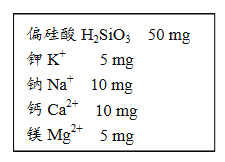
(1)此矿泉水中至少含有 种元素。
(2)在偏硅酸H2SiO3中,氢元素与氧元素的质量比为 。
(3)在偏硅酸H2SiO3中,求算硅元素的质量分数的计算式为 。
(4)某同学喝了500 g该矿泉水,他同时摄入的钾元素的质量为 mg。
-
科目: 来源: 题型:
查看答案和解析>>【题目】金属钛(Ti)的合金具有耐高温,耐腐蚀、强度高等性能,所以,钛合金广泛用于航空、航天工业及化学工业.工业上冶炼金属钛的过程是以钛矿石(主要成分为钛酸亚铁,化学式为FeTiO3)、焦炭、氯气为原料,在高温条件下制取TiCl4,其反应化学方程式为:2FeTiO3+6C+7Cl2
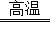 2TiCl4+2X+6CO,然后用镁与TiCl4在高温条件下反应生成金属钛和氯化镁.请根据以上信息回答下列问题:
2TiCl4+2X+6CO,然后用镁与TiCl4在高温条件下反应生成金属钛和氯化镁.请根据以上信息回答下列问题:(1)FeTiO3中钛元素的化合价为 价.
(2)在制备TiCl4的反应中,X的化学式为 .
(3)镁与TiCl4反应的化学方程式为: .
-
科目: 来源: 题型:
查看答案和解析>>【题目】人类的生产生活离不开金属材料.
(1)人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”,在“五金”顺序中把金属__的位置移到最后,正好符合由弱到强的__顺序.
(2)铝、铁、铜是我们生产生活中使用比较广泛的金属.如图1所示用品中,利用金属导热性的是__,延展性的是__(填字母序号).

(3)铜也容易生锈,铜锈的主要成分是碱式碳酸铜(Cu2(OH)2CO3),是铜与空气中的氧气、水和__共同作用的结果.
(4)合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质.一般来说,合金的熔点低于任何一种组成金属的熔点.下表是一些金属的熔点数据.
金属
铜
锌
锡
铅
铋
镉
熔点/℃
1083
419.6
231.9
327.5
271.3
320.9
①铅锡合金中某种金属的质量分数与合金的熔点有如图2所示的关系,其中横坐标表示的是__的质量分数;当合金熔点最低时,合金中铅与锡的质量比为__.
②保险丝由铋、铅、锡、镉组成,其熔点约为__.
A.15~30℃; B.60~80℃; C.235~250℃; D.300~320℃.
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室有一包纯净的铁粉,小明为了探究金属的化学性质并测定铁的相对原子质量,设计了如图的实验。
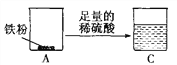

【实验步骤】
①取两份质量同为wg的铁粉,分别置于质量相等的A、B烧杯中。
②向装有铁粉的A烧杯中加入50 g足量的稀硫酸;向装有铁粉的B烧杯中加入50 g足量的硫酸铜溶液。
③充分反应后进行称量。C烧杯和烧杯内物质的总质量为mg,D烧杯和烧杯内物质的总质量为ng。
(1)请写出C烧杯中发生反应的化学方程式:___________。通过C烧杯中发生的化学反应,你能得出的结论是_______。
(2)D烧杯中发生反应的化学方程式为______________。此反应可以证明铁的金属活动性比铜_______(填“强”或“弱”)。
(3)铁的相对原子质量的表达式为_______。
相关试题

