【题目】某研究小组用如图所示装置,探究能否用镁条代替红磷测定空气中氧气含量。
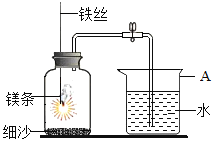
(提出猜想)
猜想1:可以代替,因为镁条与氧气反应后不会产生气体
猜想2:不能代替,因为镁条可能会与空气中的其他成分发生反应
(进行实验)
步骤 | 实验操作 | 实验现象 |
Ⅰ | 组装好装置后,打开止水夹,手捂集气瓶,一段时间后,松开手 | 烧杯中导管口有气泡冒出,松手后,烧杯中导管末端有一段液柱 |
Ⅱ | 关闭止水夹,点燃镁条,迅速伸入集气瓶中,塞好塞子 | 镁条燃烧,放出大量热,发出耀眼白光,生成大量白烟,剩余固体为白色带状物还夹杂着极少量淡黄色的固体 |
Ⅲ | 冷却至室温,打开止水夹 | 烧杯中水从导管进入集气瓶中,体积约为集气瓶体积的 |
(解释与结论)
(1)步骤Ⅰ的实验目的是_____。
(2)步骤Ⅱ中,关闭止水夹的目的是_____。
(3)根据实验现象中的_____(写一个即可)可以推测猜想2成立。
①(继续探究)经查阅资料得知氮化镁(Mg3N2)为淡黄色的固体,于是小晴猜想镁条还可能会与空气中的_____发生反应;
②(设计实验)她设计实验方案证明自己的猜想_____;
③(实验结论)镁条与氮气反应的化学方程式为:_____;
④(反思与评价)通过上述探究活动,你对燃烧有什么新的认识?_____。
参考答案:
【答案】检查装置的气密性 防止温度升高导致气压增大,将部分气体压出集气瓶 生成物中有极少量淡黄色的固体或进入集气瓶中水的体积约为集气瓶体积的![]() (写一个即可)。 氮气 将点燃的镁条伸入充满氮气的集气瓶中; 3Mg+N2
(写一个即可)。 氮气 将点燃的镁条伸入充满氮气的集气瓶中; 3Mg+N2![]() Mg3N2 燃烧不一定在氧气中进行(其他合理答案均可)
Mg3N2 燃烧不一定在氧气中进行(其他合理答案均可)
【解析】
(1)步骤Ⅰ的实验目的是:检查装置的气密性。
(2)步骤Ⅱ中,关闭止水夹的目的是:防止温度升高导致气压增大,将部分气体压出集气瓶。
(3)根据实验现象中的:已知氧气和镁反应生成白色的氧化镁,生成物中有极少量淡黄色的固体说明反应生成了其他物质,且已知氧气只占空气总体积的![]() ,故进入集气瓶中水的体积约为集气瓶体积的
,故进入集气瓶中水的体积约为集气瓶体积的![]() 说明空气中的其他物质参与了反应。
说明空气中的其他物质参与了反应。
①继续探究:经查阅资料得知氮化镁(Mg3N2)为淡黄色的固体,猜想镁条还可能会与空气中的氮气发生反应;
②设计实验:设计实验方案:将点燃的镁条伸入充满氮气的集气瓶中,观察现象;
③实验结论:镁条与氮气反应生成氮化镁,反应方程式为:3Mg+N2![]() Mg3N2;
Mg3N2;
④反思与评价:通过上述探究活动可知:燃烧不一定在氧气中进行;在一定的条件下,氮气也支持燃烧等(其他合理答案均可)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】2018年10月24日上午,被称为“现代世界新七大奇迹”之一的港珠澳大桥正式通车运营。
(1)大桥建设过程中离不开吊装,吊装缆绳采用的超高分子聚乙烯纤维干法纺丝。聚乙烯的化学式为(C2H4)n,其中碳、氢元素的质量比为_____。
(2)大桥横跨“伶仃洋”。海洋中蕴含丰富的水资源,海水属于_____(填“纯净物”或“混合物”),我们可以通过_____操作除去海水中的难溶性杂质。检验海水是硬水还是软水的方法是_____。

-
科目: 来源: 题型:
查看答案和解析>>【题目】首届进口博览会的吉样物“进宝”为手持的四叶草的“国宝”大熊猫,代表幸运幸福。化学物质世界也迎来了一只手持四叶草的“进宝”物质X,如图所示。四叶草的叶子由A、B、C、D四种物质构成,且相邻两叶片之间会发生反应;其中C、D是黑色固体,B、C为单质,A、D为氧化物。
(1)物质C为_____;物质B在生活中的一种用途是_____;
(2)A和D反应的化学方程式可能是_____;
(3)手持四叶草的“进宝”物质X需满足:A、B、C、D分别通过一步反应能直接转化为X,则物质X是_____。

-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室制取气体的部分装置如图所示.
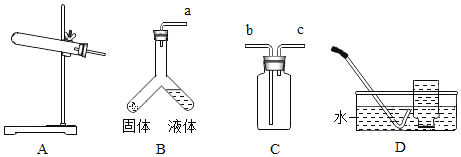
(1)用装置A制备O2
①若用高锰酸钾为原料,装置A中缺少的仪器是_____.该反应的化学 方程式为_____.
②若用过氧化氢溶液和二氧化锰为原料,改造装置A的操作是:_____.
(2)用组合装置BD制取气体
①实验室一般不用D装置收集二氧化碳,原因是_____.
②该装置中发生反应的化学方程式为_____(写一个).
③待观察到气泡_____放出时,才能开始收集气体.
(3)用组合装置BC制取二氧化碳
①装置B中盛有的固体是_____(填名称,下同),液体是_____,将固体与液体药品混合后可制得二氧化碳.
②检验二氧化碳是否集满,可将燃着木条置于装置C的_____(填“b”或“c”)端管口处观察现象.
-
科目: 来源: 题型:
查看答案和解析>>【题目】学小组用如图所示自制装置进行“人体吸入和呼出气体成分”的探究。
(提出假设)人体呼出气体中二氧化碳的含量高于吸入气体。
(实验活动1)
装置
实验操作
现象

①在饮料瓶中装水至没过长吸管底端,对着短吸管缓慢吹气
水从长吸管端快速流出
②将饮料瓶中装满水,对着短管吹气,用排水法收集呼出气体,将燃着的木条快速伸入饮料瓶中
饮料瓶中木条熄灭
③将水倒掉,向饮料瓶中加入澄清石灰水至没过长吸管底,从短吸管端吸气30秒,观察石灰水的变化;再从长吸管端吹气30秒,观察石灰水的变化
(1)步骤①说明,自制装置的气密性_____(填“良好”或“不好”)。
(2)步骤②中的现象_____(填“能”或“不能”)证明呼出气体中含二氧化碳,原因是_____。
(3)若假设成立,步骤③中,预期会观察到的现象是_____。发生反应的化学方程式为_____。
(实验活动2)实验1中有同学发现,吹气一段时间后发现,浑浊的石灰水重新变得澄清,他用上述装置加入与实验1等体积的石灰水,做下列实验来研究这一问题。
实验编号
石灰水浓度
持续吹气时间
瓶底现象
④
0.16%
30秒
澄清石灰水变浑浊
⑤
0.16%
2分钟
澄清石灰水先变浑浊,后又变得澄清
⑥
0.08%
30秒
澄清石灰水先变浑浊,后又变得澄清
⑦
0.08%
2分钟
澄清石灰水先变浑浊,后又变得澄清
(反思与评价)
(4)能说明石灰水重新变澄清与石灰水浓度有关的实验是_____(填实验编号)。
(5)实验1中,吹气时间均为30秒,有同学观察到石灰水变澄清,而有的学生未观察到产生现象差异的可能原因是_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】今年我省人大和政协两会使用了一种含碳酸钙的“石头纸”:为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。分别在5只烧杯中进行了实验,实验数据见下表(假设纸张其他成分既不溶于水,也不与酸反应):
烧杯①
烧杯②
烧杯③
烧杯④
烧杯⑤
加入样品的质量/g
10
10
10
10
10
加入稀盐酸的质量/g
10
20
30
40
50
充分反应后生成气体的质量/g
0.88
1.76
2.64
3.52
3.52
(1)10g样品与足量稀盐酸反应最多生成_____g气体;
(2)上述实验中盐酸过量的是烧杯_____(填序号);
(3)求样品中碳酸钙的质量分数_____。(写出计算过程)
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列事实与对应的解释相符合的是
A. 甘蔗甜,苦瓜苦:不同分子性质不同
B. 空气能被压缩:分子体积可以变小
C. 结冰的水不能流动:结冰时水分子不再运动
D. 50mL水和50mL酒精混合后的总体积小于100mL:分子的质量和体积都很小
相关试题

