3. 道尔顿的原子学说曾起了很大作用,他的学说中,包含有下述三个论点:
(1)原子是不能再分的粒子。
(2)同种元素的原子的各种性质和质量都相同。
(3)原子是微小的实心球体。
用现在的观点看,你认为这三个论点中,不确切的是()
A. (3) B. (1)(3)
C. (2)(3) D. (1)(2)(3)
32.(5分)某厂用石灰石高温煅烧制得生石灰,若每天消耗含杂质5%的石灰石原料300吨。请根据计算回答下列问题:
⑴理论上每天可生产氧化钙多少吨(假设杂质受热不分解)?
⑵若每吨石灰石以100元的价格买入,制得的生石灰(含原杂质)以每吨250元卖出,扣除每吨石灰石原料生产的加工费30元,则该厂每天可获利润多少元?
泰州市2005年初中毕业、升学统一考试化学试题
31.(3分)我国科学家陈乾旺等最新研究成果表明,在440℃和800大气压条件下,二氧化碳和金属钠反应产生金刚石和碳酸钠,合成的金刚石最大达1.2mm,完全可以满足工业用途。
⑴二氧化碳与金属钠反应生成金刚石和碳酸钠的化学方程式为:
。
⑵请从人类生存的角度分析,金刚石与水相比谁更宝贵? ,
理由是: 。

30.(2分)二氧化碳在化学家的眼里是可以利用的重要资源,只要有合适的条件,可以像发生光合作用那样将二氧化碳转变为所需要的产物。二氧化碳可以为化工合成提供足够的碳元素,既可以减少化工产业对煤和石油的消耗,又可以缓解大气中二氧化碳含量的增加。
⑴二氧化碳和水通过光合作用转变为葡萄糖和氧气的化学方程式为:
。
⑵化肥厂用二氧化碳与氨气在一定条件下反应生成尿素[CO(NH2)2]和水的化学方程式为:
。
29.(6分)常温常压下1体积水约溶解1体积二氧化碳气体,氢氧化钠溶液与二氧化碳反应时没有明显的现象变化。某研究小组设计了下列实验装置 (所有装置的气密性良好) ,试图通过观察现象来间接证明二氧化碳与氢氧化钠发生了反应。





⑴请根据上图实验装置和下表的操作方法,将可能观察到的实验现象填入下表中:
|
所选 装置 |
操作方法 |
实验现象 |
|
A |
将充满二氧化碳的试管倒扣在水中 |
试管内的液面略有上升 |
|
B |
将充满二氧化碳的试管倒扣在氢氧化钠溶液中 |
|
|
C |
将氢氧化钠溶液滴入烧瓶 |
|
|
D |
将氢氧化钠溶液滴入锥形瓶 |
|
|
E |
将胶头滴管中氢氧化钠溶液挤入烧瓶 |
|
⑵若再分别向A、B装置的烧杯中滴入少量氯化钙溶液,将会看到的现象是:
A: ;B: 。
28.(5分)为减缓二氧化碳使全球变暖的趋势,有科学家提出大胆设想:将排放到空气中的二氧化碳压缩使其液化,然后将其压入到冰冷的深海中。但也有科学家担心海水中富含二氧化碳后酸度会增加,可能会杀死一些海洋生物,甚至会溶解掉部分海床,同时气候变化也可能改变海洋环流,把海底的二氧化碳又带回海面,另外把二氧化碳压入海底所消耗的能源可能会再增加二氧化碳的排放。
⑴ 二氧化碳气体转变为液体时将会 能量(填“释放”或“消耗”);
⑵二氧化碳使海水酸度增加的原理用化学方程式表示为: ;
⑶二氧化碳在深海中的溶解度比在通常状况下的水中的溶解度 ,原因是
。
环境问题是人类可持续发展必须解决的一个重要问题,温室效应被列为21世纪人类面临的最大威胁之一,已引起人们的广泛关注。旨在限制发达国家温室气体排放量、抑制全球范围内气候持续变暖的《京都议定书》,已于2005年2月16日正式生效。
27.(2分)二氧化碳是大气中的主要温室气体,我国二氧化碳的排放量位居世界第二,为减少二氧化碳这种温室气体的排放,我们可以采取的措施有(只填2种):
; 。
26.(12分)甲同学在某食品包装袋内,发现有一个装有白色颗粒状固体A的小纸袋,上面写着“生石灰干燥剂,请勿食用”。甲同学随手将小纸袋拿出来放在空气中,经过一段时间后,发现纸袋内的白色颗粒粘在一起成为块状固体B。请你与甲同学一起对块状固体B进行探究。
(1)猜想一:块状固体B中除氧化钙外还可能有: 、 。
写出白色颗粒状固体A在空气中转化为块状固体B的化学反应方程式:
;
。
(2)猜想二:块状固体B溶于水可能有 现象(填“放热”或“吸热”)。请设计实验方案验证你的这一猜想(至少写出两种方案,如果写出三种正确方案奖励1分):
① ;
② ;
③ 。
(3)取适量块状固体B加入盛有一定量水的试管中,振荡、静置、过滤,得到少量白色固体C。就白色固体C的成分,甲同学与乙同学进行讨论,一起猜想。
甲同学认为,白色固体C可能是:氢氧化钙;
乙同学认为,白色固体C可能是:碳酸钙;
你认为,白色固体C还可能是: 。
请设计实验证明你的猜想(填写下表):
|
方 案 |
现 象 和 结 论 |
|
|
|

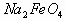 ),铁元素的化合价是(
)
),铁元素的化合价是(
)