【题目】(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为__________、_______。
(2)用甲烷制取氢气的两步反应的能量变化如下图所示:

甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是________________。
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-159.5KJ/mol
②NH2CO2NH4(s)= CO(NH2)2(s) +H2O(g) △H=+116.5KJ/mol
③H2O(l)=H2O(g) △H=+44KJ/mol
写出CO2与NH3合成尿素和液态水的热化学方程式__________________。
(4)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极在碱性条件下发生反应的电极反应式为_________________。
参考答案:
【答案】 正极:O2 + 4e- +2H2O = 4OH- 负极:Fe - 2e- = Fe 2+ CH4 (g)+ 2H2O(g) = CO2(g) +4H2(g) △H=-136.5KJ/mol 2NH3(g) +CO2(g) = CO(NH2)2(g) +H2O(g) △H=-87.0KJ/mol 2NH3 -6e- +6OH- = N2 + 6H2O
【解析】(1)钢铁发生吸氧腐蚀时,铁作负极,发生失电子的氧化反应,即Fe=Fe2++2e-,碳作正极,正极上氧气得电子发生还原反应,电极反应式为:2H2O+O2+4e-=4OH-,故答案为:负极:Fe=Fe2++2e-,正极:2H2O+O2+4e-=4OH-;:
(2)根据第一步反应过程可以得出:CH4(g)+H2O(g)=3H2(g)+CO(g),△H=-103.3KJ/mol;根据第二步反应过程可以得出:CO(g)+H2O(g)=H2(g)+CO2(g),△H=-33.2KJ/mol;根据盖斯定律,上下两式相加可得:CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=-136.5kJ/mol,故答案为:CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=-136.5kJ/mol;
(3)①2NH3(g)+CO2(g)→NH2CO2 NH4(s)△H=-l59.5kJ/mol,②NH2CO2NH4(s)→CO(NH2)2(s)+H2O(g)△H=+116.5kJ/mol,③H2O(l)→H2O(g)△H=+44.0kJ/mol,依据热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-87.0 kJmol-1;故答案为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-87.0 kJmol-1;
(4)在燃料电池中,燃料做负极,则通入氨气的电极是负极,碱性条件下,该电极发生反应的电极反应式为2NH3-6e-+6OH-=N2+6H2O,故答案为:2NH3-6e-+6OH-=N2+6H2O。
-
科目: 来源: 题型:
查看答案和解析>>【题目】检验二氧化碳中是否含有二氧化硫,可将气体通入
A.澄清石灰水B.品红溶液
C.小苏打溶液D.紫色石蕊试液
-
科目: 来源: 题型:
查看答案和解析>>【题目】以下物质之间的每步转化中,都能通过一步实现的是( )
①Fe→FeCl2→Fe(OH)2→ Fe(OH)3
②Na→Na2O→Na2CO3→NaHCO3→NaOH
③Mg→MgCl2→Mg(OH)2
④Al→Al2O3→Al(OH)3
⑤Al→NaAlO2→Na2CO3
A. ②③④ B. ①③④⑤ C. ①②③⑤ D. ①②③④⑤
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图所示,某同学设计了一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和原理和粗铜的精炼原理,乙装置中X为阳离子交换膜。根据要求回答下列相关问题:

(1)通入氧气的电极为_____(填“正极”或“负极”),写出负极的电极反应式_____.
(2)铁电极为_____(填“阳极”或“阴极”),石墨电极的电极反应式为_____.
(3)反应一段时间后,乙装置中生成NaOH主要在_____(填“铁极”或“石墨极”)区.
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为_____,反应一段时间,硫酸铜溶液浓度将_____(填“增大”“减小”或“不变”).
(5)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下的体积为_____;丙装置中阴极析出铜的质量为_____.
-
科目: 来源: 题型:
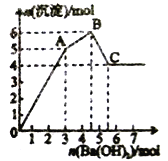
查看答案和解析>>【题目】向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2溶液,形成沉淀的情况如图所示。
氢氧化物
溶液pH
开始沉淀
沉淀完全
沉淀开始溶解
沉淀完全溶解
Fe(OH)3
2.3
3.4
-
-
A1(OH)3
3.3
5.2
7.8
12.8
A. 据图计算原溶液中c(Cl-)>c(SO42-)
B. C点的沉淀为Fe (OH)3
C. AB段可能发生的反应是:2SO42-+ 2Ba2+ + Al3+ + 3OH- == 2BaSO4↓ + A1(OH)3↓
D. OA段可能发生的反应是:3Ba2+ + 6OH- + 3SO42- + Fe3+ + Al3+ = 3BaSO4↓ + Fe (OH)3↓ + A1(OH)3↓
-
科目: 来源: 题型:
查看答案和解析>>【题目】工业上,向500﹣600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢生产无水氯化亚铁.现用如图所示的装置模拟上述过程进行实验.

回答下列问题:
(1)制取无水氯化铁的实验中,A中反应的化学方程式为 , 当生成1molCl2时,转移的电子数为 , 玻璃丝的作用是 , 装置B中加入的试剂是 . 装置D中加入的试剂是 .
(2)制取无水氯化亚铁的实验中,尾气的成分是 . 若仍用D的装置进行尾气处理,存在的问题是、 .
(3)若操作不当,制得的FeCl2 会含有少量FeCl3杂质,下列说法中正确的是
A.检验FeCl3常用的试剂是KSCN溶液
B.可向固体混合物中加入适量Fe粉除去杂质
C.可向固体混合物中通入适量Cl2除去杂质
D.欲制得纯净的FeCl2 , 在实验操作中应先点燃A处的酒精灯,在点燃C处的酒精灯.
(4)现有一包FeCl2和FeCl3混合物,某化学兴趣小组为测定各成分的含量进行如下两个实验:
实验1:①称取一定质量的样品,将样品溶解;②向溶解后的溶液中加入足量的AgNO3溶液,产生沉淀;③将沉淀过滤、洗涤、干燥得到白色固体28.7g.
实验2:①称取与实验1中相同质量的样品,溶解;②加入足量的NaOH溶液,③将沉淀过滤、洗涤后,加热灼烧到质量不再减少,得到固体6.4g.
则样品中FeCl3的物质的量为 . -
科目: 来源: 题型:
查看答案和解析>>【题目】试回答下列中和热测定的有关问题。
(1)实验桌上备有大烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、环形玻璃搅拌棒、0.50mol/L盐酸、0.55mol·L-1NaOH溶液,尚缺少的实验用品是_________。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒______,其原因是_________。
(3)实验时所用盐酸及NaOH溶液的体积均为50mL,各溶液密度为1g/cm3,生成溶液的比热容c=4.18J/(g·℃),实验起始温度为t1℃,终止温度为t2℃。试计算该反应的中和热ΔH=_________。
相关试题

