【题目】某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略)。实验开始前,向装置中通入一段时间的N2,排尽装置内的空气。

已知:在溶液中.FeSO4+NO![]() [Fe(NO)]SO4(棕色),该反应可用于检验NO。下列说法不正确的是
[Fe(NO)]SO4(棕色),该反应可用于检验NO。下列说法不正确的是
A. 装置B、E中的试剂依次为水、硫酸亚铁溶液
B. 若观察到装置D中红色粉末变黑色,则NO与Cu发生了反应
C. 实验结束后,先关闭分液漏斗的活塞,再熄灭酒精灯
D. 装置F收集的气体中可能含有NO
参考答案:
【答案】C
【解析】
稀硝酸与铜反应生成一氧化氮,能够被氧气氧化为二氧化氮,因此实验前需要通入氮气,排除装置中的空气;硝酸具有挥发性,生成的一氧化氮中混有少量硝酸蒸气,可以通过水吸收后再干燥,然后再探究干燥的一氧化氮在加热时与铜的反应,未反应的NO可以利用硫酸亚铁溶液检验;据以上分析解答。
稀硝酸与铜反应生成一氧化氮,能够被氧气氧化为二氧化氮,因此实验前需要通入氮气,排除装置中的空气;硝酸具有挥发性,生成的一氧化氮中混有少量硝酸蒸气,可以通过水吸收后再干燥,然后再探究干燥的一氧化氮在加热时与铜的反应,未反应的NO可以利用硫酸亚铁溶液检验,
A项,根据上述分析,装置F、I中的试剂依次为水、硫酸亚铁溶液,故A项正确;
B项,若观察到装置H中红色粉末变黑色,说明NO与Cu发生了反应,生成了氧化铜,故B项正确;
C项,实验结束后,为了防止倒吸,需要先熄灭酒精灯,再关闭分液漏斗的活塞,停止通入NO,故C项错误。
D项,由于FeSO4+NO![]() [Fe(NO)]SO4(棕色),为可逆反应,装置J收集的气体中可能含有NO ,故D项正确;
[Fe(NO)]SO4(棕色),为可逆反应,装置J收集的气体中可能含有NO ,故D项正确;
综上所述,本题选C。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据物质结构和元素周期表的相关知识回答下列问题:
I.用A+、B-、C2-、D表示含有18个电子的离子或分子。请填空:
(1)A元素是__________,B元素是__________,C元素是__________。(用元素符号表示)
(2)物质D由两种元素组成,每个分子中含有三个原子,其电子式表示D形成过程是 _____。
Ⅱ.X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。回答下列问题:
(1)Y在元素周期表中的位置为______,
(2)上述元素的最高价氧化物对应的水化物酸性最强的是_______ (写化学式)。
(3)Y和Z的两元素之间形成的原子个数比为1:1的化合物的电子式为________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列过程,观察不到颜色变化的是( )
A.NO气体暴露在空气中
B.往FeCl3溶液中滴入KSCN溶液
C.Cl2通过湿润的有色布条
D.往NaOH溶液中通入CO2
-
科目: 来源: 题型:
查看答案和解析>>【题目】在反应5NH4NO3=2HNO3+4N2↑+9H2O中,发生氧化反应和发生还原反应的氮原子个数比是
A.5:8B.3:5C.5:4D.5:3
-
科目: 来源: 题型:
查看答案和解析>>【题目】对可逆反应4NH3(g)+ 5O2(g)
 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是A. 达到化学平衡时,4υ正(O2)= 5υ逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
C. 达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D. 化学反应速率关系是:2υ正(NH3)= 3υ正(H2O)
-
科目: 来源: 题型:
查看答案和解析>>【题目】在一体积为2 L的密闭容器中充入2 mol X,一定条件下可发生反应:2X(g)
 3Y(g),该反应的反应速率(v)与时间(t)的关系如图所示,已知t2 min时容器内有1.5 mol Y。下列叙述正确的是( )
3Y(g),该反应的反应速率(v)与时间(t)的关系如图所示,已知t2 min时容器内有1.5 mol Y。下列叙述正确的是( )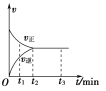
A. t1 min时,只有正反应发生
B. t2~t3 min内,v(X)正=0,反应已经停止
C. 0~t2 min内,v(X)=
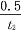 mol·L-1·min-1
mol·L-1·min-1D. 若t3 min时升高温度,则反应速率不变
-
科目: 来源: 题型:
查看答案和解析>>【题目】某无色透明溶液可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-等,取该溶液进行如下实验:
①用蓝色石蕊试纸检测该溶液,试纸显红色;
②取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇到空气立即变为红棕色;
③取溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④取溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤取实验④后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。
请回答下列问题:
(1)在实验①中,下图所示的操作中正确的是________________(填代号)。

(2)根据上述实验判断原溶液中肯定存在的离子是__________,肯定不存在的离子是_________。
(3)写出与②和③两个实验有关的离子方程式:
②______________________________,③_______________________________。
相关试题

