【题目】在一定条件下发生下列反应,其中反应后固体质量增重的是
A. H2还原三氧化钨(W03)B. 铝与氧化铁发生铝热反应
C. 锌粒投入硫酸铜溶液中D. 过氧化钠吸收二氧化碳
参考答案:
【答案】D
【解析】
A、H2还原三氧化钨(W03),固体由WO3变成W,质量减少,故A错误;B、铝与氧化铁发生铝热反应生成氧化铝和铁,固体质量不变,故B错误;C、锌粒投入硫酸铜溶液中生成铜和硫酸锌,相对原子质量锌为65,铜为64,由锌变成铜质量减小,故C错误;D、过氧化钠吸收二氧化碳生成碳酸钠和氧气,2Na2O2+2CO2=2Na2CO3+O2,1molNa2O2变成1molNa2CO3质量增大,故D正确;故选D。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知:(1)Zn(s)+
 O2(g)===ZnO(s) ΔH=-348.3 kJ·mol-1
O2(g)===ZnO(s) ΔH=-348.3 kJ·mol-1(2)2Ag(s)+
 O2(g)===Ag2O(s) ΔH=-31.0 kJ·mol-1
O2(g)===Ag2O(s) ΔH=-31.0 kJ·mol-1则Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s)的ΔH等于
A.-317.3 kJ·mol-1 B.-379.3 kJ·mol-1
C.-332.8 kJ·mol-1 D.317.3 kJ·mol-1
-
科目: 来源: 题型:
查看答案和解析>>【题目】燃煤烟气的脱硫(除SO2)技术和脱硝(除NOx)技术是环境科学研究的热点。下面是目前科学家正致力于研究的三种燃煤烟气脱硫和脱硝的方法。
(1)方法I:用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4。氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2 + H2O=(NH4)2SO3 (NH4)2SO4+ SO2 + H2O=2 NH4HSO3
①为了提高燃煤烟气中SO2去除率,可以采取的措施有:使燃煤烟气与氨水充分接触和______。
②燃煤烟气中含有大量的CO2,但在脱硫过程中,不需要先除去燃煤烟气的CO2原因是___________。
(2)方法II:用电化学原理将SO2转化为重要的化工原料H2SO4进行脱硫,装置如图所示。

①写出通入SO2的电极的电极反应式:________。
②为使该脱硫过程稳定持续进行,硫酸溶液的浓度应维持不变,则通入的O2和加入的H2O的质量比为_________。
(3)方法Ⅲ:用乙烯作为还取剂将氨的氧化物还原为N2进行脱硝,其机理如图,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图所示。


①写出该脱硝过程中乙烯和NO2反应的化学方程式:________________。
②如图,当负载率一定,达到某温度时脱硝率最高,而后却随着温度的升高脱硝率反而降低,其原因是__________;要达到最佳脱硝效果,应采取的条件是_________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】第三周期元素中,微粒半径最大的是
A.NaB.Na+C.S2-D.Cl-
-
科目: 来源: 题型:
查看答案和解析>>【题目】决定元素种类的微粒是( )。
A. 质量数 B. 中子数
C. 核外电子数 D. 质子数
-
科目: 来源: 题型:
查看答案和解析>>【题目】25 ℃、101 kPa时,强酸与强碱的稀溶液中发生中和反应的中和热为57.3 kJ·mol-1,则下列描述正确的是
A. KOH(aq)+
 H2SO4(aq)===
H2SO4(aq)=== K2SO4(aq)+H2O(1) ΔH=-57.3 kJ·mol-1
K2SO4(aq)+H2O(1) ΔH=-57.3 kJ·mol-1B. NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(1) ΔH=+57.3 kJ·mol-1
C. H2SO4和Ca(OH)2反应的中和热为ΔH=2×(-57.3) kJ·mol-1
D. 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室欲用NaOH固体配制1.0mol/L的NaOH溶液240mL.一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤移液 ⑥洗涤 ⑦定容 ⑧冷却 ⑨摇动
(1)配制溶液时,其正确的操作顺序为(填序号).本实验必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、、 .
(2)某同学欲称量NaOH的质量,先用托盘天平称量烧杯的质量,托盘天平平衡后的状态如图所示.烧杯的实际质量为g,要完成本实验该同学应称量g NaOH.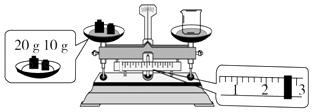
(3)使用容量瓶前必须进行的一步操作是 .
(4)配制过程中,下列操作会引起所配溶液浓度偏高的是(填序号).
A.转移溶液时,有少量溶液洒到容量瓶外面
B.定容时俯视刻度线
C.未冷却至室温就将溶液移入容量瓶中并定容
D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加蒸馏水至刻度线.
相关试题

