【题目】如图是利用废铜屑(含杂质)制备胆矾(硫酸铜晶体)的过程 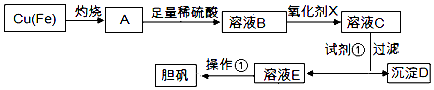
已知:
溶液中被沉淀的离子 | Fe3+ | Fe2+ | Cu2+ |
完全生成氢氧化物的沉淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
请回答:
(1)下列物质中最适宜做氧化剂X的是(填字母).
A.NaClO
B.H2O2
C.KMnO4
D.FeCl3
(2)加入试剂①是为了调节pH,试剂①可以选择(填化学式).
(3)操作①的名称是 .
(4)沉淀D加入盐酸可以得到FeCl3溶液,关于FeCl3溶液的性质中说法不正确的是 .
A.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
B.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
C.将FeCl3溶液滴加NaOH溶液,将沉淀干燥灼烧,得到Fe(OH)3固体
D.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(5)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉防止FeCl2溶液变质,其原因是(用离子方程式表示).
(6)若用碳电极电解硫酸铜溶液200mL.通电5min后,阴极增重0.64g,则电解后溶液的pH=(溶液体积变化忽略不计).
参考答案:
【答案】
(1)B
(2)CuO或CuCO3或Cu(OH)2
(3)蒸发浓缩、冷却结晶
(4)C
(5)Fe+2Fe3+=3Fe2+
(6)1
【解析】解:(1)氧化剂X是将亚铁离子氧化成铁离子,同时不能引入新的杂质,所以可以用H2O2;
所以答案是:B;(2)加入试剂①是为了调节pH,与溶液中的氢离子反应,同时不能引入新的杂质,试剂①可以选择CuO或CuCO3或Cu(OH)2;
所以答案是:CuO或CuCO3或Cu(OH)2;(3)操作①是从硫酸铜 溶液中获得硫酸铜晶体,其名称是蒸发浓缩、冷却结晶;
所以答案是:蒸发浓缩、冷却结晶;(4)A.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体为氢氧化铁胶体,氢氧化铁胶体能产生丁达尔效应,故A正确;
B.向FeCl3溶液滴加NaOH溶液,生成氢氧化铁红褐色沉淀,故B正确;
C.将FeCl3溶液加热蒸干并灼烧,由于氯化铁水解,最终得到Fe2O3固体,故C错误;
D.向FeCl3溶液中滴加KSCN溶液生成Fe(SCN)3,溶液变为红色,故D正确;
所以答案是:C;(5)实验室保存FeCl2溶液,需加入过量的铁粉防止FeCl2溶液变质,铁粉有还原性,离子方程式为:Fe+2Fe3+=3Fe2+;
所以答案是:Fe+2Fe3+=3Fe2+;(6)用碳电极电解硫酸铜溶液200mL.通电5min后,阴极增重0.64g,阴极为为铜离子放电得铜单质,即生成Cu的物质的量为 ![]() =0.01mol,根据铜和氢离子的关系式Cu~2H+知,氢离子的物质的量为0.02mol,溶液中氢离子浓度为
=0.01mol,根据铜和氢离子的关系式Cu~2H+知,氢离子的物质的量为0.02mol,溶液中氢离子浓度为 ![]() =0.1mol/L,则溶液的pH=lgc(H+)=1;
=0.1mol/L,则溶液的pH=lgc(H+)=1;
所以答案是:1.
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是金属镁和卤素单质(X2)反应的能量变化示意图。下列叙述中,正确的说法有几项 ( )

①Mg(s)所具有的能量高于MgX2(s)所具有的能量
②MgCl2电解制Mg(s)和Cl2(g)是吸热过程
③热稳定性:MgI2>MgBr2>MgCl2>MgF2
④常温下氧化性:F2<Cl2<Br2<I2
A. 1项 B. 2项
C. 3项 D. 4项
-
科目: 来源: 题型:
查看答案和解析>>【题目】某小组同学设想用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾.
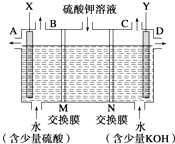
(1)X极与电源的(填“正”或“负”)极相连,氢气从(填“A”、“B”、“C”或“D”)口导出.
(2)离子交换膜只允许一类离子通过,则M为(填“阴离子”或“阳离子”)
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的反应式为 .
(4)若在标准状况下制得11.2L氢气,则生成硫酸的质量是 , 转移的电子数为 . -
科目: 来源: 题型:
查看答案和解析>>【题目】H2O2分解速率受多种因素影响。实验测得70℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是( )
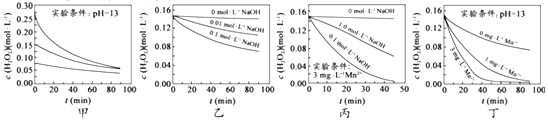
A. 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 图乙表明,其他条件相同时,溶液PH 越小,H2O2分解速率越快
C. 图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快
D. 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列说法中不正确的是( )
A. H与O可形成既含极性共价键又含非极性共价键的化合物
B. 28g由 C2H4和 C3H6组成的混合物中,H原子的数目为4NA
C. 在D218O中,质量数之和是质子数之和的两倍
D. 1mol —CH3中含有的电子数为9NA
-
科目: 来源: 题型:
查看答案和解析>>【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是( )
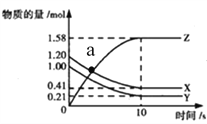
A. 反应的化学方程式为X(g)+Y(g)===Z(g)
B. a点正、逆反应速率相等
C. 反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
D. 反应开始到10s,Y转化率为79%
-
科目: 来源: 题型:
查看答案和解析>>【题目】在容积固定容器中,发生反应2HI(g)
 H2(g)+I2(g), 下列方法中能证明已达到平衡状态的是( )
H2(g)+I2(g), 下列方法中能证明已达到平衡状态的是( )①混合气体的颜色不再变化 ②
 各组分浓度相等 ③
各组分浓度相等 ③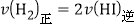
④一个H-H键断裂的同时有两个H-I键断裂 ⑤混合气体的平均摩尔质量不再变化
A. ①④ B. ①②④ C. ①③⑤ D. ①④⑤
相关试题

