【题目】某课外兴趣小组探究利用废铜屑制取CuSO4溶液,设计了以下几种实验方案:
(1)方案一:以铜和浓硫酸反应制备硫酸铜溶液.方案二:将废铜屑在空气中灼烧后再投入稀硫酸.和方案一相比,方案二的优点是;
(2)方案二的实验中,发现容器底部残留少量紫红色固体,再加入稀硫酸依然不溶解,该固体为 .
(3)方案三的实验流程如图1所示:溶解过程中有气体放出,该气体是 . 随着反应的进行,生成气体速度加快,推测可能的原因 . 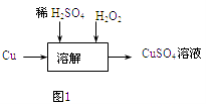
(4)设计实验证明你的推测 .
(5)方案四的实验流程如图2所示:为了得到较纯净的硫酸铜溶液,硫酸和硝酸的物质的量之比应为 . 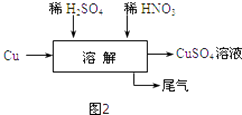
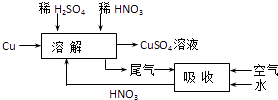
(6)对方案四进行补充完善,设计一个既能防止污染,又能实现物料循环的实验方案(用流程图表示).
参考答案:
【答案】
(1)不产生污染空气的SO2气体,制取等量的CuSO4溶液,消耗的硫酸量少
(2)Cu
(3)O2;反应产生的Cu2+对H2O2分解有催化作用
(4)取H2O2溶液,向其中滴加CuSO4溶液,观察产生气泡的速率是否加快
(5)3:2
(6)
【解析】解:(1)、(2)方案一:第一个方案中放出的有毒气体二氧化硫会造成对空气的污染;第二个方案铜和氧气加热生成氧化铜,氧化铜和硫酸反应产生硫酸铜和水,因此反应过程中没有污染物,且原料的利用率高,方案二的实验中,发现容器底部残留少量紫红色固体,为铜,不溶于稀硫酸;所以答案是:不产生污染空气的SO2气体,制取等量的CuSO4溶液,消耗的硫酸量少;Cu;
(3.)方案三的实验流程如图1中,双氧水反应氧化还原反应生成O2;随着反应的进行,生成气体速度加快,可能是反应产生的Cu2+对H2O2分解有催化作用,所以答案是:O2;反应产生的Cu2+对H2O2分解有催化作用;
(4.)取H2O2溶液,向其中滴加CuSO4溶液,如果产生气泡的速率加快,则证明Cu2+对H2O2分解有催化作用,否则,Cu2+对H2O2分解没有催化作用;所以答案是:取H2O2溶液,向其中滴加CuSO4溶液,观察产生气泡的速率是否加快;
(5.)根据离子方程式,3Cu+2NO3﹣+8H+=3Cu2++2NO↑+4H2O,反应消耗2mol硝酸,生成3mol硫酸铜,故为了得到较纯净的硫酸铜溶液,硫酸和硝酸的物质的量之比应为3:2,所以答案是:3:2;
(6.)设计实验方案时,为防止NO污染空气,应通入空气氧化NO为NO2 , 用水吸收后,生成HNO3再循环利用。
所以答案是:  .
.
-
科目: 来源: 题型:
查看答案和解析>>【题目】研究小组用如图装置制取Cl2 , 证明产生的气体中含有HCl.
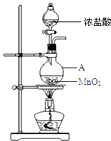
(1)仪器A的名称为;A中反应的离子方程式为;
(2)甲同学将A中产生的气体通入如表溶液:实验序号
试剂
现象
a
紫色石蕊溶液
b
AgNO3溶液
出现白色沉淀
①实验a中的现象为;
②不能证明产生的气体中含有HCl的实验是(填字母序号);
(3)已知将HCl气体通入饱和食盐水中有白色固体析出.乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因;
(4)已知:2S2O32﹣+I2═S4O62﹣+2I﹣ . 丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl.
I.测定X中溶解的Cl2 . 取25.00mL溶液X,加入过量KI溶液,然后用0.04molL﹣1 Na2S2O3溶液滴定生成
的I2 , 达滴定终点时消耗Na2S2O3溶液V mL.
Ⅱ.测定X中Cl元素总量.另取25.00mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl﹣ , 再用0.10molL﹣1 AgNO3溶液滴定所得溶液中的Cl﹣ .
①X中的HClO不会影响I的测定结果,原因是;
②由I、Ⅱ中实验数据可证明A中产生的气体中含有HCl,则Ⅱ中消耗0.10molL﹣1 AgNO3溶液的体积应大于mL(用含V的代数式表示). -
科目: 来源: 题型:
查看答案和解析>>【题目】在2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O反应中( )
A. 氧化剂与还原剂的物质的量之比为1∶8
B. 氧化剂与还原剂的物质的量之比为5∶1
C. 氧化产物与还原产物的物质的量之比为5∶2
D. 氧化产物与还原产物的物质的量之比为2∶5
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列化学用语表示正确的是( )
A.乙酸的结构简式:C2H4O2
B.乙烯的电子式: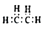
C.硫离子结构示意图: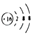
D.氢氧化钡的电离方程式:Ba(OH)2=Ba2++(OH﹣)2 -
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质的水溶液经加热浓缩,蒸干灼烧仍能得到原物质的是( )
A.FeCl3
B.Cu(NO3)2
C.Na2SO3
D.NaAlO2 -
科目: 来源: 题型:
查看答案和解析>>【题目】化学反应原理揭示了不同的物质在水溶液中有不同的行为。请按要求回答下列问题:(已知:H2SO3: Ka1=1.7×10-2,Ka2=6.0×10-8 ; NH3·H2O:Kb=1.8×10-5)
(1)将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈_________性,该溶液中各离子浓度由大到小的顺序为:_____________________________________________,所得溶液中c(H+)- c(OH-)=___________________________(填写表达式)

(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如右图所示(电极材料为石墨)。
① 图中a极要连接电源的(填“正”或“负”)________极;C口流出的物质是________。
②SO32-放电的电极反应式为______________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】25 ℃时,在20 mL 0.1 mol·L-1 NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是
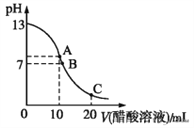
A. 在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B. 在B点:c(OH-)=c(H+),c(Na+)= c(CH3COO-)
C. 在A点:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D. 在C点: c(CH3COO-)+c(CH3COOH)=2c(Na+)
相关试题

