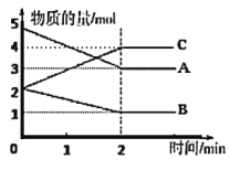
【题目】某反应在体积为5L的恒容密闭容器中进行,在0~3分钟内各物质的量的变化情况如图所示(A,B,C均为气体,且A气体有颜色)。
(1)该反应的化学方程式为______________________________;
(2)反应开始至2分钟时,A的平均反应速率为______________;
(3)下列措施能使该反应加快的是____________(仅改变一个条件)
a.降低温度 b.缩小容积 c.恒容时充入Ar气,增大压强
(4)能说明该反应已达到平衡状态的是__________(填序号)。
①单位时间内生成nmolB的同时生成2nmolC
②单位时间内生成nmolB的同时生成2nmolA
③容器内压强不再随时间而发生变化的状态
④A、B、C的物质的量浓度之比保持3:1:4不变的状态
⑤混合气体的颜色不再改变的状态
⑥混合气体的密度不再改变的状态
⑦υ逆(B)=2υ正(C)
参考答案:
【答案】![]() 0.2mol·L-1·min-1 b ①③④⑤
0.2mol·L-1·min-1 b ①③④⑤
【解析】
(1)由图象可以看出,A、B的物质的量逐渐减小,则A、B为反应物,C的物质的量逐渐增多,所以C为生成物,当反应到达2min时,△n(A)=2mol,△n(B)=1mol,△n(C)=2mol,化学反应中,各物质的物质的量的变化值与化学计量数呈正比,则△n(A):△n(B):△n(C)=2:1:2,2min时反应达到平衡状态,说明是可逆反应,所以反应的化学方程式为:2A(g)+B(g)2C(g);
(2)由图象可以看出,反应开始至2分钟时,△n(A)=2mol,A的平均反应速率为:![]() =0.2mol/(Lmin);
=0.2mol/(Lmin);
(3)a.降低温度,化学反应速率减慢,故错误;
b.缩小容积,相当于增大压强,化学反应速率加快,故正确;
c.恒容时充入Ar气,增大压强,参与反应的各物质的浓度不变,化学反应速率不变,故错误;
答案选b;
(4)①单位时间内生成nmolB的同时生成2nmolC,则正逆反应速率相等,反应达平衡状态;
②按反应,始终有单位时间内生成nmolB的同时生成2nmolA,反应不一定达平衡状态;
③反应为气体体积减小的反应,容器内压强不再随时间而发生变化的状态则达到平衡状态;
④A、B、C的物质的量浓度之比保持3:1:4不变的状态,按图中信息可知,则各物质的物质的量保持不变,反应达平衡状态;
⑤只有A气体有颜色,混合气体的颜色不再改变的状态则反应达平衡状态;
⑥恒容条件下所有反应物均为气体,则混合气体的密度始终保持不变,密度不再改变不一定达到平衡状态;
⑦υ逆(B)=2υ正(C),不符合反应化学计量数比例,正逆反应速率不相等,反应没达到平衡状态;
答案选①③④⑤。
-
科目: 来源: 题型:
查看答案和解析>>【题目】铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的“铜腐蚀现象”产生电能,其放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是( )

A. 放电时,Li+透过固体电解质向Cu极移动
B. 放电时,电子从锂电极通过负载流向铜电极
C. 放电时,锂电极为负极,发生氧化反应
D. 用该电池电解饱和食盐水,每产生1mol氯气(2Cl--2e-→Cl2)时,铜极质量改变64g
-
科目: 来源: 题型:
查看答案和解析>>【题目】有失去标签的NaCl、FeCl2、FeCl3、MgCl2四种溶液,只需要一种试剂就可以把它们鉴别开来,这种试剂是( )
A.氨水B.硝酸银溶液C.Na2SO4溶液D.KSCN溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】生产生活中一时一刻也离不开化学物质。下列常见物质属于硫酸盐的是
A.苏打B.明矾C.铁红D.水玻璃
-
科目: 来源: 题型:
查看答案和解析>>【题目】“结晶玫瑰”具有强烈的玫瑰香气,是一种很好的定香剂,其化学名称为“乙酸三氯甲基苯甲酯”,通常以三氯甲基苯基甲醇和醋酸酐为原料制备:
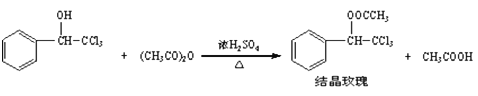
已知:

操作步骤如下:
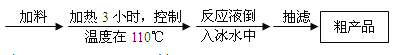
请根据以上信息,回答下列问题:
(1)加料时,应先加入三氯甲基苯基甲醇和酷酸酐,然后慢慢加入浓硫酸并______,待混合均匀后,最适宜的加热方式为______(填“水浴加热”或“油浴加热”)。
(2)粗产品的成分是结晶攻瑰与少量_______(填名称)的混合物,设计了如下方案进行提纯和检验。请完成表中内容:
序号
实验方案
实验现象
结论
①
将粗产品溶解在中,按粗产品、溶剂的质量比为1:__混合,用水浴加热到70℃回流溶剂使粗产品充分溶解
得到无色溶液
②
将步骤1所得溶液____________抽滤
得到白色晶体
③
干燥步骤2所得白色晶体,____________
_____________
白色晶体是结晶玫瑰
(3)4.51g三氯甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰4.68g,则产率是________(小数点后保留两位有效数字)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】扁桃酸衍生物Z是重要的医药中间体,其合成路线如下:

下列叙述正确的是
A. 化合物X、Y、Z和H2发生加成反应后的产物均含2个手性碳原子
B. 两分子X可生成一个含有3个六元环的分子
C. 化合物Z可发生氧化反应、取代反应、加聚反应和缩聚反应
D. 化合物X与NaHCO3和Na2CO3溶液都能反应,且都可以产生CO2气体
-
科目: 来源: 题型:
查看答案和解析>>【题目】某实验小组收集“铜与浓硝酸反应”生成的气体进行探究。试回答下列问题
(1)下图是“铜与浓硝酸反应”的实验装置
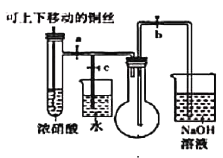
①指出装置中的错误_________________________。
②装置改进后,为了使生成的气体充满烧瓶,实验时先关闭弹簧夹_______,再打开弹簧夹________。
③当气体充满烧瓶后,___________________________,即可使反应停止。
(2)当烧瓶中充满红棕色的气体时停止实验,取下烧瓶,塞好橡皮塞。
①把烧瓶倒扣在装水的水槽中并打开烧瓶的橡皮塞,烧瓶中水面上升,根据化学方程式3NO2+H2O=2HNO3+NO计算烧瓶中溶液的浓度是______mol/L(假设溶质未扩散到水槽,且当时条件下气体的摩尔体积为25L/mol)
②把烧瓶倒扣在装水的水槽中并打开烧瓶的橡皮塞,实验时发现烧瓶中液面上升几乎充满了整个烧瓶,产生这种现象的原因可能是收集的NO2中含有__________。
A.NO B.N2O4 C.O2 D.空气
③小组同学查阅资料发现,NO2溶于水时能生成硝酸和亚硝酸:2NO2+H2O=HNO3+HNO2,为了证明这是造成剩余气体少的主要原因,小组同学把烧瓶中的溶液滴加高锰酸钾溶液,发现高锰酸钾溶液褪色,写出高锰酸钾溶液褪色的离子方程式____________________________。
(3)HNO2是一种不稳定易分解的弱酸:Ⅰ.2HNO2=NO↑+NO2↑+H2O,Ⅱ.3HNO2=HNO3+2NO↑+H2O。为了探究不同温度、浓度下亚硝酸的分解产物,小组同学进行如下实验:
第一步:配制1mol/LNaNO2溶液100mL(标为溶液A)。
第二步:取溶液A分别加水稀释为0.5mol/L、0.2mol/L、0.1mol/L的溶液,依次标为溶液B、C、D。
第三步:分别取两滴管溶液A~D溶液于试管中,塞上橡皮塞后置于不同温度的水中加热5min,再加入一滴管10mol/LH2SO4溶液并立即塞紧橡皮塞,观察生成气体的颜色
水浴温度/℃
A
B
C
D
沸水浴
红棕色
红棕色
红棕色
红棕色
80-70
红棕色
红棕色
红棕色
无色
50-40
红棕色
仅液面上红棕色
无色
无色
20-10
仅液面上红棕色
无色
无色
无色
①第一步实验要用到玻璃仪器有:烧杯、100mL容量瓶、玻璃棒和___________。
②用NaNO2溶液加硫酸而不直接用HNO2溶液的原因是______________。
③通过实验现象得出结论:____________条件下,亚硝酸按反应Ⅰ发生分解。
相关试题

