【题目】有失去标签的NaCl、FeCl2、FeCl3、MgCl2四种溶液,只需要一种试剂就可以把它们鉴别开来,这种试剂是( )
A.氨水B.硝酸银溶液C.Na2SO4溶液D.KSCN溶液
参考答案:
【答案】A
【解析】
A、NaCl、FeCl2、FeCl3、MgCl2四种溶液分别与氨水混合的现象为:无现象、白色沉淀迅速变为灰绿色最后为红褐色、红褐色沉淀、白色沉淀,现象不同,可鉴别,故A正确;
B、均与盐酸不反应,不能鉴别,故B错误;
C、加入硫酸钠溶液,均不反应,不能鉴别,故C错误;
D、KSCN只能鉴别出FeCl3,故D错误;
答案选A。
-
科目: 来源: 题型:
查看答案和解析>>【题目】物质Ⅲ(2,3—二氢苯并呋喃)是一种重要的精细化工原料,其合成的部分流程如下:

下列叙述正确的是
A. 可用溴水可以鉴别化合物Ⅰ和Ⅱ
B. 物质Ⅰ在NaOH醇溶液中加热可发生消去反应
C. 物质Ⅱ中所有原子可能位于同一平面内
D. 物质Ⅲ与足量H2加成所得产物分子中有2个手性碳原子
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列类型的反应一定可以用来设计原电池的是
A.放热反应B.离子反应C.氧化还原反应D.复分解反应
-
科目: 来源: 题型:
查看答案和解析>>【题目】铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的“铜腐蚀现象”产生电能,其放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是( )

A. 放电时,Li+透过固体电解质向Cu极移动
B. 放电时,电子从锂电极通过负载流向铜电极
C. 放电时,锂电极为负极,发生氧化反应
D. 用该电池电解饱和食盐水,每产生1mol氯气(2Cl--2e-→Cl2)时,铜极质量改变64g
-
科目: 来源: 题型:
查看答案和解析>>【题目】生产生活中一时一刻也离不开化学物质。下列常见物质属于硫酸盐的是
A.苏打B.明矾C.铁红D.水玻璃
-
科目: 来源: 题型:
查看答案和解析>>【题目】某反应在体积为5L的恒容密闭容器中进行,在0~3分钟内各物质的量的变化情况如图所示(A,B,C均为气体,且A气体有颜色)。
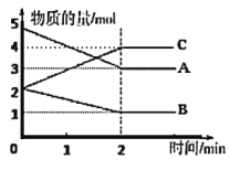
(1)该反应的化学方程式为______________________________;
(2)反应开始至2分钟时,A的平均反应速率为______________;
(3)下列措施能使该反应加快的是____________(仅改变一个条件)
a.降低温度 b.缩小容积 c.恒容时充入Ar气,增大压强
(4)能说明该反应已达到平衡状态的是__________(填序号)。
①单位时间内生成nmolB的同时生成2nmolC
②单位时间内生成nmolB的同时生成2nmolA
③容器内压强不再随时间而发生变化的状态
④A、B、C的物质的量浓度之比保持3:1:4不变的状态
⑤混合气体的颜色不再改变的状态
⑥混合气体的密度不再改变的状态
⑦υ逆(B)=2υ正(C)
-
科目: 来源: 题型:
查看答案和解析>>【题目】“结晶玫瑰”具有强烈的玫瑰香气,是一种很好的定香剂,其化学名称为“乙酸三氯甲基苯甲酯”,通常以三氯甲基苯基甲醇和醋酸酐为原料制备:
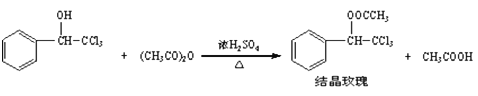
已知:

操作步骤如下:
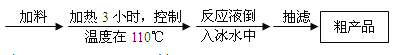
请根据以上信息,回答下列问题:
(1)加料时,应先加入三氯甲基苯基甲醇和酷酸酐,然后慢慢加入浓硫酸并______,待混合均匀后,最适宜的加热方式为______(填“水浴加热”或“油浴加热”)。
(2)粗产品的成分是结晶攻瑰与少量_______(填名称)的混合物,设计了如下方案进行提纯和检验。请完成表中内容:
序号
实验方案
实验现象
结论
①
将粗产品溶解在中,按粗产品、溶剂的质量比为1:__混合,用水浴加热到70℃回流溶剂使粗产品充分溶解
得到无色溶液
②
将步骤1所得溶液____________抽滤
得到白色晶体
③
干燥步骤2所得白色晶体,____________
_____________
白色晶体是结晶玫瑰
(3)4.51g三氯甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰4.68g,则产率是________(小数点后保留两位有效数字)。
相关试题

