【题目】常温下含碳各微粒H2CO3、![]() 和
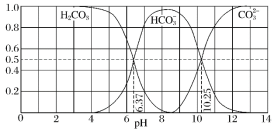
和![]() 存在于CO2和NaOH溶液反应后的溶液中,其物质的量分数与溶液pH的关系如图所示,下列说法错误的是( )
存在于CO2和NaOH溶液反应后的溶液中,其物质的量分数与溶液pH的关系如图所示,下列说法错误的是( )
A.pH=10.25时,c(Na+)=c(![]() )+c(
)+c(![]() )
)
B.为获得尽可能纯的NaHCO3,宜控制溶液的pH为7~9之间
C.根据图中数据,可以计算得到H2CO3第一步电离的平衡常数K1(H2CO3)=10-6.37
D.若是0.1molNaOH反应后所得的1L溶液,pH=10时,溶液中存在以下关系:c(Na+)>c(![]() )>c(
)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
参考答案:
【答案】A
【解析】
A.pH=10.25时,溶质为碳酸钠和碳酸氢钠,碳酸钠溶液中满足物料守恒:![]() ,碳酸氢钠溶液中存在物料守恒:
,碳酸氢钠溶液中存在物料守恒:![]() ,则混合液中
,则混合液中![]() ,故A说法错误;
,故A说法错误;
B.根据图示可知,pH在79之间,溶液中主要存在![]() ,该pH范围内可获得较纯的NaHCO3,故B说法正确;
,该pH范围内可获得较纯的NaHCO3,故B说法正确;
C.根据图象曲线可知,pH=6.37时,H2CO3和![]() 的浓度相等,碳酸的第一步电离的平衡常数
的浓度相等,碳酸的第一步电离的平衡常数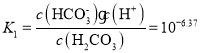 ,故C说法正确;
,故C说法正确;
D.pH=10时的溶液为碱性,则c(OH)>c(H+),溶质为碳酸钠和碳酸氢钠,c(Na+)离子浓度最大,结合图象曲线变化可知:![]() ,OH-为
,OH-为![]() 、
、![]() 水解所得,水解程度微弱,因此离子浓度大小为:
水解所得,水解程度微弱,因此离子浓度大小为:![]() ,故D说法正确;
,故D说法正确;
综上所述,说法错误的是A,故答案为:A。
-
科目: 来源: 题型:
查看答案和解析>>【题目】汽车尾气净化原理为2NO(g)+2CO(g)N2(g)+2CO2(g)ΔH=-746.5kJ·mol-1,如图为在不同初始浓度的CO和不同催化剂Ⅰ、Ⅱ作用下(其他条件相同),体积为2L的密闭容器中n(N2)随反应时间的变化曲线,下列说法正确的是( )
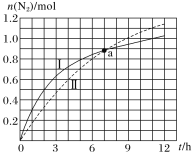
A.a点时,催化剂Ⅰ、Ⅱ作用下CO的转化率相等
B.0~6h内,催化剂Ⅰ的催化效果比催化剂Ⅱ的好
C.0~5h内,催化剂Ⅰ作用下CO的反应速率为0.32mol·L-1·h-1
D.0~12h内,催化剂Ⅱ作用下反应放出的热量比催化剂Ⅰ的多
-
科目: 来源: 题型:
查看答案和解析>>【题目】Cu2O广泛用作颜料和化工生产的催化剂。
Ⅰ.制备Cu2O
(1)电解法:工业上用铜作阳极,钛片为阴极,电解一定浓度的NaOH 溶液可制备氧化亚铜,写出阳极的电极反应式为_____________________
(2)微乳液-还原法:在 100℃ Cu(NO3)2 的水溶液中加入一定体积的 NaOH 水溶液,并搅拌使之混合均匀, 再逐滴加入水合肼的水溶液,直至产生红色沉淀,经抽滤、洗涤和真空干燥,得到Cu2O 粉末。
已知: N2H4(l)+O2(g)=N2(g)+2H2O(l)△H= -akJ/mol
Cu(OH)2(s)=CuO(s)+H2O(l)△H= +bkJ/mol
4CuO(s)=2Cu2O(s)+O2(g)△H= +ckJ/mol
则由N2H4 和Cu(OH)2 反应制备 Cu2O 的热化学方程式为 ________________________。
Ⅱ.工业上用Cu2O 与 ZnO 组成的催化剂可用于工业上合成甲醇: CO(g)+2H2(g)
 CH3OH(g) △H = -90.8 kJ/mol,回答下列问题:
CH3OH(g) △H = -90.8 kJ/mol,回答下列问题:(1)能说明反应CO(g)+2H2(g)
 CH3OH(g)已达平衡状态的是(_______)
CH3OH(g)已达平衡状态的是(_______)A.当反应的热效应△H = -90.8 kJ/mol 时反应达到平衡状态
B.在恒温恒压的容器中,混合气体的密度保持不变
C.在绝热恒容的容器中,反应的平衡常数不再变化
D.在恒温恒容的容器中,气体的平均摩尔质量不再变化
(2)在 T1℃时,体积为 2 L 的恒容容器中充入物质的量之和为 3mol 的 H2 和CO,当起始 n(H2)/n(CO)= 2 时,经过 5min 达到平衡,CO 的转化率为 0.6,则0~5min 内平均反应速率 v (H2)=___;该温度下的平衡常数为__________________ ;若此时再向容器中加入CO(g) 和 CH3OH(g)各 0.4mol,达新平衡时 H2 的转化率将 ______(填“增大”、 “减小”或“不变”);
(3)工业实际合成 CH3OH 生产中,采用下图M点而不是N点对应的反应条件,运用化学反应速率和化学平衡知识,同时考虑生产实际,说明选择该反应条件的理由:________。

-
科目: 来源: 题型:
查看答案和解析>>【题目】磷酸铁锂电池是绿色环保型电池,电池的总反应为:Li1-xFePO4+LixC6= LiFePO4+C6。
(1)LiFepO4中Fe2+的价电子排布图(轨道表达式)为___________,该电池反应物中涉及第二周期的元素的第一电离能由大到小的顺序是___________(用元素符号表示)。
(2)H3PO4和H2CO3中P和C原子的杂化方式_____(填“相同”或“不相同”)。PO43-的空间结构为___________。
(3)石墨可用作锂离子电池的负极材料,Li+嵌人石墨的两层间,导致石墨的层堆积方式发生改变,形成化学式为LixC6的嵌入化合物。某石墨嵌入化合物的平面结构如右图所示,则x=___________;若每个六元环都对应一个L i+,则化学式为___________。

(4)某金属锂的硼氢化物是优质固体电解质,并具有高储氢密度。阳离子为Li+,阴离子是由12个硼原子和12个氢原子所构成的离子团。阴离子在晶胞中位置如图所示,其堆积方式为___________,Li+占据阴离子组成的所有正四面体中心,该化合物的化学式为___________(用最简整数比表示)。假设晶胞边长为a nm,则两个最近的Li+的距离为___________nm。

-
科目: 来源: 题型:
查看答案和解析>>【题目】冰晶石又名六氟铝酸钠(Na3AlF6),白色固体,微溶于水,常用作电解铝工业的助熔剂。工业上用萤石(主要成分是CaF2)、浓硫酸、氢氧化铝和碳酸钠溶液通过湿法制备冰晶石,某化学实验小组模拟工业上制取Na3AlF6的装置图如图(该装置均由聚四氟乙烯仪器组装而成)。
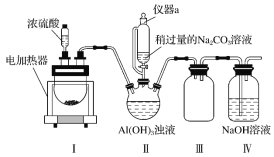
已知:CaF2+H2SO4
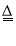 CaSO4+2HF↑
CaSO4+2HF↑(1)装置Ⅲ的作用为__。
(2)在实验过程中,装置Ⅱ中有CO2气体逸出,同时观察到有白色固体析出,请写出该反应的离子方程式:__。
(3)在实验过程中,先向装置Ⅱ中通入HF气体,然后再滴加Na2CO3溶液,而不是先将Na2CO3和Al(OH)3混合后再通入HF气体,其原因是__。
(4)装置Ⅱ反应后的混合液经过过滤可得到Na3AlF6晶体,在过滤操作中确定沉淀已经洗涤干净的方法是__。
(5)萤石中含有少量的Fe2O3杂质,可用装置Ⅰ反应后的溶液来测定氟化钙的含量。具体操作如下:取8.0g萤石加入装置Ⅰ中,完全反应后,将混合液加水稀释,然后加入足量的KI固体,再以淀粉为指示剂,用0.1000mol·L-1 Na2S2O3标准溶液滴定,当出现__现象时,到达滴定终点,消耗Na2S2O3标准溶液40.00mL,则萤石中氟化钙的百分含量为__。(已知:I2+2
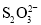 =
=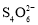 +2I-)
+2I-) -
科目: 来源: 题型:
查看答案和解析>>【题目】三盐(3PbO·PbSO4·H2O,相对分子质量为990)可用作聚氯乙烯的热稳定剂,不溶于水。以200.0t铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如图所示:
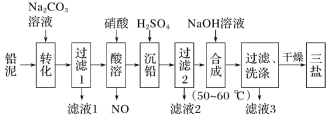
已知:Ksp(PbSO4)=1.82×10-8;Ksp(PbCO3)=1.46×10-13。回答下列问题:
(1)加Na2CO3溶液转化的目的是__。
(2)酸溶时,不直接使用H2SO4溶液的原因可能是__;铅与硝酸在酸溶过程中发生反应的离子方程式为__。
(3)流程中可循环利用的物质是__;洗涤操作时,检验沉淀是否洗涤干净需要的试剂是__。
(4)当沉淀转化达平衡时,滤液l中c(
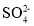 )与c(
)与c(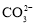 )的比值为__。
)的比值为__。(5)50~60℃时合成三盐的化学方程式为__;若得到纯净干燥的三盐99.0t,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为__。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学与生活、环境密切相关,下列说法错误的是
A.生活中钢铁制品生锈主要是由于发生吸氧腐蚀所致
B.石油的裂化、裂解和煤的干馏都属于化学变化
C.焚烧废旧塑料可有效防止“白色污染”
D.工业废水中的
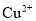 、
、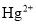 等重金属阳离子可以通过加入
等重金属阳离子可以通过加入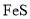 除去
除去
相关试题

