【题目】下列有机物的分离提纯方法正确的是
A.除去乙酸乙酯中含有的乙酸杂质,可以加氢氧化钠溶液充分振荡后,分液。
B.用重结晶的方法分离苯甲酸和氯化钠的混合物
C.将工业酒精直接蒸馏可以获得无水酒精
D.用酸性高锰酸钾溶液可以除掉甲烷中的乙烯杂质。
参考答案:
【答案】B
【解析】
A.乙酸乙酯在氢氧化钠溶液中水解,应用饱和碳酸钠溶液除杂,故A错误;
B.苯甲酸与氯化钠的溶解度随温度变化不同,可用重结晶的方法分离,故B正确;
C.工业酒精含有甲醇,直接蒸馏得到共沸物,不能得到纯净的无水酒精,故C错误;
D.乙烯被氧化生成二氧化碳,引入新杂质,应用溴水除杂,故D错误;
故选B。
-
科目: 来源: 题型:
查看答案和解析>>【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 1 mol FeI2与1 mol Cl2反应时转移的电子数为3NA
B. 2 g H
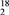 O与D
O与D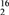 O的混合物中所含中子、电子数目均为NA
O的混合物中所含中子、电子数目均为NAC. 273 K、101 kPa下,28 g乙烯与丙烯混合物中含有C—H键的数目为5NA
D. pH=1的H2SO4溶液10 L,含H+的数目为2NA
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知下列三种气态物质之间的反应:
C2H2(g)+H2(g)
 C2H4(g)①
C2H4(g)①2CH4(g)
 C2H4(g)+2H2(g)②
C2H4(g)+2H2(g)②已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
C(s)+2H2(g)=CH4(g) ΔH=-Q1kJ/mol
C(s)+
 H2(g)=
H2(g)= C2H2(g) ΔH=-Q2kJ/mol
C2H2(g) ΔH=-Q2kJ/molC(s)+H2(g)=
 C2H4(g) ΔH=-Q3kJ/mol
C2H4(g) ΔH=-Q3kJ/molQ1、Q2、Q3均为正值,下列关系正确的是( )
A. Q1>Q3>Q2 B. Q1>Q2>Q3 C. Q2>Q1>Q3 D. Q3>Q1>Q2
-
科目: 来源: 题型:
查看答案和解析>>【题目】N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g)=4NO2(g)+O2(g),△ H>0, T1温度时,向密闭容器中通入N2O5,部分实验数据见表下列说法中不正确的是
时间/s
0
500
1000
1500
c (N2O5) /rnol/L
5.00
3.52
2.50
2.50
A. 500s内用O2表示的平均速率为1.48×10-3mol/(L-s)
B. T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2
C. T1温度下N2O5的平衡转化率为50%
D. 平衡后其它条件不变,将容器的体积压缩到原来的一半,则再平衡时 c(N2O5)>5.00mol/L
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下图及描述,回答下列问题:
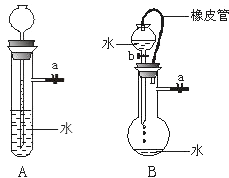
(1)关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示.试判断:A装置是否漏气?(填“漏气”、“不漏气”或“无法确定”) , 判断理由: .
(2)关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶.试判断:B装置是否漏气?(填“漏气”、“不漏气”或“无法确定”) , 判断理由: . -
科目: 来源: 题型:
查看答案和解析>>【题目】Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下。下列说法不正确的是

A. 石墨电极是该电池的正极
B. 石墨电极上发生还原反应
C. Mg电极的电极反应式:Mg-2e-=Mg2+
D. 电池工作时,电子从Mg电极经导线流向石墨电极,再从石墨电极经电解质溶液流向Mg电极
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列对化学平衡移动的分析中,不正确的是( )
①已达平衡的反应C(s)+H2O(g)
 CO(g)+H2(g),当增加反应物物质的量时,则平衡向正反应方向移动;
CO(g)+H2(g),当增加反应物物质的量时,则平衡向正反应方向移动;②已达平衡的反应N2(g)+3H2(g)
 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率升高;
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率升高;③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体总物质的量增大的方向移动;
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动.
A. ①④ B. ①②③ C. ②③④ D. ①②③④
相关试题

