【题目】1774 年瑞典化学家_____在研究软锰矿(主要成分是 MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色的气体,有强烈的刺鼻气味。这种方法至今还是实验室制取的主要方法之一,请写出该反应的化学方程式:__________ 。在实验室,这种黄绿色气体作为尾气通常用_____溶液(填化学式)来吸收, 发生反应的离子方程式是:_________。
参考答案:
【答案】舍勒 MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑+ 2 H2O NaOH 或 KOH Cl2+2OH-=Cl-+ClO-+H2O
MnCl2 + Cl2↑+ 2 H2O NaOH 或 KOH Cl2+2OH-=Cl-+ClO-+H2O
【解析】
1774年,瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,意外地发现生成了一种黄绿色有刺激性气味的气体氯气,反应中MnO2做氧化剂,浓盐酸做还原剂,氯气有毒,常用碱液来吸收,防止污染环境。
1774年,瑞典化学家舍勒在研究软锰矿时,用MnO2与浓盐酸混合加热制得氯气,MnO2与浓盐酸反应生成氯化锰、氯气和水,反应的化学方程式为MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑+ 2 H2O;氯气有毒,常用碱液如NaOH或KOH溶液来吸收,氯气与碱反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:舍勒;MnO2 + 4HCl(浓)
MnCl2 + Cl2↑+ 2 H2O;氯气有毒,常用碱液如NaOH或KOH溶液来吸收,氯气与碱反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:舍勒;MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑+ 2 H2O;NaOH 或 KOH;Cl2+2OH-=Cl-+ClO-+H2O。
MnCl2 + Cl2↑+ 2 H2O;NaOH 或 KOH;Cl2+2OH-=Cl-+ClO-+H2O。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质不属于石油主要成分的是
A. 烷烃B. 烯烃C. 环烷烃D. 芳香烃
-
科目: 来源: 题型:
查看答案和解析>>【题目】下面图(1)和图(2)是A、B两种物质的核磁共振氢谱。已知A、B两种物质都是烃类,都含有6个氢原子。请根据图(1)和图(2)两种物质的核磁共振氢谱图选择出可能属于图(1)和图(2)的两种物质 ( )

A. A是C3H8;B是C6H6 B. A是C4H10;B是C6H6
C. A是C3H6;B是C3H6 D. A是C3H6;B是C2H6
-
科目: 来源: 题型:
查看答案和解析>>【题目】加热 42g NaHCO3 和 Na2CO3 固体混合物,至没有气体放出时,剩余的固体质量是 35.8 g。那么原固体混合物中Na 2CO3 的质量是
A. 25.2g B. 16.8 g C. 10.6 g D. 24.8g
-
科目: 来源: 题型:
查看答案和解析>>【题目】MnO2是碱锰电池材料中最普通的正极材料之一,在活性材料MnO2中加入CoTiO3纳米粉体,可以提高其利用率,优化碱锰电池的性能。
(1)写出基态Mn原子的价电子排布式_____________,基态Mn原子核外电子的运动状态有___种;
(2)①CoTiO3晶体结构模型如图1所示,晶胞参数a=0.53nm。在CoTiO3晶体中1个Ti原子、1个Co原子周围距离最近的O原子数目分别为________个、________个。
②列式表示CoTiO3晶体的密度:________g.cm-3(不必计算出结果,用NA表示阿伏加德罗常数的值)。
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。O2在其催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO- 互为等电子体的分子、离子化学式分别为___________、___________(各写一种)。
(4)三聚氰胺是一种含氮化合物,其结构简式如图2所示。
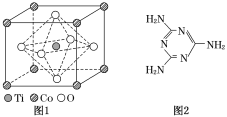
三聚氰胺分子中氮原子轨道杂化类型是____________,1 mol三聚氰胺分子中σ键的数目为________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列反应不属于氧化还原反应的是
A. Zn+2HCl===ZnCl2+H2↑
B. Ca(ClO)2+2HCl===CaCl2+2HClO
C. Pb3O4+8HCl(浓)===3PbCl2+Cl2↑+4H2O
D. 3Cl2+6KOH(浓)
 5KCl+KClO3+3H2O
5KCl+KClO3+3H2O -
科目: 来源: 题型:
查看答案和解析>>【题目】I. 处于下列状态的物质中:
①硫酸钡晶体 ②干冰 ③HCl气体 ④铜 ⑤蔗糖 ⑥熔融的硝酸钾 ⑧NaCl溶液 ⑨醋酸
(1)能导电的是(填序号,下同)______________________;
(2)属于弱电解质_______________;
(3)属于非电解质的是___________________________。
II.某消毒液的主要成分为NaClO(混有少量NaCl),请用相应的化学用语来解释下列事实。
(1)该消毒液可用NaOH 溶液吸收Cl2 制备,化学方程式为_______________________;
(2)该消毒液的pH 约为12,离子方程式为_______________________________________;
(3)向FeSO4溶液中滴入少量该消毒液,溶液变成棕黄色,反应的离子方程式为______________________________________;
(4)该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。每产生1 mol Cl2(标准状况下),转移电子个数约为__________。
相关试题

