【题目】实验创新是中学生最为重要的科学素养,以下是化学兴趣小组的同学在学习“二氧化锰催化过氧化氢分解制氧气实验”后,对实验的创新设计。
实验一:设计新的实验装置
实验过程如下:
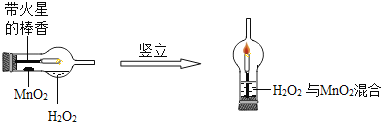
①将一支球形干燥管水平放置,用滴管吸取3mL(密度为1g/mL)质量分数为5%的H2O2加入干燥管的球泡中,再用药匙取0.2gMnO2粉末,加在干燥的进气管的管壁上;②点燃橡胶塞上固定的棒香后,塞紧干燥管并将其竖立,观察现象;
(1)可观察到带火星的棒香立即___;
(2)下列各项是同学们对该创新实验的评价,你认为评价不合理的是___(填序号)
A. 实验所用的仪器、材料及药品均易得到
B. 实验室用的药品用量太大
C. 反应速度太慢,耽误时间
D. 实验现象明显,整个装置好似点燃的灯塔,趣味性强
实验二:寻找新的催化剂
(实验探究)
实验步骤 | 实验现象 |
I、分别量取5mL5%过氧化氢溶液放入A.B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A.B两支试管中插入带火星的木条,观察现象。 | A试管中产生气泡,带火星木条复燃.B试管中无明显现象。 |
Ⅱ、待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃。 |
Ⅲ、将试验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥,称量。 | 所的固体质量为___ |
IV、分别量取5ml5%过氧化氢溶液放入C.D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 |
(实验结论)
(1)A中产生的气体是___;
(2)实验Ⅱ、Ⅲ可以证明:___,再结合实验I和Ⅲ的结论可以证明氧化铁可以作为过氧化氢分解的催化剂。
(3)写出氧化铁(Fe2O3)催化过氧化氢分解的化学方程式:___________________;
(实验评价)
(1)设计实验IV的目的是___;
(2)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是___.
(实验拓展)
查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可做过氧化氢溶液分解的催化剂,下列有关催化剂的说法正确的是___
A.MnO2只能作为过氧化氢溶液分解的催化剂
B. 同一个化学反应可以有多种催化剂
C. 催化剂能使原本不发生的反应也能快速进行
D. 用作催化剂的物质不可能是其它反应的反应物或生成物
参考答案:
【答案】复燃 BC a g 氧气 氧化铁的质量和化学性质在反应前后均没有发生变化 2H2O2![]() 2H2O+O2↑ 氧化铁与二氧化锰哪一个更适合做过氧化氢分解生成氧气的催化剂 二氧化锰更适合做过氧化氢分解生成氧气的催化剂 B
2H2O+O2↑ 氧化铁与二氧化锰哪一个更适合做过氧化氢分解生成氧气的催化剂 二氧化锰更适合做过氧化氢分解生成氧气的催化剂 B
【解析】
实验一:(1)过氧化氢溶液在二氧化锰的催化作用下能快速放出氧气,因为氧气具有支持燃烧的性质,所以能使带到火星的棒香立即复燃;
(2)评价要实事求是,不能随便乱说,实验使用的药品用量不算大;反应速度并不慢,故答案为:BC;
实验二:
实验探究:催化剂反应前后质量不变,故答案:ag;
实验结论:(1)氧气具有助燃性,能使带火星木条复燃,所以由实验现象A试管中产生气泡,带火星木条复燃,可知A中产生的气体是氧气;
(2)实验Ⅱ、Ⅲ证明:氧化铁的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(3)氧化铁催化过氧化氢分解生成水和氧气,化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
实验评价:(1)二氧化锰也能做过氧化氢分解生成氧气的催化剂,所以设计实验Ⅳ的目的是氧化铁与二氧化锰哪一个更适合做过氧化氢分解生成氧气的催化剂;
(2)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰更适合做过氧化氢分解生成氧气的催化剂;
实验拓展:A.MnO2不是只能作为氧化氢溶液分解的催化剂,还可以作其他反应的催化剂,故A错误;B.根据题目的信息可知同一个化学反应可以有多种催化剂,故B正确;C.催化剂不只是加快化学反应的速率,还能减慢化学反应的速率,故C错误;D.用作催化剂的物质可能是其它反应的反应物或生成物,例如二氧化锰是高锰酸钾受热分解制氧气的生成物,故D错误。故本题选B。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A~E为初中化学常见的物质,它们有如图所示的转化关系,图中“﹣”表示相连的物质间能相互发生反应,“→”表示物质间有相应的转化关系,其中A、B都是黑色固体,通常情况下,C是一种能使澄清石灰水变浑浊的气体,D是无色无味的液体,请回答下列问题:

(1)物质C的化学式是________;
(2)写出下列反应的化学方程式 ②__________其基本反应类型为 __________;
(3)写出由D转化为E的化学方程式____________该反应会____________(填“吸热”或“放热” )
-
科目: 来源: 题型:
查看答案和解析>>【题目】水是重要的自然资源。
(1)关于水的认识不正确的是(填序号)______.
A. 自然界的水是纯净物B. 自然界的水是取之不尽,用之不竭的
C. 地球上的总水储量很大,但淡水资源并不充裕D. 工业废水和生活污水的任意排放会造成水体污染
(2)天然水中含有许多杂质,将天然水变成纯水的方法是______.
(3)若用过滤的方法在实验室净化一杯浑浊的河水,必须要使用的玻璃仪器有:烧杯、玻璃棒和______,其中玻璃棒的作用是______.
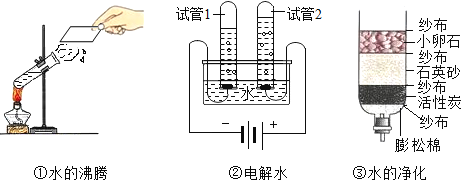
(4)如图所示的3个实验中,发生物理变化的是______(填序号).实验②中试管1所收集的气体为______(填化学式),此实验说明水是由______组成的。实验③中小卵石和石英砂的作用是______,活性炭的作用是______.
-
科目: 来源: 题型:
查看答案和解析>>【题目】碘是紫黑色固体,可以溶解在无色透明的酒精中,形成紫红色的碘酒溶液。
(1)碘的元素符号是___;其颜色和___(填物质名称)的颜色一样。
(2)在生活中常用碘酒对皮肤上的伤口进行消毒,预防伤口发炎。消毒属于___变化。
(3)固体碘受热时升华为碘蒸气,此时碘分子本身没有发生变化,只是___发生变化,因而属于___变化。
(4)固体碘、碘蒸气、碘酒都能使无色的淀粉溶液变蓝,说明___.
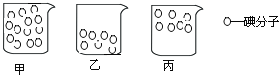
(5)甲、乙、丙三个同学分别画出下面的示意图,表示碘酒中碘分子的分布(酒精分子没有画出).
①如果乙同学的示意图符合事实,应该观察到的现象是___;
②根据你在实验中观察到的现象,___(填甲、乙、丙)的示意图符合事实。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学兴趣课上,同学们对过氧化钠(Na2O2)可以做供氧剂产生了浓厚兴趣,于是在老师的指导下展开了以下探究活动。
(提供资料)① 二氧化碳与过氧化钠反应生成氧气和另一种物质。
② 碳酸钠(Na2CO3)、碳酸氢钠(NaHCO3)与盐酸反应均能生成CO2。
③ 2Na2O2 + 2H2O= 4NaOH + O2↑。
(1)证明二氧化碳与过氧化钠反应产生氧气并收集一瓶氧气。同学们在老师的指导下设计了如下图所示装置。
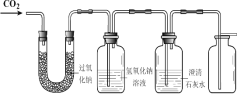
① 如何证明氧气已经收集满 ______。
② 氢氧化钠溶液的作用是除去未反应的二氧化碳,若观察到________ ,说明二氧化碳已经除尽。
(2)探究二氧化碳与过氧化钠反应生成的另一种物质。
(猜想与假设)下面是同学们提出的3种猜想。
猜想1:是氢氧化钠 猜想2:是碳酸氢钠 猜想3:是碳酸钠
通过对反应物中有关元素的组成分析,你认为猜想_____是不正确的,理由是____。
(进行实验)同学们通过以下实验验证了另一种物质,请完成下述实验报告。
实验操作
实验现象
实验结论
取少量CO2与Na2O2反应后的固体于试管中,___________。
有大量气泡产生,澄清石灰水变浑浊。
猜想_____ 是正确的。
(反思与评价)若用人呼出的气体通过上图装置,证明二氧化碳与过氧化钠反应生成了氧气,你是否同意这种做法,并阐述理由____ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图所示实验操作规范的是
A. 将铁钉放入试管
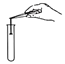 B. 氢气验纯
B. 氢气验纯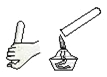
C. 移走蒸发皿
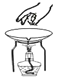 D. 合作滴加液体
D. 合作滴加液体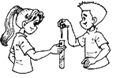
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是五种粒子的结构示意图,下列说法错误的是( )

A.图中粒子共能表示四种元素
B.图中表示阴离子的是c、e
C.图中b粒子的化学符号为Mg2+
D.图中d粒子在化学反应中易失去电子
相关试题

