【题目】煤的综合利用是将煤隔绝空气加强热,使煤分解成许多有用的物质,煤气是其中一种。煤气的主要成分是什么呢?某兴趣小组为此展开了探究。
【查阅资料】(1)煤气中可能含有 CO、CO2、H2、CH4 中的一种或几种。
(2)常温下,氯化钯(PdCl2)溶液吸收 CO 时发生的化学反应方程式为:
CO +PdCl2+H2O ![]() CO2+Pd↓(灰色) +2HCl
CO2+Pd↓(灰色) +2HCl
【实验方案】兴趣小组的同学设计如下装置探究煤气中的成分。
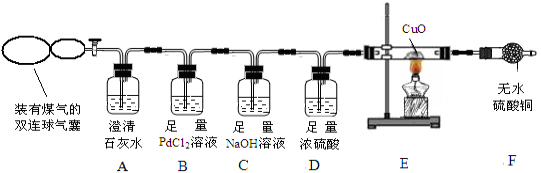
【交流讨论】请回答实验中的有关问题:
(1)实验开始后,A 中无明显现象,说明煤气中不存在____________________;
(2)若煤气中有 CO 存在,则 B中产生的现象是 ;
(3)写出 C 中发生反应的化学方程式__________________________(写一个即可);
D 中浓硫酸的作用是_________________________。
(4)若 F 中无水CuSO4变蓝色,则E中一定发生的化学方程式为 ;
(5)点燃F装置导出的气体,有火焰产生。江枫认为煤气中含 CH4,理由是CH4可以燃烧,CH4燃烧的化学方程式是___________________,老师则认为不能确认煤气中含有 CH4,理由是______________________。为了确定煤气中是否有CH4,老师接着采取的操作方法是 ;观察到的现象是___________________________________。由此验证煤气中一定含有CH4。
参考答案:
【答案】【交流讨论】(1)CO2(2)溶液中产生灰色沉淀(3)NaOH+ HCl ![]() NaCl +H2O 或 2NaOH+ CO2
NaCl +H2O 或 2NaOH+ CO2 ![]() Na2CO3 +H2O 干燥气体或除去气体中的水分
Na2CO3 +H2O 干燥气体或除去气体中的水分
(4)H2 +CuO![]() Cu +H2O (5)CH4 +2O2
Cu +H2O (5)CH4 +2O2 ![]() CO2 +2H2O
CO2 +2H2O
(5)不能确认H2与E装置中的 CuO 是否完全反应或F导出的气体中可能有 H2 或回答出上述 2 点(合理答案即可得分 ) 在火焰上方罩一个内壁附有澄清石灰水的烧杯(合理答案即可得分) 烧杯内壁澄清石灰水变浑浊(或附有一层白色物质)
【解析】
试题分析:(1)实验开始后,A 中无明显现象,说明煤气中不存在二氧化碳;(2) 若煤气中有 CO 存在,根据一氧化碳的性质具有还原性及资料可知, B中产生的现象是溶液中产生灰色沉淀;(3) 写出 C 中发生反应的化学方程式NaOH+ HCl ![]() NaCl +H2O 或 2NaOH+ CO2
NaCl +H2O 或 2NaOH+ CO2 ![]() Na2CO3 +H2O ,D 中浓硫酸的作用是干燥气体或除去气体中的水分 ;(4) 若 F 中无水CuSO4变蓝色,说明有水生成,则E中一定发生的化学方程式为H2 +CuO
Na2CO3 +H2O ,D 中浓硫酸的作用是干燥气体或除去气体中的水分 ;(4) 若 F 中无水CuSO4变蓝色,说明有水生成,则E中一定发生的化学方程式为H2 +CuO![]() Cu +H2O;(5)点燃F装置导出的气体,有火焰产生。江枫认为煤气中含 CH4,理由是CH4可以燃烧,CH4 燃烧的化学方程式是CH4 +2O2
Cu +H2O;(5)点燃F装置导出的气体,有火焰产生。江枫认为煤气中含 CH4,理由是CH4可以燃烧,CH4 燃烧的化学方程式是CH4 +2O2 ![]() CO2 +2H2O;不能确认煤气中含有 CH4,理由是H2与E装置中的 CuO 是否完全反应或F导出的气体中可能有 H2为了确定煤气中是否有CH4,老师接着采取的操作方法在火焰上方罩一个内壁附有澄清石灰水的烧杯;观察到的现象是烧杯内壁澄清石灰水变浑浊,由此验证煤气中一定含有CH4。
CO2 +2H2O;不能确认煤气中含有 CH4,理由是H2与E装置中的 CuO 是否完全反应或F导出的气体中可能有 H2为了确定煤气中是否有CH4,老师接着采取的操作方法在火焰上方罩一个内壁附有澄清石灰水的烧杯;观察到的现象是烧杯内壁澄清石灰水变浑浊,由此验证煤气中一定含有CH4。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组用如图所示装置研究以下两个问题。
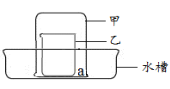
【实验1】可燃物燃烧的条件
步骤1:水槽中放有一定量热水,水面下a处放一小块白磷,此时观察到白磷不燃烧。
步骤2:在乙中放入二氧化锰和过氧化氢溶液,立即将甲倒扣在乙上。
此时观察到甲中水面下降,白磷露出水面, 。
此实验运用对比的方法研究了可燃物燃烧的一个条件是 。
【实验2】浓盐酸的性质
步骤1:a处放一湿润的紫色石蕊试纸,乙中放入浓盐酸,立即将甲倒扣在乙上。此时观察到试纸变为红色。说明浓盐酸具有的性质为 。
步骤2:将试纸取出,立即向水槽中加入滴有酚酞的氢氧化钠溶液,此时观察到红色溶液逐渐变为无色。出现此现象的原因是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某研究性学习小组在验证“碱使酚酞试液变红”的实验时,发现一个意外现象:将酚酞试液滴入某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失了。
【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;
乙同学:可能是NaOH溶液与空气中的CO2发生了反应;
丙同学:可能与NaOH溶液浓度大小有关;
你认为可能还与_________________________________有关(写一条即可)。
【设计实验】三位同学分别设计实验验证自己的猜想:
(1)甲同学设计了如下实验,请你填写下表。
实验步骤
设计这一步骤的目的
实验现象
实验结论
1.将NaOH溶液加热煮沸
溶液变红,过一会儿红色消失
甲同学猜想_______(填“正确”或不正确”)
2.向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方
(2)乙同学设计如图装置进行实验,一段时间后,试管中溶液的红色褪去,于是认定自己的猜想正确。请写出CO2与NaOH溶液反应的化学方程式:________________________。甲同学认为乙同学的实验不够严谨,理由是__________________________________________________。

[注意:若答对第(3)小题奖励4分,化学试卷总分不超过60分。]
(3)丙同学使用了色度传感器测溶液的颜色。他在a、b、c三个比色皿中分别加入等量5%、10%、20%的NaOH1溶液,然后各滴加2滴酚酞试液。溶液颜色的变化曲线如图[说明:溶液无色时色度值(透过率)为100%]。请你观察下图回答问题。
①写出两条规律性结论:_____________________;____________________。

②推测5%的NaOH溶液滴加2滴酚酞试液后褪为无色的时间约为( )
A.小于30s
B.30-90s
C.90-140s
D.140-180s
E.180-280s
F.大于280s
-
科目: 来源: 题型:
查看答案和解析>>【题目】小强在一次查阅资料时得知:二氧化碳与氢氧化钠反应,若二氧化碳过量,生成的碳酸钠会继续与二氧化碳反应生成碳酸氢钠,反应原理为:Na2CO3+CO2+H2O=2NaHCO3.出于好奇,他和同学一起向一定量的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后,低温蒸发结晶,得到了白色固体.
【提出问题】白色固体是什么?
【作出猜想】
猜想Ⅰ:只有Na2CO3;
猜想Ⅱ:可能是Na2CO3和NaOH的混合物;
猜想Ⅲ: _________
【査阅资料】
(1)碳酸氢钠不稳定受热易分解2NaHCO3
 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O(2)Na2CO3与NaOH的热稳定性较好
(3)CaCl2和NaCl的水溶液呈中性
【设计实验】
取一定量的白色固体,加热,若固体质量不变,猜想 _________ 错误;若固体质量减少,则二氧化碳与氢氧化钠反应后, _________ 过量.
【交流讨论】
小方认为,要想知道白色固体中是否有氢氧化钠,可将白色固体配成溶液后,直接用pH试纸测试即可作出判断,你认为是否可行? _________ ;理由是 _________ .
【继续探究】白色固体中是否有氢氧化钠?
实验操作
实验现象
目的/结论
①取白色固体适量配制成溶液.往所得溶液中滴加过量的 _________ ,充分反应后,过滤.
有白色沉淀生成
除去白色固体中的
_________
②取滤液,往滤液中滴入几滴 _________
_________
白色固体中没有氢氧化钠
【交流与反思】
由于氢氧化钠能与二氧化碳反应,所以实验室保存氢氧化钠一定要注意 _________ .
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列化学实验中能达到预期实验结果的是
A. 借助托盘天平和其他手段测定铜锌合金中锌的质量分数为36.25%
B. 用pH试纸测定某未知溶液的pH为5.5
C. 20℃时,配制2%的氢氧化钙溶液
D. 将100g 10%的稀盐酸加热蒸发掉50g水,使得稀盐酸溶质质量分数变成20%
-
科目: 来源: 题型:
查看答案和解析>>【题目】日常生活中发生的下列变化,属于化学变化的是
A.玻璃杯爆裂 B.植物光合作用
C.湿衣服晒干 D.酒精挥发
-
科目: 来源: 题型:
查看答案和解析>>【题目】物质的性质决定用途。下列因果关系不成立的是
A.因为氧气能支持燃烧,所以可能作燃料
B.因为氮气化学性质不活泼,所以可用于食品包装袋内防腐
C.因为磷燃烧能产生大量白烟,所以可用于制作烟幕弹
D.因为一氧化碳具有还原性,所以工业上用于炼铁
相关试题

