【题目】(发现问题)某校化学兴趣小组同学在检验二氧化碳气体的实验过程中,意外发现随着二氧化碳气体的持续通入,变浑的石灰水又逐渐变澄清。
(查阅资料1)向澄清石灰水中持续通入二氧化碳,会先后发生以下两个反应:先发生的反应化学方程式为________________________,导致澄清石灰水变浑浊;后发生的反应化学方程式为CO2+H2O+CaCO3=Ca(HCO3)2,其中Ca(HCO3)2常温下可溶,导致浊液又变澄清。
(类比思考)该小组同学又提出:“向NaOH溶液中持续通入CO2是否也会发生类似的反应呢?”
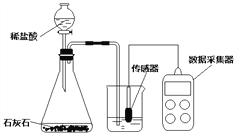
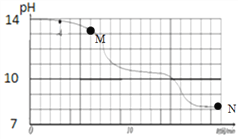
(实验设计)室温(约20℃)下,将10gNaOH溶于80g水中,然后向其中持续平稳的通入二氧化碳气体,同时用数字传感器测定溶液的pH变化,采集数据并绘制图像 。
(查阅资料2)
①根据本实验中数据,溶液中溶质若只有NaOH,溶液pH约为14;若只有Na2CO3,溶液pH约为11.6;若只有NaHCO3,溶液pH约为8.3
②20℃时,NaHCO3溶解度约为9.6g
(反思交流)
(1)实验中,用“分液漏斗”而不用“长颈漏斗”的原因是_______________________;
(2)锥形瓶中发生反应的化学方程式为_______________________________;
(3)根据资料和图像判断:M点溶质应为______________(填化学式,下同),N点溶质应为___________;
(4)同学们多次重复实验,所得实验结果基本一致。实验过程中,同学们发现18min后溶液的pH基本不再变化,则此时烧杯内的现象是____________________;
(5)待pH不再变化后,取适量溶液,向其中滴加几滴稀盐酸,立即产生气泡,该反应的化学方程式为________________________________。
参考答案:
【答案】 CO2 + Ca(OH)2 = CaCO3↓+ H2O 控制反应速率(或控制CO2气流速率) CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ NaOH和Na2CO3 NaHCO3 溶液变浑(或有晶体析出) NaHCO3+HCl=NaCl+ H2O+CO2↑
【解析】【查阅资料1】根据二氧化碳与氢氧化钙溶液反应生成碳酸钙沉淀和水解答;【反思交流】(1)根据分液漏斗能控制反应速率(或控制CO2气流速率)解答;(2)根据碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳解答;(3)(4)根据图像结合【查阅资料2】分析解答;(5)根据碳酸氢钠与稀盐酸反应生成氯化钠、水和二氧化碳解答。【查阅资料1】二氧化碳与氢氧化钙溶液反应生成碳酸钙沉淀和水,反应的化学方程式为CO2 + Ca(OH)2 = CaCO3↓+ H2O;【反思交流】(1)实验中,用“分液漏斗”而不用“长颈漏斗”的原因是控制反应速率(或控制CO2气流速率);(2)碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为CaCO3 + 2HCl = CaCl2 + H2O + CO2↑;(3)由【查阅资料2】①根据本实验中数据,溶液中溶质若只有NaOH,溶液pH约为14;若只有Na2CO3,溶液pH约为11.6;若只有NaHCO3,溶液pH约为8.3。由图可知,M点时13<pH<14,N点时8<pH<9。故M点溶质应为NaOH和Na2CO3;N点溶质应为NaHCO3;(4)由【查阅资料2】②20℃时,NaHCO3溶解度约为9.6g。18min后溶液的pH基本不再变化,则此时烧杯内的现象是溶液变浑(或有晶体析出);(5)碳酸氢钠与稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为NaHCO3+HCl=NaCl+ H2O+CO2↑。
-
科目: 来源: 题型:
查看答案和解析>>【题目】聚合硫酸铁(PFS)是水处理中重要的絮凝剂。下图是以生锈的废铁屑为原料制备PFS的一种工艺流程。
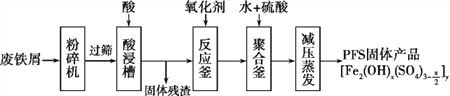
下列说法的错误的是
A. 粉碎过筛的目的是为了增大反应物的接触面积,提高“酸浸”的反应速率
B. 酸浸槽中加入的酸应选择硫酸
C. 酸浸槽中存在的金属阳离子只含Fe2+
D. 相对于常压蒸发,减压蒸发的优点是防止温度过高聚合硫酸铁分解
-
科目: 来源: 题型:
查看答案和解析>>【题目】人类生活离不开能源、资源和营养物质。请结合所学知识回答下列问题
(1)下图表示泰州市家用燃料使用的发展历程(括号内为主要成分)
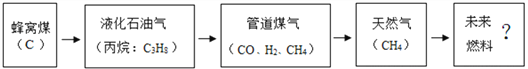
①如果“?”处是氢气,请说出氢气作为未来理想能源的优点之一____________________。
②丙烷燃烧微观示意图如下图所示
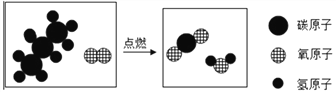
该反应前后不变的粒子是氧原子、_________、________(填化学符号);该反应的化学方程式为____________________________。
(2)水是生命之源,对人类具有重要意义。
①标出水中氢元素的化合价__________。
②发生火灾时,消防员利用高压水枪灭火的主要原理是_________________。
③天然水体多为硬水,是因为其中含有较多的钙离子和镁离子,“镁离子”用化学符号表示为__________。日常生活中可用________________的方法降低水的硬度。
(3)民以食为天,中国的饮食文化博大精深。
①下列食物中富含蛋白质的是__________(填写字母序号)。
A.米饭 B.精肉 C.苹果 D.青菜
②在人体中存在量极少、低于人体体重0.01%的元素称为“微量元素”。人体每日对微量元素的需要量很小但却必不可少。下列属于人体必需微量元素的是_________。
A.铁 B.汞 C.铅 D.碘
-
科目: 来源: 题型:
查看答案和解析>>【题目】A~F 为初中化学常见的六种物质,它们之间有如图所示的转化和反应关系(图中“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去)。其中A、B、C、D、E物质类别不同,E与F物质类别相同,B为磁铁矿的主要成分,D和E用于配制农药波尔多液。
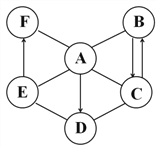
请回答下列问题:
(1)A的化学式__________,E的俗称_____________。
(2)写出下列反应的化学方程式:
①B→C:___________________________________;
②E→F:____________________________________。
(3)上述反应中没有涉及到的基本反应类型是__________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】稀硫酸是一种重要的化学试剂,现用10g 98%的浓硫酸配制10%的稀硫酸,请回答下列问题:
(1)实验的主要步骤有:计算、____________、配制、装瓶并贴标签。
(2)由计算可知,稀释时需加水______________mL(水的密度为:1g/ mL),取水时选用量筒的量程最合适的是_______________(填序号)。
A.25mL B.50mL C.100mL D. 250mL
(3)实验所需要的玻璃仪器有量筒、胶头滴管、烧杯、_______________和试剂瓶。
(4)某课外活动小组为测定某铜锌合金中铜的质量分数,取合金样品10g放入烧杯,向其中逐渐加入10%的稀硫酸,所加稀硫酸与生成氢气质量的关系如图所示。计算:
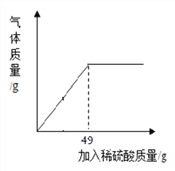
①完全反应后,产生氢气的质量为________g;
②样品中铜的质量分数为___________;(写出计算过程)
-
科目: 来源: 题型:
查看答案和解析>>【题目】碘是甲状腺激素的主要成分。碘元素的部分信息如图。 则下列说法错误的是
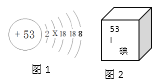
A. 图1表示的微粒是I—
B. 人体中碘是常量元
C. X = 8
D. 碘原子的质子数是53
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图的实验设计能实现其对应实验目的是
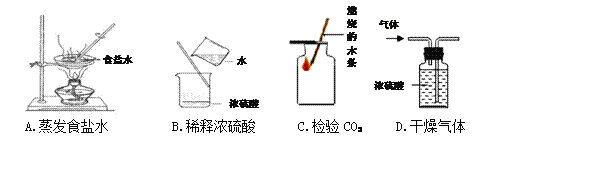
A. A B. 、B C. C D. D
相关试题

