【题目】物质的性质决定其用途,在1766年,英国化学家卡文迪许用锌粒和稀盐酸制得氢气,并把氢气收集到一只倒置在水槽中的装满水的瓶中,最初,氢气被用于飞艇和载人气球.工业上氢气主要用来跟氮气反应制取氨气;还可以用来制备金属;氢气燃烧时,放出大量的热,是等质量汽油燃烧放热的3倍;氢气燃烧后的产物是水,不会造成污染,因此氢气正在成为新兴的能源.
(1)物质的性质决定物质的用途.请写出相应的氢气的性质(用文字表述)
氢气的性质 | 应用 |
①_____ | 用倒置在水槽中的装满水的瓶子收集氢气 |
②_____ | 氢气被用于飞艇和载人气球中 |
③_____ | 氢气正在成为新兴的能源 |
(2)点燃氢气前需要先_____,若操作不当,点燃氢气可能会发生爆炸,请写出氢气爆炸的反应表达式_____,该反应基本类型是_____
(3)氢气正在成为新兴的能源,其主要原因是:_____(写出一条即可)
参考答案:
【答案】 氢气难溶于水 氢气的密度小 氢气燃烧生成水,无污染 检验氢气的纯度 2H2+O2![]() 2H2O 化合反应 燃烧时放出热量多(热值高)或生成物不会污染环境(绿色能源)
2H2O 化合反应 燃烧时放出热量多(热值高)或生成物不会污染环境(绿色能源)
【解析】(1) ①氢气难溶于水,可用排水法收集;②氢气的密度小,可用于填充气球;③氢气燃烧放出大量热,生成物只有水,无污染,是最清洁的燃料;(2)点燃氢气前需要先检验氢气的纯度,若操作不当,点燃氢气可能会发生爆炸,氢气爆炸的反应表达式为2H2+O2 ![]() 2H2O ,该反应基本类型是由一种物质生成两种或两种以上物质的分解反应;(3)氢气正在成为新兴的能源,其主要原因是:燃烧时放出热量多(热值高)或生成物不会污染环境(绿色能源),制取氢气的原料——水,来源广。
2H2O ,该反应基本类型是由一种物质生成两种或两种以上物质的分解反应;(3)氢气正在成为新兴的能源,其主要原因是:燃烧时放出热量多(热值高)或生成物不会污染环境(绿色能源),制取氢气的原料——水,来源广。
-
科目: 来源: 题型:
查看答案和解析>>【题目】20℃时,某物质溶解于水的实验数据如表.则下列叙述正确的是( )
实验序号
水的质量(g)
加入该物质的质量(g)
剩余未溶解固体的质量(g)
①
10
2
0
②
10
3
0
③
10
4
0.4
④
10
5
1.4
A. 溶液质量由大到小的顺序为:④>③>②>①
B. 20℃时10g饱和溶液溶有3.6g该物质
C. 20℃时10g水最多溶解3.6g该物质
D. ①所得溶液的溶质质量分数为20%
-
科目: 来源: 题型:
查看答案和解析>>【题目】小刚收集到一瓶浑浊的长江水,他要模拟自来水厂的净水过程,最终制成自来水.其实验过程如图所示:
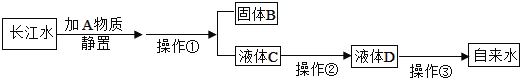
请回答以下问题.
(1)操作①的名称是_____;该操作中用到的玻璃仪器有玻璃棒、烧杯和_____,其中玻璃棒的作用是_____.
(2)操作②主要是用活性炭除去一些异味和色素,其净水原理是利用活性炭的_____作用,该过程主要是_____变化(填“物理”或“化学”).
(3)硬水给生活和生产带来很多麻烦,生活中常常用_____方法来降低水的硬度.
(4)操作③是消毒杀菌,该过程主要是_____变化(填“物理”或“化学”).
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室用溶质质量分数为10%氢氧化钠溶液进行水的电解实验
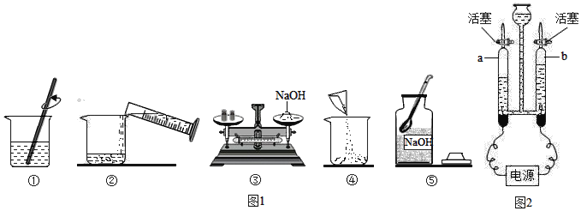
实验一:实验室配制50克质量分数为10%的氢氧化钠溶液,如图1是小军实验操作过程示意图:
(1)图1中一处明显错误的操作是_____(填序号),改正操作后,用上述图示的序号表示配制溶液的正确操作顺序_____.
(2)图1①中玻璃棒搅拌的目的是_____.
(3)称量时,氢氧化钠固体应放于天平_____(填“左”或“右”)盘的烧杯内;量取的需的水(水的密度为1g/cm3),应选择的量筒的规格是_____mL(选填“10”、“100”或“250”).
(4)若最终配制的氢氧化钠溶液的溶质质量分数小于10%,导致该结果可能原因是_____(填序号)
①用量筒量取水时俯视读数 ②配制溶液的烧杯用少量蒸馏水润洗
③氢氧化钠固体不纯 ④盛装溶液的试剂瓶用蒸馏水润洗
实验二:水的电解实验
用如图装置进行水的电解实验,已知氢氧化钠在水的电解实验中,只起到增强水的导电性作用
(5)开始反应前a,b两管内都充满溶液.关闭活塞,接通电源,一段时间后,两管产生的气体如图2所示,则a管下方导线应接电源的_____极(填“正”或“负”).用_____验证b管中的气体,写出电解水的化学反应式:_____.该反应的基本反应类型为_____
(6)说明水是一种化合物的实验事实:_____.
(7)电解后溶液的溶质质量分数_____10%(填“<”、“=”或“>”)
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知元素周期表中第三周期各元素原子结构示意图如图,请回答:
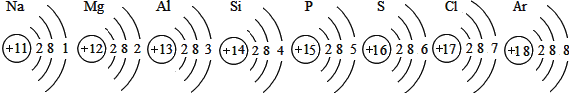
(1)在化学反应中,铝元素的原子容易失去电子变成_____(填“阴”或“阳”)离子;
(2)元素的化学性质与原子结构中的_____数关系密切;
(3)从原子结构方面看,同一周期的元素具有相同的_____数;
(4)在此周期中,各元素的原子结构呈现的变化规律是_____依次递增;
(5)由此可预测原子序数为19的元素原子的电子层数是_____,最外层电子数为_____,与图中_____元素的化学性质相似.
(6)在镁和氧气生成氧化镁的反应中,得到电子的是_____原子,画出镁离子的结构示意图_____,由图可知,氧化镁是由_____(填“分子”“原子”“离子”)构成的.

-
科目: 来源: 题型:
查看答案和解析>>【题目】根据如图物质的溶解度曲线,判断下列说法正确的是

A. 将乙的饱和溶液过滤,能得到不饱和溶液
B. t1℃时,甲溶液、乙溶液的溶质质量相等
C. t2℃185g甲溶液降温至t1℃时,能析出49g晶体
D. 将26%的甲溶液从t2℃降温到t1℃时,溶质质量分数不变
-
科目: 来源: 题型:
查看答案和解析>>【题目】某班学生在老师指导下探究铁与水蒸气的反应。
(1)按图甲装好药品,连接装置(夹持仪器已略去)。其中A装置的作用是________。
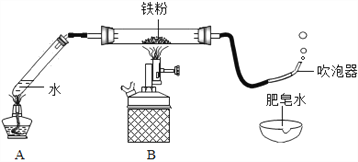
(2)加热一段时间后,灰色铁粉逐渐变黑,吹泡器连续吹出气泡,且气泡向上飞起;用燃着的木条靠近气泡,能产生爆鸣。该气体燃烧的化学方程式为_____________。
(3)同学们讨论后认为:铁与水蒸气反应生成的固体是“铁的一种氧化物”,玻璃管内的黑色固体中还可能含有“过量的铁”。
【查阅资料】铁有三种氧化物(FeO、Fe2O3、Fe3O4),其中FeO接触到空气会立即由黑色变为红棕色;铁的三种氧化物都不与硫酸铜溶液反应。
【实验探究】
实验步骤
实验现象
实验结论
倒出玻璃管中黑色固体,平铺于白纸上
黑色固体不变色
黑色固体中一定没有____(填物质名称)
取上述黑色固体少许,装入试管,加入足量____溶液
________,且有红色固体出现
黑色固体中一定含有__________学科,网
【探究结论】铁与水蒸气发生置换反应,有关的化学方程式是_________。
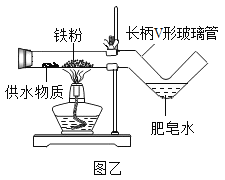
【拓展创新】同学们利用微型仪器“长柄V形玻璃管”改进了图甲装置,设计出图乙装置,并分别选用湿棉花、湿粉笔、芦荟叶、芭蕉茎、氢氧化镁、氢氧化铜等作为供水剂,实验都获得成功。
①甲、乙装置相比,乙装置有很多优点,请你写出一条:__________。
②分析上述供水剂的供水原理,其中正确的是______(填字母)
A.疏松、多孔的物质,有良好的吸水和保水性能
B.新鲜的富水植物,在受热时水分容易释放出来
C.本身不含水的固体物质,不能用作供水剂
相关试题

