【题目】实验室用溶质质量分数为10%氢氧化钠溶液进行水的电解实验
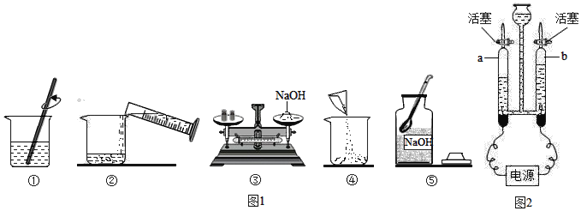
实验一:实验室配制50克质量分数为10%的氢氧化钠溶液,如图1是小军实验操作过程示意图:
(1)图1中一处明显错误的操作是_____(填序号),改正操作后,用上述图示的序号表示配制溶液的正确操作顺序_____.
(2)图1①中玻璃棒搅拌的目的是_____.
(3)称量时,氢氧化钠固体应放于天平_____(填“左”或“右”)盘的烧杯内;量取的需的水(水的密度为1g/cm3),应选择的量筒的规格是_____mL(选填“10”、“100”或“250”).
(4)若最终配制的氢氧化钠溶液的溶质质量分数小于10%,导致该结果可能原因是_____(填序号)
①用量筒量取水时俯视读数 ②配制溶液的烧杯用少量蒸馏水润洗
③氢氧化钠固体不纯 ④盛装溶液的试剂瓶用蒸馏水润洗
实验二:水的电解实验
用如图装置进行水的电解实验,已知氢氧化钠在水的电解实验中,只起到增强水的导电性作用
(5)开始反应前a,b两管内都充满溶液.关闭活塞,接通电源,一段时间后,两管产生的气体如图2所示,则a管下方导线应接电源的_____极(填“正”或“负”).用_____验证b管中的气体,写出电解水的化学反应式:_____.该反应的基本反应类型为_____
(6)说明水是一种化合物的实验事实:_____.
(7)电解后溶液的溶质质量分数_____10%(填“<”、“=”或“>”)
参考答案:
【答案】 ③ ⑤③④②① 加速固体溶解速度 左 250 ②③④ 负 带火星的木条 略 分解 水生成了氢气和氧气 >
【解析】(1)根据所学仪器的使用可知图中一处明显错误的操作是③,天平称量物体时要左物右码;改正操作后,用上述图示的序号表示配制溶液的正确操作顺序按照取药品、称量固体、转移药品固体、量取液体、溶解等步骤,故为⑤③④②①;(2)图①中玻璃棒搅拌的目的是搅拌,加速固体溶解速度;(3)称量时,氢氧化钠固体应放于天平左盘的烧杯内;配制时应选择50 mL的量筒来量取所需水的体积。因为选择量筒量液体时要选择一次量取且量程最小的量筒。(4)若最终配制的氢氧化钠溶液的溶质质量分数小于10%,导致该结果可能原因是氢氧化钠的质量偏少了,或水的量多了。①用量筒量取水时俯视读数,结果是水的量偏少,不符合题意; ②配制溶液的烧杯用少量蒸馏水润洗 ,水的量偏多,符合题意;③氢氧化钠固体不纯 ,导致氢氧化钠偏少,符合题意;④盛装溶液的试剂瓶用蒸馏水润洗,导致水的量偏多符合题意。实验二: (5) 电解水时正极生成的是氧气,负极生成的是氢气,氢气是氧气体积的2倍;由图中信息可知,则a管下方导线应接电源的负极。B管中生成的是氧气,常用带火星木条检验,电解水的化学反应式:2H2O ![]() 2H2↑+ O2↑;该反应的基本反应类型为由一种物质生成两种或两种以上物质的分解反应;(6)据质量守恒定律可知反应前后元素种类不变,水在通电条件下生成氢气和氧气,说明水是一种由氢元素和氧元素组成的化合物;(7)电解水的过程中溶剂减少,溶质不变,所以电解后溶液的溶质质量分数大于10%。
2H2↑+ O2↑;该反应的基本反应类型为由一种物质生成两种或两种以上物质的分解反应;(6)据质量守恒定律可知反应前后元素种类不变,水在通电条件下生成氢气和氧气,说明水是一种由氢元素和氧元素组成的化合物;(7)电解水的过程中溶剂减少,溶质不变,所以电解后溶液的溶质质量分数大于10%。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图所示实验操作正确的是( )
A.
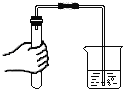 检查装置气密性 B.
检查装置气密性 B. 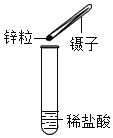 往试管中加入锌粒
往试管中加入锌粒C.
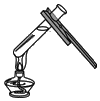 加热液体 D.
加热液体 D.  固体药品的取用
固体药品的取用 -
科目: 来源: 题型:
查看答案和解析>>【题目】20℃时,某物质溶解于水的实验数据如表.则下列叙述正确的是( )
实验序号
水的质量(g)
加入该物质的质量(g)
剩余未溶解固体的质量(g)
①
10
2
0
②
10
3
0
③
10
4
0.4
④
10
5
1.4
A. 溶液质量由大到小的顺序为:④>③>②>①
B. 20℃时10g饱和溶液溶有3.6g该物质
C. 20℃时10g水最多溶解3.6g该物质
D. ①所得溶液的溶质质量分数为20%
-
科目: 来源: 题型:
查看答案和解析>>【题目】小刚收集到一瓶浑浊的长江水,他要模拟自来水厂的净水过程,最终制成自来水.其实验过程如图所示:
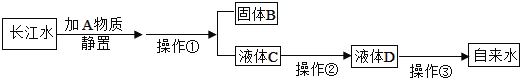
请回答以下问题.
(1)操作①的名称是_____;该操作中用到的玻璃仪器有玻璃棒、烧杯和_____,其中玻璃棒的作用是_____.
(2)操作②主要是用活性炭除去一些异味和色素,其净水原理是利用活性炭的_____作用,该过程主要是_____变化(填“物理”或“化学”).
(3)硬水给生活和生产带来很多麻烦,生活中常常用_____方法来降低水的硬度.
(4)操作③是消毒杀菌,该过程主要是_____变化(填“物理”或“化学”).
-
科目: 来源: 题型:
查看答案和解析>>【题目】物质的性质决定其用途,在1766年,英国化学家卡文迪许用锌粒和稀盐酸制得氢气,并把氢气收集到一只倒置在水槽中的装满水的瓶中,最初,氢气被用于飞艇和载人气球.工业上氢气主要用来跟氮气反应制取氨气;还可以用来制备金属;氢气燃烧时,放出大量的热,是等质量汽油燃烧放热的3倍;氢气燃烧后的产物是水,不会造成污染,因此氢气正在成为新兴的能源.
(1)物质的性质决定物质的用途.请写出相应的氢气的性质(用文字表述)
氢气的性质
应用
①_____
用倒置在水槽中的装满水的瓶子收集氢气
②_____
氢气被用于飞艇和载人气球中
③_____
氢气正在成为新兴的能源
(2)点燃氢气前需要先_____,若操作不当,点燃氢气可能会发生爆炸,请写出氢气爆炸的反应表达式_____,该反应基本类型是_____
(3)氢气正在成为新兴的能源,其主要原因是:_____(写出一条即可)
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知元素周期表中第三周期各元素原子结构示意图如图,请回答:
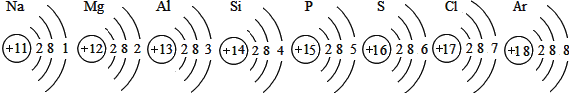
(1)在化学反应中,铝元素的原子容易失去电子变成_____(填“阴”或“阳”)离子;
(2)元素的化学性质与原子结构中的_____数关系密切;
(3)从原子结构方面看,同一周期的元素具有相同的_____数;
(4)在此周期中,各元素的原子结构呈现的变化规律是_____依次递增;
(5)由此可预测原子序数为19的元素原子的电子层数是_____,最外层电子数为_____,与图中_____元素的化学性质相似.
(6)在镁和氧气生成氧化镁的反应中,得到电子的是_____原子,画出镁离子的结构示意图_____,由图可知,氧化镁是由_____(填“分子”“原子”“离子”)构成的.

-
科目: 来源: 题型:
查看答案和解析>>【题目】根据如图物质的溶解度曲线,判断下列说法正确的是

A. 将乙的饱和溶液过滤,能得到不饱和溶液
B. t1℃时,甲溶液、乙溶液的溶质质量相等
C. t2℃185g甲溶液降温至t1℃时,能析出49g晶体
D. 将26%的甲溶液从t2℃降温到t1℃时,溶质质量分数不变
相关试题

