【题目】某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2等。利用该固体废渣制取Cu(NO3)2的部分工艺流程如图所示:
【资料】(1)硝酸受热易分解,且硝酸具有挥发性;
(2)二氧化硅不溶于酸。

(1)Cu、CuO及Cu2O均能溶于稀硝酸。“酸溶”时加入过量的稀硝酸的目的是______。
(2)“酸溶”时,反应温度不宜超过70 ℃,其主要原因是_____________,若保持反应温度为70 ℃,欲加快反应速率还可采取的措施为_____。
(3)“中和”时,试剂A最好选用________________(填字母)。
a.Fe2O3 b.CaCO3 c.Cu(OH)2
(4) “过滤”时所需的玻璃仪器有烧杯、____________、玻璃棒,玻璃棒的作用是_____,所得废渣的主要成分的化学式为______________。
(5)由Cu(NO3)2溶液制Cu(NO3)2晶体的操作方法:蒸发浓缩、________、过滤、冰水洗涤、低温烘干,采用冰水洗涤的目的是_________________。
参考答案:
【答案】 将Cu、CuO及Cu2O完全反应转化为Cu(NO3)2 防止温度过高HNO3分解(或者挥发) 搅拌、将固体废渣粉碎、适当提高硝酸的浓度 c 漏斗 引流 SiO2 冷却结晶(或降温结晶) 洗去杂质的同时减少Cu(NO3)2晶体损耗
【解析】本题在利用固体废渣制取Cu(NO3)2的部分工艺流程的情境下考查了酸的性质,过滤和物质的结晶。
(1) “酸溶”时加入过量的稀硝酸的目的是将Cu、CuO及Cu2O完全反应转化为Cu(NO3)2;
(2)硝酸受热易分解,且硝酸具有挥发性。“酸溶”时,反应温度不宜超过70 ℃,其主要原因是防止温度过高HNO3分解(或者挥发),搅拌、将固体废渣粉碎、适当提高硝酸的浓度都能加快反应速率;
⑶“中和”时,试剂A最好是能与硝酸反应且不引入新的杂质,氢氧化铜能与硝酸反应生成硝酸铜和水。故选C。
⑷ “过滤”时所需的玻璃仪器有烧杯、漏斗、玻璃棒,玻璃棒的作用是引流;固体废渣中的Cu、CuO、Cu2O、SiO2,只有二氧化硅不溶于酸,所得废渣的主要成分的化学式为SiO2;
⑸由Cu(NO3)2溶液制Cu(NO3)2晶体的操作方法:蒸发浓缩、冷却结晶(或降温结晶)、过滤、冰水洗涤、低温烘干,采用冰水洗涤的目的是洗去杂质的同时减少Cu(NO3)2晶体损耗。
-
科目: 来源: 题型:
查看答案和解析>>【题目】研究表明,在同温同压下,相同体积的任何气体中含有的气体分子数相同。在如图所示的密闭容器中有一个理想活塞(滑动自如,且密封性绝对可靠),处在容器体积的
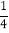 处;其中
处;其中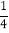 的部分充的是空气,另
的部分充的是空气,另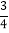 的部分充的是H2和O2的混合气体;当后者用电火花点燃引爆时,活塞先被冲到左边;而当容器内的气体逐渐恢复到原来的温度时,活塞渐渐向右边移动,最终停在容器容积的
的部分充的是H2和O2的混合气体;当后者用电火花点燃引爆时,活塞先被冲到左边;而当容器内的气体逐渐恢复到原来的温度时,活塞渐渐向右边移动,最终停在容器容积的 处,则原来的氢气和氧气的体积比可能是
处,则原来的氢气和氧气的体积比可能是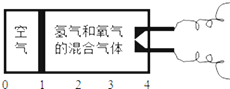
A. 8:1 B. 7:2 C. 4:5 D. 2:7
-
科目: 来源: 题型:
查看答案和解析>>【题目】类比推理是化学学习中的一种重要方法,化学用语是学习化学的重要工具。
(1)尿素[CO(NH2)2]和碳酸氢铵都属于_____________肥,碳酸氢铵中阳离子符号是_____________,两者鉴别的方法是___________________(用化学方程式表示)。
(2)“三酸两碱”中的两碱是指_____________、_____________(填化学式),写出能和稀硫酸发生中和反应的化学方程式:___________________。
(3)利用碘化银[AgI]进行人工降雨,具体地说,就是利用高炮,将碘化银炮弹发射到高空云团的零度层以上,利碘化银在高空中分解生成银单质和碘单质,经过一系列变化实现人工降雨。碘化银中碘元素的化合价为_____________价,写出碘化银分解的化学方程式:_________________。写出另外一种可用于人工降雨的物质名称_____________。
(4)聚乙烯[ ―CH2 ―CH2― ]n和聚氯乙烯[ ―CH2 ―CHCl― ]n都属于塑料。其中可用于包装食品的是_____________。它们_____________有机高分子(填“是”或“不是”)。鉴别方法是___________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学能帮助我们更好地认识生活、改善生活。
(1)紫薯营养丰富,具有特殊的保健功能。下表是100 g紫薯粉的营养成分含量表:
营养成分
含量(每100 g)
营养成分
含量(每100 g)
水分
9.9 g
钙元素
23.00 mg
脂肪
0.2 g
铁元素
1.10 mg
蛋白质
4.8 g
硒元素
0.02 mg
淀粉
82.5 g
其他
……
① 紫薯中能为人体提供能量的营养物质为脂肪、淀粉和_______;
②以上营养成分中_____(填元素符号,下同)是人体中含有的微量元素,______摄入不足,会导致骨质疏松、佝偻病;
③在酶的作用下,淀粉先水解为葡萄糖,葡萄糖再转化为乙醇和二氧化碳。写出葡萄糖转化为乙醇的化学方程式__________________。
(2)创新发展材料技术可推动人类社会进步。
①石墨烯可用作太阳能电池的电极,这里主要利用了石墨烯的________性;
②高铁座椅内填充有聚氨酯软质泡沫。聚氨酯属于________(填字母);
a.金属材料 b.无机非金属材料 c.有机高分子材料
③高铁信息传输系统中使用了光导纤维。光导纤维的主要成分是________(填字母);
a.铜 b.石墨 c.二氧化硅
④基础工程建设中常用到水泥、玻璃、钢材等。在钢材中添加铬、镍等元素的目的是______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学与科学、技术、社会、环境密切相关。
(1) 改善空气质量、保护水土资源是实现美丽中国的基础。
①下列气体的排放会导致酸雨形成的是_____________(填字母,下同)。
a. CH4 b. CO c. SO2
②下列处理废水的方法属于中和法的是_____________。
a. 用熟石灰处理废水中的酸 b. 用铁粉回收废水中的铜
③ 下列做法会造成土壤重金属污染的是_____________。
a. 作物秸杆露天焚烧 b. 废干电池就地填埋 c. 废旧塑料随意丢弃
(2) 新鲜牛肉含蛋白质、脂肪、糖类、维生素A、维生素C、钙、铁等,其中:
① 属于人体所需微量元素的是_____________。
② 属于脂溶性维生素的是_____________。
③ 可为人体提供能量的是_____________、_____________和_____________。
(3)材料的发展与应用促进了人类社会的进步。“复兴号”高铁使用了大量新材料、新技术。
①“复兴号”车厢连接处关键部位特高压过桥线电缆的耐磨护板为增强聚四氟乙烯板。聚四氟乙烯属于_____________(填字母,下同)。

a. 金属材料 b. 无机非金属材料 c. 有机高分子材料
②“复兴号”上网速可达90兆,信息传输使用了光导纤维。光导纤维主要成分是_____________。
a. 石墨 b. 二氧化硅 c. 晶体硅
③“复兴号”车体不用钢材而用镁铝合金型材,是因为镁铝合金_____________。
a. 强度大 b. 密度小 c. 价格便宜
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组进行草酸亚铁晶体(FeC2O42H2O)分解的实验探究。
【猜 想】草酸亚铁晶体分解会产生CO、CO2和H2O三种气体。
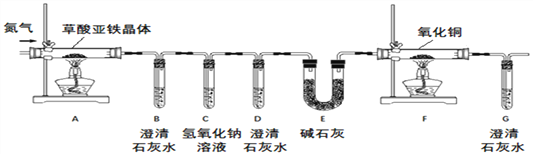
【实验方案】按照上图装置进行实验(夹持装置未画出)。
【问题讨论】(1)实验开始前需要先鼓入一段时间的N2,该操作的目的为_________;
(2)C中氢氧化钠溶液的作用是_______;
(3)E中碱石灰的作用是___________;
【结果分析】(4)定性分析:
①试管D中出现浑浊,证明产物中有_____存在;证明分解产物中存在CO的现象是_____。
②小明认为应增加H装置,则H装置应放在____两个装置之间,若观察到____,则证明有水生成;
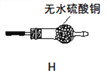
(5)定量分析(假定每一步反应进行完全):取3.6g样品进行上述实验,测得装置A硬质玻璃管中残余1.44g黑色固体FeO,装置F中硬质玻璃管固体质量减轻0.32g,则草酸亚铁晶体(FeC2O42H2O)分解得到的CO2的质量为______。
【反思评价】(6)从环保角度考虑,该套实验装置的明显缺陷是______;
(7)文献显示,FeC2O42H2O受热分解时,固体的质量随温度变化的曲线如下图所示,写出加热到400oC时,FeC2O42H2O受热分解的化学方程式_______。
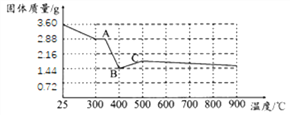
根据图像,若有3.6gFeC2O42H2O在敞口环境中充分加热,最终得到红棕色固体1.60g,则该物质的化学式为_______。由此,你认为进行该实验需要注意的事项是________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】人类社会的发展离不开能源。当今社会,人类利用的能源主要来自化石燃料。
(1)化石燃料蕴藏的能量来源于生物体吸收的_____________; “可燃冰”又称天然气水合物,它是在海底的高压、低温条件下形成的,1体积“可燃冰”可储藏100~200体积的甲烷。下列关于“可燃冰”的叙述中,不正确的是_____________。
A.“可燃冰”不是冰 B.“可燃冰”有可能成为人类未来的重要能源
C.“可燃冰”的可燃成分是甲烷 D.“可燃冰”的实质是水变成的固态油
(2)用来驱动汽车、飞机和轮船的燃料主要是从石油中根据不同沸点范围分馏出来的汽油、航空煤油、柴油等,石油分馏的过程属_____________变化。石油中主要含有碳、氢元素,还含有硫、氮等元素,燃烧时会产生的污染物有_____________(写一种)。
(3)在实验室里,可用稀高锰酸钾溶液检验二氧化硫,现象是________________________;反应的化学方程式为:5SO2+2KMnO4+xH2O═K2SO4+2MnSO4+2H2SO4。其中x的值为_____________,恰好完全反应后,溶液中大量存在的阴离子是_____________(填符号)。
(4)开发和利用清洁高效而又用之不竭的新能源,是21世纪人类面临的重要课题。2006年1月起,我国部分地区推广使用乙醇汽油。乙醇可利用农作物发酵制得,农作物在催化剂作用下转化为葡萄糖(C6H12O6),然后葡萄糖在酒化酶的作用下分解为乙醇和二氧化碳,写出葡萄糖分解为乙醇的化学方程式_________。
(5)科学家用转基因的方法培育出一种“食电”细菌,它“吃进”电能,把二氧化碳和水转化为甲烷等物质,能量转化率高达80%,下列说法中正确的是_____________。
A.细菌“食电”过程能释放出氧气 B.上述反应属于化合反应
C.这种方法能缓解白色污染 D.“食电”细菌不属于生物
相关试题

