【题目】某同学进行如图两个实验。
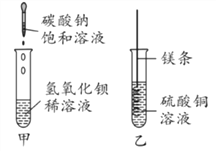
(1)甲实验中反应的化学方程式为________________________________。
(2)乙实验观察到的现象是__________________,溶液由蓝色变成无色。
(3)把甲、乙反应后的溶液倒入同一烧杯,发现有白色沉淀生成。他决定对白色沉淀的成分进行探究。
(查阅资料)硫酸钡不溶于酸。
(提出猜想)白色沉淀为:Ⅰ.________;
Ⅱ.Mg(OH)2和BaSO4;
Ⅲ.Mg(OH)2和MgCO3。
(实验方案)
实验操作 | 实验现象与结论 |
过滤、洗涤白色沉淀备用;向白色沉淀加入盐酸至过量 | ①若沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化学反应方程式为__________________。 ②若________________且无气体产生,猜想Ⅱ成立。 ③若沉淀完全溶解,____________,猜想Ⅲ成立。 |
(反思评价)如果猜想Ⅲ成立,产生此结果的原因是做甲实验时________________;上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是:_________________。
参考答案:
【答案】 Na2CO3+Ba(OH)2=BaCO3↓+2NaOH 镁条表面有红色固体析出 Mg(OH)2 Mg(OH)2+2HCl=MgCl2+2H2O 沉淀部分溶解 且有气泡产生 碳酸钠过量 甲实验中碳酸钠与氢氧化钡会发生反应,两者不可能同时过量
【解析】(1)根据碳酸钠和氢氧化钡反应生成碳酸钡沉淀和氢氧化钠解答;(2)根据镁和硫酸铜溶液反应,生成铜和硫酸镁解答;(3)【提出猜想】甲溶液中一定有氢氧化钠,还可能有碳酸钠或氢氧化钡;乙溶液中一定含有硫酸镁,二者混合后,产生的白色沉淀中一定有氢氧化镁,还可能有碳酸镁、硫酸钡,因此猜想Ⅰ是Mg(OH)2;【实验方案】①猜想Ⅰ成立,沉淀是氢氧化镁,氢氧化镁与盐酸反应生成氯化镁和水;②根据猜想Ⅱ成立,稀盐酸与氢氧化镁反应、与硫酸钡不反应分析解答;③根据猜想Ⅲ成立,氢氧化镁、碳酸镁都能和盐酸反应分析解答;【拓展与思考】根据甲实验中碳酸钠溶液过量分析解答。(1)碳酸钠和氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,反应的化学方程式为Na2CO3+Ba(OH)2=BaCO3↓+2NaOH;(2)金属活动性顺序,镁可以把铜从其盐溶液中置换出来,镁与硫酸铜反应,生成铜与硫酸镁,乙实验观察到的现象是:镁条表面有红色固体析出;【提出猜想】甲溶液中一定有氢氧化钠,还可能有碳酸钠或氢氧化钡;乙溶液中一定含有硫酸镁,二者混合后,产生的白色沉淀中一定有氢氧化镁,还可能有碳酸镁、硫酸钡,因此猜想Ⅰ是Mg(OH)2;【实验方案】①猜想Ⅰ成立,沉淀是氢氧化镁,氢氧化镁与盐酸反应生成氯化镁和水,反应的化学方程式为Mg(OH)2+2HCl=MgCl2+2H2O;②猜想Ⅱ成立,加入稀盐酸,氢氧化镁溶解、硫酸钡不溶解,现象是沉淀部分溶解,无气体产生;③猜想Ⅲ成立,氢氧化镁、碳酸镁都能和盐酸反应生成可溶性的物质,且碳酸镁和盐酸反应生成二氧化碳,则反应现象是沉淀全部溶解且有气体产生;【反思评价】如果猜想Ⅲ成立,产生此结果的原因是做甲实验时碳酸钠过量;上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是:甲实验中碳酸钠与氢氧化钡会发生反应,两者不可能同时过量。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某种矿石由氧化镁、氧化铁、氧化铜和二氧化硅组成,用它制备氢氧化镁的流程示意图如图所示(已知:二氧化硅不溶于水也不与稀盐酸反应)。
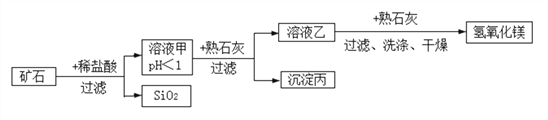
在溶液甲中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子逐步转化为沉淀。该实验条件下,使金属阳离子沉淀的相关pH数据见下表。为保证产品纯度、减少产品损失,并便于操作,所得溶液乙的pH的取值有一定的范围。
氢氧化物
Fe(OH)3
Cu(OH)2
Mg(OH)2
开始沉淀的pH
1.5
4.2
8.6
完全沉淀的pH
3.2
6.7
11.1
下列说法错误的是
A. 溶液甲中共含有三种阳离子
B. 溶液乙的pH的范围是6.7<pH<8.6
C. 沉淀丙的成分是Fe(OH)3、Cu(OH)2、Mg(OH)2
D. 溶液乙中加入熟石灰发生的化学反应方程式:MgCl2+Ca(OH)2= Mg(OH)2↓+CaCl2
-
科目: 来源: 题型:
查看答案和解析>>【题目】CO2、O2、H2是中学化学中常见的气体,请根据下列装置图回答问题:
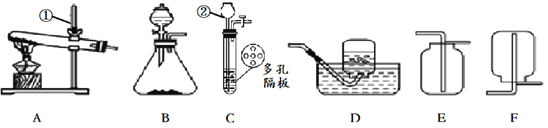
(1)写出图中仪器的名称:①___________,②_____________。
(2)实验室制取CO2的发生装置应选用________(用字母A~F填空)装置,该反应的化学方程式为_____________________。
(3)实验室用A装置制取O2的化学方程式是____________________,实验室用B装置制取O2时,加入的固体起________作用。
(4)实验室可用B装置或C装置制取H2,C装置与B装置比较的优点是_______;收集H2选用的装置是D或F,其原因是______________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知A、B、C、D、E是初中化学中常见的不同类别的物质。它们之间的关系如图所示(“→”表示物质间的转化关系,“—”表示两端的物质能发生化学反应)。A是使用最广泛的金属,C是常用的食品干燥剂,E是配制波尔多液的主要成分之一,其溶液为蓝色,F是由三种元素组成的化合物。请回答下列问题:
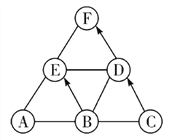
(1)写出化学式:D________,F________。
(2)物质C所属的物质类别是________,选择C作为食品干燥剂的原因有_______________(答两条即可)。
(3)写出A与E反应的化学方程式____________________。
(4)B在生产上的用途有____________,上述反应没有包含的基本反应类型是___________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知NaHCO3在270 ℃时完全分解为碳酸钠、水和二氧化碳,而Na2CO3受热不分解。现有某工厂生产出的一批NaHCO3产品中混有少量的Na2CO3,某兴趣小组同学为了测定该产品中NaHCO3的质量分数,设计了下列两种实验方案。
方案一:样品
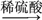 测定生成CO2的质量。
测定生成CO2的质量。(1)NaHCO3俗称_______,本实验采用如图所示的装置,C中盛放的物质是_______。
(2)若无装置E,在其他操作正确的情况下,_______(填“能”或“不能”)准确测定样品中NaHCO3的质量分数。
(3)在其他操作正确的情况下,不能将分液漏斗中的稀硫酸改为稀盐酸的原因是___________。
方案二:样品
 测定剩余固体质量
测定剩余固体质量具体操作步骤如下:
①取一只洁净的坩埚,称得质量为21.2克,再向其中加入样品,称得总质量为41.2克;
②加热盛有样品的坩埚;
③将坩埚充分冷却,称量坩埚和剩余固体的质量;
④多次重复步骤②和③至恒重,称得坩埚和剩余固体的总质量为35.0克。
(4)实验时需要重复“加热、冷却、称量”操作多次,其目的是__________________。
(5)根据题目中的信息,写出NaHCO3完全分解的化学方程式__________________。
(6)根据题意,计算样品中NaHCO3的质量分数为_____________。(请写出计算过程)
-
科目: 来源: 题型:
查看答案和解析>>【题目】某兴趣小组的同学对一包久置的生石灰(CaO)干燥剂产生了好奇,于是他们对这包干燥剂的成分展开了探究。
【提出问题】这包干燥剂是否变质,成分是什么?
【猜想假设】猜想一:全部是CaO; 猜想二:是CaO和Ca(OH)2的混合物;
猜想三:全部是Ca(OH)2; 猜想四:是Ca(OH)2和CaCO3的混合物。
【实验探究】(1)取部分该干燥剂于试管中,加水无放热现象,说明干燥剂中不含 。
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有 。
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以下二种方案。
另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于3支试管中。请你参与实验,并填写表中的空白:
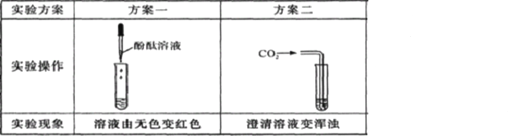
写出方案二发生的化学反应方程式 。
【实验结论】通过以上实验探究,得出猜想 成立。
【拓展迁移】小组同学反思生石灰干燥剂变质原因,认识到实验室保存氧化钙应注意 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图表示化学反应中溶液的颜色变化。下列叙述错误的是
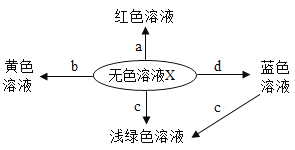
A. 若X是稀硫酸,a可能是紫色石蕊试液 B. 若X是稀硫酸,b可能是氧化物
C. 若X是稀盐酸,c不可能是单质 D. 若X是稀盐酸,d不可能是单质
相关试题

