【题目】甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了如下图所示的四组实验方案。
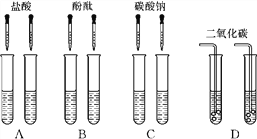
(1)其中能达到实验目的的是________。
(2)在C组实验中发生反应的化学方程式为______________________________________。
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有________(填化学式)生成,滴入酚酞后溶液呈红色。
(4)滴入酚酞后溶液呈红色,说明溶液呈碱性。使溶液呈碱性的物质是什么呢?甲同学进一步推测:溶液中呈碱性的物质可能是碳酸钠、氢氧化钙和________三种物质中的一种,或是三种物质两两混合组成的混合物。
参考答案:
【答案】 C、D Ca(OH)2+Na2CO3===CaCO3↓+2NaOH CaCO3 NaOH
【解析】(1) 氢氧化钠和氢氧化钙溶液与盐酸反应都无明显现象,不能区分;都能使紫色石蕊试液变红,不能区分;氢氧化钙和碳酸钠反应生成沉淀,氢氧化钠和碳酸钠不反应,无明显现象,氢氧化钙和二氧化碳反应生成碳酸钙沉淀,使澄清石灰水变浑浊,氢氧化钠和二氧化碳反应无明显现象,所以能达到实验目的的是C、D。(2)氢氧化钙和碳酸钠反应反应的化学方程式为Ca(OH)2+Na2CO3===CaCO3↓+2NaOH。(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有碳酸钙沉淀生成,化学式为:CaCO3 生成;(4) 滴入酚酞后溶液呈红色,说明溶液呈碱性,盐酸一定反应完;碳酸钠、氢氧化钙和氢氧化钠的溶液都呈碱性,由于氢氧化钙和碳酸钠不共存,所以可能是三种物质中的一种或是三种物质氢氧化钙和氢氧化钠、氢氧化钠和碳酸钠组成的混合物。
-
科目: 来源: 题型:
查看答案和解析>>【题目】小明从小都只习惯吃米饭、吃肉和油炸食品,此外还喜欢喝牛奶,但却不喜欢吃蔬菜,也不习惯吃水果。那么根据你所学的知识判断,小明的饮食习惯中,容易导致哪种营养素缺失
A.油脂 B.维生素 C.蛋白质 D.糖类
-
科目: 来源: 题型:
查看答案和解析>>【题目】在化学课上,老师带来一瓶未知溶液A,已知它是稀盐酸或稀硫酸中的一种。进行如下实验:
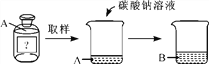
观察到烧杯中的现象是____________。
【提出问题】A是哪一种酸?
老师要求甲、乙同学从反应后的溶液B分别展开探究。
【猜想假设】甲同学:A是稀盐酸;乙同学:A是稀硫酸。
【实验探究】
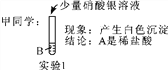
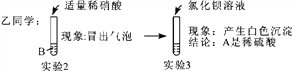
【评价交流】甲同学的实验________(填“能”或“不能”)得出正确结论,乙同学的实验________(填“能”或“不能”)得出正确结论。
实验3发生反应的化学方程式为______________________________________;反应后所得溶液中一定含有的离子是__________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关对一些现象的解释,不正确的是
A.湿衣服在阳光下比在阴凉处干得快是因为温度越高分子运动速率越快
B.物质具有热胀冷缩现象是因为分子或原子的大小可随温度的变化而变化
C.糖是甜的,醋是酸的是因为不同的物质分子具有不同的性质
D.水通电后可以产生氢气和氧气说明分子在化学反应中还可以再分 -
科目: 来源: 题型:
查看答案和解析>>【题目】现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价).则下列说法中不正确的是( )

A.生成氢气的质量:甲>乙>丙
B.相对原子质量:乙>丙>甲
C.金属活动性:乙>甲>丙
D.消耗硫酸的质量:甲>乙>丙
-
科目: 来源: 题型:
查看答案和解析>>【题目】人类文明进步与金属材料的发展关系十分密切,金属在生活生产中有着非常广泛的应用。请回答下列问题:

(1)根据如图金属应用实例推断,金属具有的物理性质有________________(至少答两点);
(2)生铁和钢都是铁的合金,二者性能不同的原因是________________;
(3)厨房中的下列物品所使用的主要材料属于金属材料的是________。
A.陶瓷碗 B.不锈钢炊具 C.橡胶手套 D.铜质水龙头
-
科目: 来源: 题型:
查看答案和解析>>【题目】A~G是初中化学中常见的物质,其相互反应及转化关系如图所示,部分反应条件省略。已知A是易于人体血红蛋白结合的有毒气体,B是赤铁矿的主要成分,C是相对分子质量最小的氧化物,F是最轻的气体。
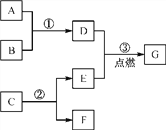
(1)G的化学式为________。
(2)反应③的实验现象是______________________________。
(3)写出相应的化学方程式:②________________________。
相关试题

